
9.C、N、S元素都是生命体的重要组成元素,它们在自然界的平衡已受到较大破坏。C、N、S元素在地球大气圈、岩石圈、水系、生物圈的循环过程中会产生的物质是
①HNO3 ②CO2 ③糖类 ④CH4
A.② B.②③ C.②③④ D.①②③④
|
A.每个分子含有相同的质子数
B.每个分子含有相同的中子数
C.具有相同的相对分子质量
D.若两者质量相同,则所含分子数也相同
33.(8分)[化学-有机化学基础]
有机化学反应因反应条件不同,可生成不同的有机产品。例如:
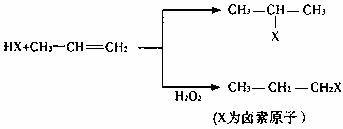
已知G属于芳香族化合物,0.2molG完全燃烧后产生的气体通入到足量的澄清石灰水中,产生沉淀的质量为180g,B中含有一式量为43的羟基,A中不含-CH3。各物质之间的转化关系如下图,请回答下列问题:
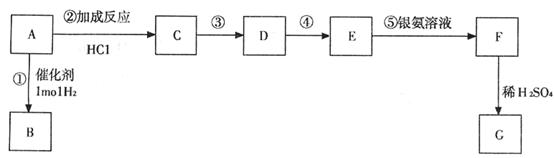
(1)D的结构简式为
(2)反应③④的反应类型分别为 、 。
(3)反应②的化学方程式为(有机物写结构简式,并注明反应条件):
(4)G有多种同分异构体,其中某些物质有下列特征:①其水溶液遇FeCl3溶液呈紫色②与新制备的Cu(OH)2共热有红色沉淀生成 ③分子中有苯环,苯环上有两个取代基且苯环上的一溴代物有两种。写出符合上述条件的G物质可能的结构简式:
32.(8分)[化学-物质结构与性质]
人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属科学家预测为是钛(Ti),它被誉为“未来世纪的金属”。
 试回答下列问题;
试回答下列问题;
(1)Ti元素在元素周期表中的位置是第 周期,第 族;其基态原子的价电子层排布为 ;
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定;
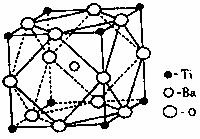
①偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如右图,它的化学式是 ;
②已知Ti3+可形成配位数为6的配合物。现在含钛的两种颜色的晶体,一种为紫色,另一为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的2/3。
则绿色晶体配合物的化学式为 ,绿色晶体中含有的化学键类型是 。
31.(8分)[化学-化学与技术](本模块因我市未选,故未命名)
30.(15分)已知A、B、C是第二周期的非金属元素,其原子序数依次增大,且它们之间可以形成AC和BC以及AC2和BC2分子,D元素是一种短周期元素,它与A、B、C可分别形成总数相等的三种分子。请回答:
(1)写出工业生产中BD3与氧气反应的化学方程式
(2)你认为B、C、D元素形成的化合物之间能否 (选填“能”或“不能”)发生下面反应;BC+BD3→DBC2+D2C,理由是 。
(3)由A、C、D三种元素形成的化合物A2D6C在一定条件下可以转化为A2D4C,写出实现该转化的化学方程式
(4)①恒温恒压下,在一定体积可变的密闭容器中发生下列反应:
4AC(g)+2BC2(g)======4AC2(g)+B2(g)
在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共amol,则AC的转化率是 (用含a的代数式表示)。
②若维持温度不变,在一个与①反应前的起始体积相同且容积固定的密闭容器中发生①所述的化学反应,开始时仍向容器中充入AC和BC2各1mol,达平衡时生成AC2和B2共bmol,将b与①中的a进行比较,则a
b(填“>”、“<”“=”或“不能确定
|
共8个题,考生从中选择2个物理题、1个化学题和1个生物题作答。
29.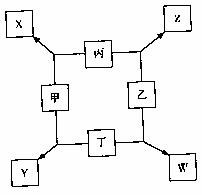 (12分)如图中每方框内的字母代表一种物质,常温常压下,甲、乙、丙、丁均为短周期元素的单质,且丙为金属,其他三种物质均为双原子分子的气体,它们在一定条件下发生图中所示的化合反应。
(12分)如图中每方框内的字母代表一种物质,常温常压下,甲、乙、丙、丁均为短周期元素的单质,且丙为金属,其他三种物质均为双原子分子的气体,它们在一定条件下发生图中所示的化合反应。
①甲与丙按物质的量之比1:2完全反应生成X
②乙与丙按物质的量之比1:2完全反应生成Z,
③乙与丁按物质的量之比1:1完全反应生成W,
④甲与丁按物质的量之比1:2完全反应生成Y,常温下Y为无色液体
请填空:
(1)丁是
(2)X的电子式是
(3)乙与Y反应的离子方程式是
(4)某物质的水溶液中由水电离出的c(H+)=10-12mol/L,则该物质可能是X、Y、Z、W中的 (选填字母)。
28.(15分)面对日益加剧的能源危机,必须下大力气发展各种有效的替代能源。燃料电池具有高效、可再生对环境友好等优点,因而日益受到人们的青睐。
(1)下列物质中可以作为燃料电池的负极反应物的是
A.CH4 B.H2 C.C2H5OH D.O2
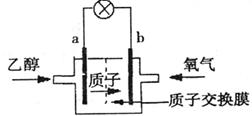 (2)最新研制的一种新型乙醇电池示意图如右,电池的两极分别充入乙醇和氧气,用磺酸类离子作溶剂。则电池工作时
(选填a或b)为负极,b极的电极反应式为
(2)最新研制的一种新型乙醇电池示意图如右,电池的两极分别充入乙醇和氧气,用磺酸类离子作溶剂。则电池工作时
(选填a或b)为负极,b极的电极反应式为
(3)现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6mL)和检验氯气的氧化性。
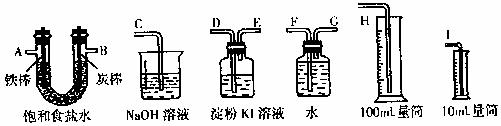
①试从上图中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是:A连 , 接 ,B接 , 接 ;
②能说明氯气具有氧化性的实验现象是
③假定装入的饱和食盐水为50mL,当测得的氢气为5.6mL(标况)时停止通电。摇匀后U形管内的溶液的pH约为 (电解前后溶液体积变化可忽略,假设生成的氯气全部逸出)。
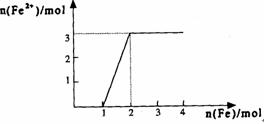
15.向某稀HNO3和Fe(NO3)3的混合溶液中逐渐加入铁粉,产生无色气体,该气体遇空气变红棕色,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如图所示:则稀溶液中HNO3和Fe(NO3)3的物质的量浓度之比为 ( )
A.2:1 B.1:1
C.4:1 D.3:1
|
[必做部分]
14.下列表述中正确的是 ( )
A.任何能使熵值增大的过程都能自发进行
B.已知反应C(s)+1/2O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ
C.反应热的大小与反应物和生成物的键能无关
D.1molNaOH分别和1mol CH3COOH、1mol HNO3反应,放出的热量:CH3COOH<HNO3
13.下列化学方程式或离子方程式正确的是 ( )
A.碳酸氢钠溶液与少量石灰水反应: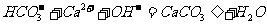
B.单质铜与3mol/L稀硝酸反应: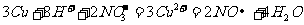
C.苯与硝酸反应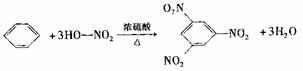
D.铝片跟氢氧化钠溶液反应:Al+2OH-+2H2O=AlO2-+H2↑
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com