
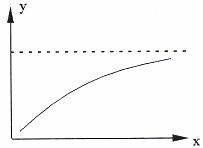
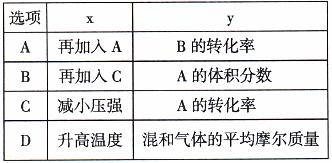
7、在密闭容器中通入A、B两种气体,一定条件下发生反应2A(g)+B(g)  2C(g);△H<O,达平衡后,改变一个条件(x),下列物理量(y)一定符合图中曲线的是
2C(g);△H<O,达平衡后,改变一个条件(x),下列物理量(y)一定符合图中曲线的是
6、下列离子方程式正确的是
A.金属镁溶于硝酸中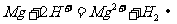
B.次氯酸钙溶液中通入过量二氧化碳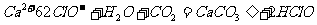
C.NH4HCO3溶液与足量的NaOH溶液混合共热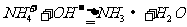
D.氯化亚铁溶液中加入稀硝酸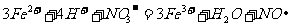
5、在由水电离产生的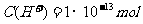 /L的溶液中,一定能大量共存的离子组是
/L的溶液中,一定能大量共存的离子组是
①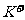 、
、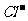 、
、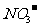 、
、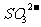 ②
②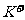 、
、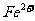 、
、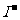 、
、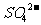 ③
③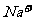 、
、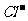 、
、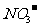 、
、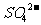
④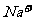 、
、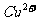 、
、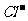 、
、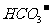 ⑤
⑤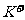 、
、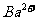 、
、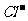 、
、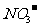
A.①③ B.③⑤ C.③④ D.②⑤
4、最近,科学家用一种称为“超酸”的化合物H(CB11H8Cl60)和C60反应,得到一种新型离子化合物[HC60]+[CB11H6Cl2]-。这个很陌生物质生成的反应原理与我们中学化学中某个反应原理相类似。该反应是
A.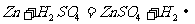 B.
B.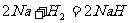
C.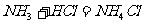 D.
D.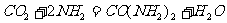
3、三氟化氮(NF3)是无色无味的气体,它是由NH3和F2直接反应制得的:
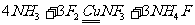 ,下列有关叙述错误的是
,下列有关叙述错误的是
A.F2氧化性比NF3强 B.NF3和NH4F都是还原产物
C.NF3是极性分子 D.NF3中的N是一3价
2、上世纪20年代,有人预言的O4分子,最近由意大利一所大学的科学家制造出了这种空间结构对称的新型氧分子,你认为该氧分子
A.与O2是同分异构体 B.与O3是同素异形体
C.是一种新的氧化物 D.该分子摩尔质量为64克
1、下列分子结构中,原子的最外层电子不能都满足8电子稳定结构的是
A.CS2 B.PCl3 C.NO2 D.CCl4
38.(8分)合成氨原料可以由天然气制取。其主要反应为:
CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1m3(标准状况)CH4按上式完全反应,产生H2 mol。
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为 。
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
|
气体 |
CO |
H2 |
N2 |
O2 |
|
体积(L) |
25 |
60 |
15 |
2.5 |
计算该富氧空气中O2和N2的体积比V(O2)/V(N2)为
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,V(H2)/V(N2)=3︰1 (合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为何
37.(8分)某化学课外小组用含铜96%的废铜屑制取胆矾(五水合硫酸铜)。将铜屑放入稀硫酸中,加热并不断鼓入空气,在氧气作用下便生成硫酸铜。
(1)写出生成硫酸铜的化学方程式 。
(2)现用1kg这种废铜屑理论上能制取胆矾 千克
(3)将胆矾与生石灰、水按质量比依次为1︰0.56︰100混合配制成无机铜杀菌剂波尔多液
① 此波尔多液中Cu2+离子和Ca2+离子的物质的量比为 (最简整数比)。
② 波尔多液有效成分的化学式可表示为CuSO4·xCu(OH)2·yCa(OH)2,此种配比当x=1时,试确定y = 。
36.(10分)有些煤炭中,硫元素是以FeS2 形式存在,在有水和空气及脱硫微生物存在的条件下,发生生物氧化还原反应,其相关的离子方程式为(以下反应都在微生物作用下进行):
2FeS2 + 7O2 + 2H2O = 4H+ + 2Fe2+ + 4SO42-
4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O
FeS2 + 2Fe3+ = 3 Fe2+ + 2S
2S + 3O2 + 2H2O = 4H+ + 2SO42-
请回答下列问题:
(1)总的化学反应方程式为:
(2)FeS2 最终被 氧化,转化为 从煤炭中分离出去
(3)某大型电厂使用的煤炭中含FeS2 的质量分数为1.2%,若每月燃烧该种煤炭100万吨,理论上能回收硫酸 吨;硫酸亚铁 吨。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com