
8.常温下,某溶液由水电离的c(H+)=1×10-13mol·L-1,该溶液可能是 ( )
①硫酸钠溶液 ②氢氧化钠溶液 ③盐酸 ④醋酸钠溶液
A.①④ B.①② C.②③ D.③④
7.下列混合物中,不能用分液漏斗进行分离的是 ( )
A.甘油和水 B.硝基苯和水 C.四氯化碳和水 D.乙酸乙酯和水
6.下列物质中,既有共价键又有分子间作用力的是 ( )
A.氧化镁 B.氦 C.铜 D.液氨
5.合金钢Q460是支撑“鸟巢”的铁骨钢筋,除含有铁元素外,还含有Mn(锰)、Ti(钛)、Cr(铬)、Nb(铌)等合金元素。下列有关说法正确的是 ( )
A.工业上利用热还原法冶炼金属Fe、Cr、Mn
B.Fe位于元素周期表的第四周期、第ⅧB族
C.46 22TiO2、48 22 TiO2、50 22 TiO2互为同位素
D.92 41Nb3+原子核内有51个中子,核外有41个电子
4.有关天然物质水解叙述不正确的是 ( )
A.蛋白质水解的最终产物均为氨基酸
B.可用碘水检验淀粉是否水解完全
C.变质的油脂有难闻的气味,是由于油脂发生了水解反应
D.纤维素水解和淀粉水解得到的最终产物相同
3.对于烃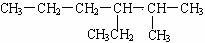 的命名正确的是 ( )
的命名正确的是 ( )
A.2-甲基-3-丙基戊烷 B.3-异丙基己烷
C.2-甲基-3-乙基己烷 D.5-甲基-4-乙基己烷
2.有一只50mL酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处,把滴定管中的溶液全部流下排出,承接在量筒中,量筒内溶液的体积 ( )
A.大于40.0 mL B.为40.0 mL
C.大于10.0 mL D.为10.0mL
1.下列各项中表达不正确的是 ( )
A.F-的结构示意图: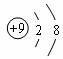 B.NaCl的电子式:
B.NaCl的电子式: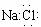
C.CO2分子的结构式:O=C=O D.碳-12原子:12 6C
21.(12分)短周期元素D、E、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为 ;Z的核外电子排布式是 。
(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式 。
(3)D和Y形成的化合物,其分子的空间构型为 ,
D原子的轨道杂化方式是 。
X与Z构成物质的晶体类型为 晶体。
(4)写出一个验证Y与Z的非金属性强弱的离子反应方程式 ;
(5)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是 ;
20.(12分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g) Si3N4(s)+
6CO(g)
Si3N4(s)+
6CO(g)
(1)该反应的氧化剂是 ,其还原产物是 ;
(2)该反应的平衡常数表达式为K= ;
(3)若知上述反应为放热反应,则其反应热△H 0(填“>”、“<”或“=”);升高温度,其平衡常数值 (填“增大”、“减小”或“不变”); 若已知CO生成速率为v(CO)=18mol·L-1·min-1,则N2消耗速率为v(N2)= 。
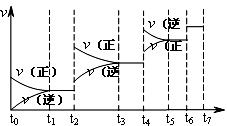
(4)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率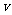 与时间t的关系如右图。图中t4时引起平衡移动的条件可能是
;图中表示平衡混合物中CO的含量最高的一段时间是
。
与时间t的关系如右图。图中t4时引起平衡移动的条件可能是
;图中表示平衡混合物中CO的含量最高的一段时间是
。
(5)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是多少?(写出计算过程) 提示:272 = 729
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com