
4.4℃时,25滴水为amL,则1滴水中含有的水分子数为 ( )
A.aNA/25 B.aNA/(25×18)
C.aNA/(25×20) D.aNA/(1000×22.4)
3.氯气是有毒的,曾被法西斯制成毒气弹用于侵略战争。当这种毒气弹顺风爆炸时,通常可用的防御方法是 ( )
A.人、畜应躲到低洼的地方 B.人、畜应至较高的地方去
C.人、畜应多喝豆浆和牛奶 D.可用氢氧化钠溶液浸湿软布蒙面
2.用NA表示阿伏加德罗常数,下列说法正确的是( )
A.100mL 2mol·L– 1的Na2SO4溶液和400mL 4mol·L– 1的NaCl溶液中c(Na+)不同
B.标准状况下NO与N2的混合气体,2.24L中所含分子数为0.1NA
C.常温常压下,1molD3O+中所含中子数为10NA
D.1molNa2O2与水完全反应,转移电子数为2NA
1.下列变化规律错误的是( )
A.微粒半径:F – < Cl – < Br – < I – B.稳定性:HI< HBr <HCl< HF
C.沸点:HF< HCl < HBr< HI D.阴离子还原性:F – < Cl – < Br – < I –
21. 标准状况下,a L Cl2通入到1 L b mol/L的FeI2溶液中,充分反应后,所得溶液中Fe2+的物质的量浓度与a、b的关系如下表,请完成其余空格。
|
a、b的关系 |
Fe2+的物质的量浓度(mol/L) |
|
a≤22.4b |
① |
|
② |
0 |
|
22.4b≤a≤33.6b |
③ |
20.(10分)A、B、C、D四种元素的原子序数均小于18,其最高正价数依次为1,4,5,7,已知B的原子核外次外层电子数为2。A、C原子的核外次外层电子数为8。D元素的最高价氧化物对应的水化物是已知含氧酸中最强酸,则:
(1)A的离子结构示意图是 ,C的原子结构示意图是 。
(2)C的最高价氧化物对应的水化物与A的氢氧化物生成 种盐,化学式分别为 。
(3)C、D的气态氢化物稳定性由强到弱的顺序是 。
19.(10分)A、B、C、D分别是由两种短周期元素组成的常见微粒(或粒子),这四种微粒中均含有相同数目的电子,且共含有三种元素。其中A中含有5个原子核,它们之间有如下的反应关系:
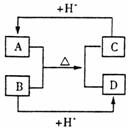
(1)A、D的电子式分别为:A ,D 。
(2)B、C、D三种微粒结合质子能力x>y>z,(x、y、z分别代表B、C、D中的某一种微粒),则x、y、z分别代表的微粒符号为x ,y ,z 。
18.(8分)A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象:
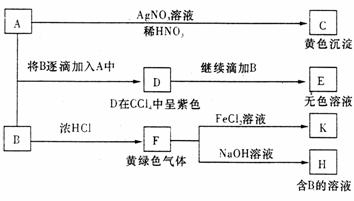
请回答:
(1)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
A→D ;
D→E 。
(2)写出将SO2气体通入K溶液中发生反应的离子方程式: 。
(3)写出由F→H的化学方程式: 。
17.(18分)已知2KCl(固体)+H2SO4(浓)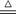 K2SO4+2HCl↑,则实验室用该原理制取HCl的发生装置与实验室制 (填气体名称)相同,将制得HCl气体溶于水即得盐酸,吸收时用倒置的漏斗。现用实验室 O2(以KClO3为原料,MnO2作催化剂)的残渣为原料,先制得HCl,再制取Cl2。
K2SO4+2HCl↑,则实验室用该原理制取HCl的发生装置与实验室制 (填气体名称)相同,将制得HCl气体溶于水即得盐酸,吸收时用倒置的漏斗。现用实验室 O2(以KClO3为原料,MnO2作催化剂)的残渣为原料,先制得HCl,再制取Cl2。
(1)某学生提出的实验步骤依次是:溶解、蒸发、结晶、制气体。其中还缺少的必要步骤是 ;
(2)某学生开列的实验用品为:烧杯、圆底烧瓶、蒸发皿、量筒、集气瓶、分液漏斗、酒精灯、药匙、托盘天平、铁架台(含铁夹、铁圈)、双孔橡皮塞、玻璃导管、橡皮管、火柴、蒸馏水。所缺少的必要试剂是 ,还缺少的必要的实验用品是
(3)写出制得的HCl溶液与MnO2反应制Cl2的离子方程式:
(4)甲同学用51.33 g的MnO2和足量浓盐酸共热制取Cl2的质量为m g。乙同学用200 mL 36.5%的浓盐酸(ρ=1.18 g/cm3)和足量的MnO2共热制取Cl2,得到Cl2的质量为n g。砂考虑反应物的损耗的前提下,m与n的大小关系是m n(填>、<、=)。
(5)多余的Cl2吸收的装置中所用的仪器是 ,试剂是 (选填序号:A. NaOH饱和溶液,B. Ca(OH)2饱和溶液),你选择的理由是
16. 已知A、B、C、D的原子序数都不超过18,它们的离子aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则下列叙述正确的是( )
A. 原子序数:a>b>c>d
B. 离子半径:A(n+1)+>Bn+>C(n+1)->Dn-
C. 离子还原性:A(n+1)+>Bn+,离子氧化性:C(n+1)->Dn-
D. 单质还原性:B>A,单质氧化性:D>C
第Ⅱ卷 非选择题(共52分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com