
29.(8分)可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:
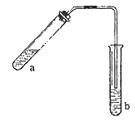
(1)试管a中需加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序是
(2)在加热前应在a中加入沸石,目的是 。
(3)若用含18O的乙醇完成该反应,则反应的化学方程式为 。
(4)试管b中加有饱和Na2CO3溶液,其作用是 。
(5)反应结束后,振荡试管b,静置。观察到的现象是
28.(4分)在试管里加入10%的NaOH溶液2mL,滴入2%的CuSO4溶液4滴-6滴,振荡,观察到的现象是 ,往该试管中加入0.5mL葡萄糖溶液,振荡,将试管加热至沸腾,观察到的现象是 ,此现象说明葡萄糖分子结构中具有的官能团是 (写结构式),因此,葡萄糖的结构简式为 。
27.(8分)牛奶放置时间长了会变酸,这是因为牛奶中含有少量乳糖,在微生物作用下乳糖分解而变成乳酸CH3CH(OH)COOH 。请回答下列问题:
①写出乳酸分子中官能团的名称 ;
②写出乳酸与氢氧化钠溶液反应的化学方程式
③若乳酸在催化剂加热的条件下,也能与氧气发生催化氧化反应,请写出发生反应的化学方程式
④乳酸在浓硫酸作用下,两分子相互反应生成环状结构的物质,写出其生成物的结构简式
26.(6分)A、B和C分别表示含有18个电子的三种微粒。请回答:
(1)A是所有含18个电子的微粒中氧化能力最强的分子,其电子式是 。
(2)B分子中含有4个原子,其结构式是 。
(3)C分子中含有8个原子,其分子式是 。
25.“喷水溶液法”是最近日本科学家研究出的一种使沙漠变绿洲的新技术,它是在沙漠中喷洒一定量的聚丙烯酸酯水溶液,水溶液中的高分子与沙土结合,在地表下30-50 cm处形成0.5cm的隔水层,既能阻止地下的盐分上升,又有拦截、蓄积雨水作用。下列对聚丙烯酸酯说法不正确的是 ( )
A.形成它的小分子结构简式为CH2=CHCOOR(R为烃基)
B.在一定条件下能发生加成反应
C.在一定条件下能发生水解反应
D.没有固定的熔沸点
第Ⅱ卷 (非选择题 50分)
24.将用于2008年北京奥运会的国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成全氟乙丙烯。下列说法错误的是 ( )
A.ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式
B.合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应
C.聚全氟乙丙烯分子的结构简式可能为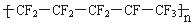
D.四氟乙烯中既含有极性键又含有非极性键
23.已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量
②1molCl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量。
下列叙述正确的是 ( )
A.氢气与氯气反应生成2mol氯化氢气体,需要释放183kJ的热量
B.氢气与氯气反应生成2mol氯化氢气体,需要吸收183kJ的热量
C.氢气与氯气反应生成1mol氯化氢气体,需要吸收183kJ的热量
D.氢气与氯气反应生成1mol氯化氢气体,需要释放183kJ的热量
22.下列除杂质的方法不可行的是 ( )
A.用新制的生石灰,通过加热蒸馏,可以除去乙醇中少量的水
B.用酸性高锰酸钾溶液,通过洗气的方法,可以除去甲烷中的乙烯
C.用苯,通过分液的方法,可以除去溴苯中的溴
D.用氢氧化钠溶液,通过分液的方法,可以除去苯中的乙酸
21.下列关于元素周期表和元素周期律的说法错误的是 ( )
A.Li、Na、K单质的熔点随着核电荷数的增加而降低
B.第二周期元素从Li到F,非金属性逐渐增强
C.卤族元素氢化物的沸点随着核电荷数的增加而升高
D.在元素周期表中第三纵列含有的元素种类最多
20.已知:H+(aq)+ OH-(aq) ==H2O(l);放出热量为57.3kJ。有以下4个化学反应:
①H2SO4(aq)+ 2NaOH(aq) == Na2SO4(aq) + 2H2O(l)
②NH3•H2O(aq)+ HCl(aq) == NH4Cl(aq) + H2O(l)
③H2SO4(aq)+ Ba(OH)2(aq) == BaSO4(s) + 2H2O(l)
④NH3•H2O(aq)+ CH3COOH (aq) == CH3COO NH4 (aq) + H2O(l)
其中放出热量由多到少的顺序正确的是 ( )
A.① = ③ >④ >② B.① = ③ >② >④
C.③ >① >② >④ D.① >③ >② = ④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com