
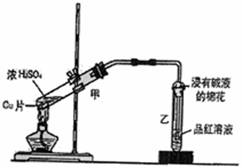
24.(7分)某教师在课堂上用下图所示的装置来验证浓硫酸与铜是否发生反应并探讨反应所产生气体的性质。
请回答下列问题:
(1)通过试管乙中发生的 现象说明了铜和浓硫酸发生了化学反应,并且进一步说明,产生的气体具有 。
(2)写出试管甲中所发生反应的化学反应方程式 。
(3)装置中浸有碱液的棉花的作用是 ,此防范措施也说明产生的气体是 气体(填“酸性”、“中性”或“碱性”), (填“有”或“无”)毒性。
23.(7分)物质W、A、B、x、y、m、n有下图的转化关系。
已知:①W是黑色固体单质;②常温下y是液体,x是无色无味的气体;③A的浓溶液和B的溶液敞口放置在空气中,一段时间后,A溶液的质量减少,B溶液的质量增大。
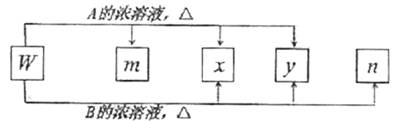
根据以上信息,回答下列问题:
(1)检验y物质的试剂是 (填化学式)。
(2)x的电子式为 ,它是 分子(填“极性”,“非极性”)。
(3)金属铁放到冷的A的浓溶液或B的浓溶液中会发生 现象。
(4)B的浓溶液对皮肤具有强烈的腐蚀性,若不慎粘到皮肤上我们应该采取的处理预案是 。
(5)写出W与A的浓溶液反应的化学方程式 。
22.(10分)A、B、C、D为短周期元素,C、D不在同一周期。B与A可形成两种常温下液态化合物X和Y,其原子个数比分别为1:1和2:1,且分子中电子总数分别为18和10;B与D能形成一种极易溶于水的碱性气体m,B与C能形成极易溶于水的酸性气体n。A、B、D可形成离子化合物Z,其化学式为B4A3D2,它能与烧碱在加热条件下生成m。回答下列问题:
(1)元素名称:A 。
(2)写出Y的结构式 ,m分子结构的空间形状为 ,X分子中共价键的类型有 。
(3)m与n相遇可观察到的现象是 。
(4)①写出B的单质与D的单质反应的化学方程式
。
②写出Z溶液与烧碱溶液加热反应的离子方程式
。
21.(9分)中学化学中有以下常见的5种气体:①O2;②Cl2;③SO2;④NH3。针对这4种气体,回答下列问题(填序号):
(1)能用浓硫酸干燥的有 。
(2)具有刺激性气味的是 ,有颜色的是 ,具有漂白能力的有 。
(3)既能用排水法又能用排空法收集的气体有 。
(4)上述气体中有的能污染大气,对环境造成危害,写出两个环境污染的名词
、 。
(5)NH3和NO2能发生反应生成N2和H2O,在横线上填写各物质的化学计量数。
NH2+ NO2=== N2+ H2O
20.物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌和硝酸均没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
( )
A.1:4 B.1:5 C.2:3 D.2:5
卷Ⅱ(非选择题,共50分)
19.按下图进行实验,试管内装有12mLNO2,然后间歇而缓慢地通入2.5mLO2,下面有关实验最终状态的描述正确的是 ( )
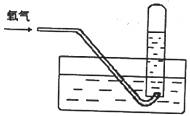
A.试管内气体呈红棕色 B.试管内气体为无色是NO
C.试管内气体为无色是O2 D.试管内液面高度上升,无气体剩余
18.下列操作的生成物中,铁元素的化合价全部呈+3价的是 ( )
A.加热条件下,铁粉与硫粉混合 B.红热的铁丝插入到氧气中
C.铁片加入到浓盐酸中 D.铁片加入到足量稀硝酸中
17.将足量的CO2气体通入下列溶液中,最终产生沉淀的是 ( )
A.CaCl2溶液 B.Ca(OH)2溶液
C.Na2SiO3溶液 D.NaOH溶液
16.浓硫酸具有下列性质:①酸性,②吸水性,③脱水性,④强氧化性。在蔗糖与浓硫酸的“黑面包”实验中,我们观察到的现象有:蔗糖逐渐变黑,体积膨胀,形成疏松多孔的海绵状的固体,同时有刺激性气味的气体产生。通过对上述现象的分析,浓硫酸在该实验中体现的性质有 ( )
A.仅有③ B.①③④ C.②③④ D.①②③④
15.下列离子方程式书写正确的是 ( )
A.碳酸钙和稀硝酸反应 CaCO3+2H+===Ca2++CO2↑+H2O
B.氯化铜溶液和氨水混合 Cu2++2OH-===Cu(OH)2↓
C.铜和稀硝酸反应 Cu+4H++NO-3==Cu2++NO↑+2H2O
D.二氧化硫与水反应 SO2+H2O==2H++SO2-3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com