
15、取100mL18.3mol·L-1浓硫酸与Zn反应,当Zn完全溶解时,生成的气体在标况下的体积为22.4L,将所得的溶液稀释至1L,测得溶液中H+浓度为1mol·L-1,则所生成的气体中SO2与H2的体积比约为( )
A.1:2 B.2:1 C.1:4 D.4:1
14、下列叙述中正确的是( )
A.1moL CO和1molN2所含分子数相等,质量也相等,所以他们所占的体积也一定相同
B.等体积、等物质的量浓度的强碱溶液中,所含的OH-数一定相等
C.22.4LH2和71gCl2反应,恰好生成2moLHCl
D.非标准状况下,1mol某气体的体积可能是22.4L
13、一定条件下,用甲烷可以消除氮氧化物(NO2)的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=―574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=―1160 kJ·mol一1。
下列选项正确的是( )
A.CH4(g)+2NO2(g)= N2(g)+CO2(g)+2H2O(l);△H=―867 kJ·mol-1
B.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ
C.CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子为3.2 mol
D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为1.6 mol
12、下列各组物质稀溶液相互反应,无论前者滴入后者,还是后者滴入前者,反应现象相同,且离子方程相同的是( )
A.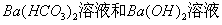 B.
B.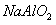 溶液与稀硫酸溶液
溶液与稀硫酸溶液
C.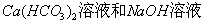 D.氨水与硝酸银溶液
D.氨水与硝酸银溶液
11、将足量的CO2不断通入KOH、Ca(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为( )
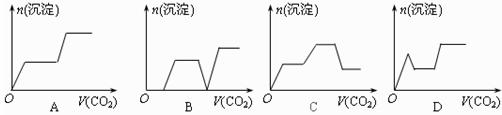
10、所谓合金,就是不同种金属(也包括一些非金属)在熔融状态下形成的一种熔合物,根据下列四种金属的熔、沸点,判断其中不能形成合金的是( )
|
|
Na |
Cu |
Al |
Fe |
|
熔点(℃) |
97.5 |
1083 |
660 |
1535 |
|
沸点(℃) |
883 |
2595 |
2200 |
3000 |
A.Cu和Al B.Fe和Cu C.Fe和Na D.Al和Na
9、将Mg、Cu组成的混合物26.4g投入到适量的稀硝酸中,固体完全溶解,收集到标准状况下的NO气体8.96L,向反应后的溶液中加入过量的5mol·L-1的NaOH溶液300mL,金属离子完全沉淀。则形成沉淀的质量是( )
A.43.2g B.46.8g C.53.6g D.63.8g
8、下列离子方程式中,只能表示一个化学反应的是( )
A.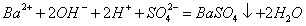
B.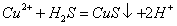
C.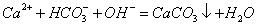
D.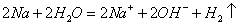
7、NA代表阿伏加德罗常数,下列说法正确的是( )
A.在同温同压时,相同体积的任何气体单质所含的原子数目相同
B.2g氢气所含原子数目为NA
C.在常温常压下,11.2L氮气所含的原子数目为NA
D.17g氨气所含电子数目为NA
6、下列反应的离子方程式书写正确的是( )
A.氢氧化钠溶液中通少量二氧化硫: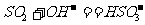
B.碳酸氢钠溶液与足量氢氧化钡溶液混合
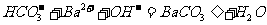
C.盐酸滴入氨水中: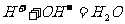
D.碳酸钙溶液于稀硝酸中: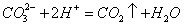
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com