
6°¢”ΫøÀ·∫Õ«øºÓ∂ºƒÐ∑¥”¶µƒªØ∫œŒÔ «£∫
°°°° A£ÆNaHCO3°°°° B£ÆKNO3°°°° C£ÆMgSO4°° °°°°°° D£ÆNaCl
5°¢ƒ≥∂˛º€—Ù¿Î◊”R2+,∫ÀÕ‚”–10∏ˆµÁ◊”£¨∆‰÷ ¡ø ˝ «24£¨À¸∫Àƒ⁄µƒ÷–◊” ˝Œ™
°°°° A£Æ14°°°°°° °°°°°°°° B£Æ12°°°°°°°° C£Æ10°°°°°° °°°° D£Æ8
4°¢”√≈®¡ÚÀ·∏…‘Ô≥± ™µƒ«‚∆¯£¨ «¿˚”√À¸µƒ
A£Æ—ıªØ–‘°°°°°° B£ÆÕ—ÀÆ–‘°°°° C£ÆŒ¸ÀÆ–‘°°°° °°°° D£ÆÀ·–‘
3°¢‘⁄pH = 1µƒŒÞ…´»Ð“∫÷–£¨ƒÐ¥Û¡øπ≤¥Êµƒ¿Î◊”◊È «£∫
°°°° A£ÆK+°¢Cu2+°¢SO42-°¢NO3-°°°°°°°° B£ÆNa+°¢H+°¢OH-°¢CO32-
°°°° C£ÆBa2+°¢NH4+°¢NO3-°¢Cl-°°°°°° °°D£ÆAg+°¢K+°¢SO42-°¢Cl-
2°¢œ¬¡–ŒÔ÷ Ù”⁄¥ø檌Եƒ «:
°°°° A£Æø’∆¯°°°°°° °°°°°°°°°°°° B£Æ“∫¬»°°°° °°°°°°°° C£Æ∆Ø∞◊∑€°°°°°° °°°°°°°° D£ÆøÛ»™ÀÆ
1°¢ø’∆¯÷–SO2µƒ∫¨¡øµƒ∂ý…Ÿ «¥Û∆¯Œ€»æ÷∏ ˝≤‚∂®÷∏±Í÷Æ“ª£¨ø’∆¯÷–SO2∆¯ÃÂ∫¨¡ø‘ˆ∂ýª·µº÷¬
°°°° A£Æ≥Ù—ıø’∂¥°°°° °°°°°° B£ÆŒ¬ “–ß”¶°°°° C£Æπ‚ªØ—ߗḬ̀°°° °°°°°° D£ÆÀ·”Í
32£Æ(8∑÷)∞—224ê˝(±Í◊º◊¥øˆ)µƒ∞±∆¯»ÐΩ‚‘⁄1ê˝ÀÆ(√Ð∂»Ω¸À∆Œ™1g/cm3)¿Ô£¨À˘µ√∞±ÀƵƒ√Ð∂»‘ºŒ™0.94 g/cm3°£«Îªÿ¥œ¬¡–Œ £∫
(1)«Û…œ ˆ∞±ÀÆ÷–»Ð÷ µƒ÷ ¡ø∑÷ ˝°£(“™«Û–¥≥ˆº∆À„π˝≥Ã)
(2)«Û…œ ˆ∞±ÀÆ÷–»Ð÷ µƒŒÔ÷ µƒ¡ø≈®∂»°£(“™«Û–¥≥ˆº∆À„π˝≥Ã)
(3)»° ¡ø…œ ˆ∞±ÀÆ”⁄ ‘πÐ÷–£¨µŒº”MgCl2»Ð“∫£¨≤˙…˙∞◊…´≥¡µÌ°£–¥≥ˆ∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
31£Æ(14∑÷)œ¬¡–Õºº◊∫Õ““∏˜Œ™“ªÃ◊ µ—È “÷∆∆¯◊∞÷√£¨ø…”√”⁄∆¯Ãµƒ∑¢…˙°¢∏…‘Ô∫Õ ’ºØ°£«Îªÿ¥œ¬¡–Œ £∫
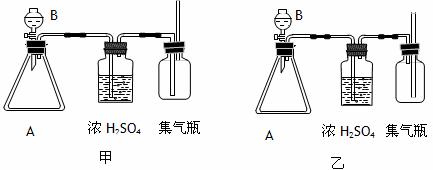
(1)»Ù”√¿¥÷∆»°H2£¨”¶—°◊∞÷√Õº_____°°°° £¨¥À ±A÷– ¢°°°°°°°° £¨B÷– ¢_______(Ãѧ Ω)£¨∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™_________________________°°°°°° °£
(2)»Ù”√¿¥÷∆±∏O2£¨”¶—°◊∞÷√Õº___°° £¨¥À ±»ÙB÷– ¢°°°°°° (Ãѧ Ω)£¨‘ÚA÷–”¶ ¢_______ (Ãѧ Ω)£ª’‚ ±∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™____________________________ °£
(3)ƒÐ∑Ò”√…œ ˆ◊∞÷√¿¥÷∆±∏∞±∆¯£ø°°°°°°°° (ÃÓ°∞ƒÐ°±ªÚ°∞≤ªƒÐ°±)°£¿Ì”… «£∫°°°°°°°°°°°°°° °£–¥≥ˆ µ—È “÷∆±∏∞±∆¯µƒªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
30£Æ(10∑÷)A°¢B°¢C°¢D°¢E∑÷±Œ™(NH4)2SO4°¢NH4Cl°¢NaCl°¢Na2SO4°¢Ba(OH)2ŒÂ÷÷»Ð“∫÷–µƒƒ≥“ª÷÷£¨∞—À¸√«¡Ω¡ΩªÏ∫œ£∫
°° ¢ŸA∫ÕBªÏ∫œ≤˙…˙∞◊…´≥¡µÌ£¨º”»»∫ÛŒÞ√˜œ‘±‰ªØ£ª
°°°° ¢⁄B∫ÕCªÏ∫œ≤˙…˙∞◊…´≥¡µÌ£¨º”»»∫Û≤˙…˙ π ™»Û∫Ï…´ Ø»Ô ‘÷Ω±‰¿∂µƒ∆¯Ã£ª
°°°° ¢€B∫ÕEªÏ∫œŒÞ√˜œ‘±‰ªØ£¨º”»»∫Û≤˙…˙ π ™»Û∫Ï…´ Ø»Ô ‘÷Ω±‰¿∂µƒ∆¯Ã°£
∏˘æð“‘…œœ÷œÛ£¨ÕÍ≥…œ¬¡–Œ £∫
°°(1)–¥≥ˆB£ÆC£ÆDµƒªØ—ß Ω£∫B°°°°°° °°C°°°°°°°° °°D°°°° °°
(2)–¥≥ˆœ¬¡–∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫
¢ŸB+C£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
¢⁄B+E£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
29£Æ(3∑÷)Ω´12.8øÀÕ≠∏˙“ª∂®¡øµƒ≈®œıÀ·∑¥”¶£¨Õ≠œ˚∫ƒÕÍ ±£¨π≤≤˙…˙∆¯ÃÂ5.6L(±Í◊º◊¥øˆ)£¨‘Úœ˚∫ƒœıÀ·µƒŒÔ÷ µƒ¡øŒ™°°°°°°°°°°°°°°°° °£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com