
10.已知A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,下列推断不正确的是( )
A.B、D不在一同周期 B.D一定在第二周期
C.A、D可能在同一主族 D.C和D的单质可能化合为离子化合物
9.在乙烯分子中有5个σ键、一个π键,它们分别是( )
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C-H之间是sp2形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键
D.C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键
8.下列各组分子中,都属于含极性键的非极性分子的是( )
A.CO2 H2S B.C2H4 CH4 C.C60 SO3 D.NH3 HCl
7.最近,意大利科学家使用普通氧分子和带正电荷的氧离子制造出了由4个氧原子构成的氧分子,并用质谱仪探测到了它存在的证据。若该氧分子具有空间对称结构,下列关于该氧分子的说法正确的是( )
A.是一种新的氧化物,属于非极性分子 B.不可能含有极性键
C.是氧元素的一种同位素 D.是臭氧的同分异构体
6.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是 ( )
A.原子半径 A>B>D>C B.离子半径 C>D>B>A
C.原子序数 d>c>b>a D.单质的还原性 A>B>D>C
5.X、Y、Z三种元素的原子,其最外层电子排布分别是ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是 ( )
A.XYZ2 B.X2YZ3 C.X2YZ2 D.XYZ3
4.已知铬的核电荷数为24,以下是一些同学绘制的基态铬原子核外电子的轨道表示式(即电子排布图),其中最能准确表示基态铬原子核外电子运动状态的是
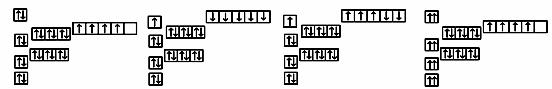
A B C D
3.下列说法正确的是( )
A.元素周期表每一周期元素原子的最外层电子排步均是从ns1 过渡到ns2np6
B.原子核外电子排布式为1s1的原子与原子核外电子排布式为1s22s1的原子的化学性质相似
C.元素周期表中ⅢB到ⅡB的10个纵行的元素都是金属,所以统称过渡金属元素
D.所有的非金属元素都分布在p区
2.下列表达方式错误的是 ( )
A. B.甲烷的电子式
B.甲烷的电子式 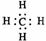
C.硫离子的核外电子排布式 1s22s22p63s23p6
D.碳-12原子构成 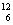 C
C
1.1919年,科学家第一次实现了人类多年的梦想--人工转变元素。这个核反应如下: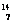 N+
N+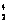 He→
He→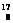 O+
O+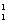 H下列叙述正确的是 ( )
H下列叙述正确的是 ( )
A.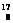 O原子核内有9个质子 ,8个电子
B.
O原子核内有9个质子 ,8个电子
B.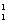 H原子核内有1个质子,1个中子
H原子核内有1个质子,1个中子
C.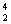 He和
He和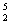 He互为同素异形体
D.CO和N2为互等电子体
He互为同素异形体
D.CO和N2为互等电子体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com