
3、X元素的阳离子和Y元素的阴离子具有相同的核外电子结构,下列叙述正确的是
A、原子序数X<Y B、原子半径X<Y
C、离子半径X>Y D、原子最外层电子数X<Y
2、下列化学用语的书写正确的是
A、乙酸的分子式:C2H4O2 B、乙醇的结构简式:C2H6O
C、F原子结构示意图: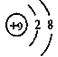 D、四氯化碳的电子式:
D、四氯化碳的电子式: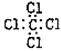
1、美国科学家将铅和氪两种元素的原子核对撞,获得了一种质子数为118、质量数为293的新元素,该元素原子核内的中子数和核外电子数之差为
A、47 B、175 C、61 D、57
22、(6分)将一定量的NaOH和NaHCO3的混合物A放在密闭容器中加热,充分反应后生成气体V1 L(V1≠0,标况),将反应后的固体残渣B与过量盐酸反应又生成CO2 V2 L(标况),则:
(1)B的成分是( )
A.Na2CO3和NaOH B.Na2CO3和NaHCO3 C.Na2CO3 D.NaOH
(2)原A中NaOH和NaHCO3的总物质的量为 mol。
(3)NaOH与NaHCO3的物质的量之比为 。
21、(12分)为了测定m g氢氧化钠和碳酸钠的固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
(1)甲同学的方案是:将样品溶解,加入过量氯化钡溶液,过滤、洗涤,取沉淀烘干,称量得固体ng。则混合物中碳酸钠的质量分数为 ;
(2)乙同学的方案是:将样品溶解后,加入稍过量的氯化钡溶液,再滴入2-3滴酚酞试液,用标准盐酸滴定。乙同学在滴定过程中所需要的主要玻璃仪器有 、 。加入过量氯化钡溶液的目的是 。
(3)丙同学的方案如下图所示
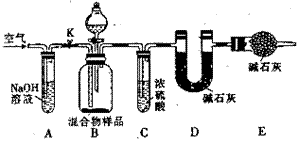
当混合物样品完全反应时,缓慢通入空气的目的是 ,其中,装置A的作用是 ,装置E的作用 。
20、(13分)已知A、B、C、D为常见单质,其中B、C、D常温常压下为气体,甲、乙、丙、丁为常见的化合物,乙常温下为液体,丙的焰色反应为黄色,下图为各种物质之间的转化关系。
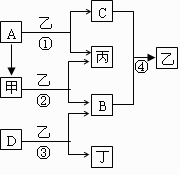
请回答下列问题:
(1)写出下列物质的化学式:A ,B ,D 。
(2)甲的电子式为 ,反应②中若有11.2L(标准状况下)B生成,则发生转移的电子的物质的量为 。
(3)写出反应③的化学方程式: 。
19、(10分)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40-50℃时反应可生成它。CuH具有的性质有:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体:Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是 (填氧化剂或还原剂)。
(2)写出CuH在氯气中燃烧的化学反应方程式
(3)CuH溶解在稀盐酸中生成的气体是 (填化学式)
(4)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式 。
18、(9分)有一包粉末,其中可能含有Na2CO3、NaHCO3、NaCl、K2SO4、Na2SO4和BaCl2,现按下列步骤进行实验。
(1)将该粉末溶于水,溶液变浑浊,过滤,得滤液和白色沉淀。
(2)向操作(1)中得到的白色沉淀中加入足量的稀HNO3后,沉淀量减少但不完全消失。
(3)向操作(1)得到的滤液中滴加NaOH溶液,有白色沉淀产生。
(4)取操作(1)得到的滤液做焰色反应,火焰呈黄色,透过蓝色钴玻璃观察,未见紫色火焰。
由上述实验现象推断:混合物中一定含有 ;一定不含有 ;不能肯定是否含有 。
17、(10分)对于两种相同的反应物,由于操作顺序不同,其反应过程不同,往往会导致不同的实验现象,有许多化学反应符合这一规律。例如碳酸钠溶液与稀盐酸滴加顺序不同反应现象不同就是一个典型。现有下列化学试剂:
A、稀盐酸 B、氢氧化钠溶液 C、氯化铝溶液 D、偏铝酸钠溶液。选取其中的两种溶液,把一种溶液滴到另一种溶液中,其滴入溶液的体积与生成的沉淀的质量关系如下图所示。
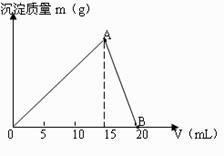
(1)上图所示的操作是把_____________滴加到_____________中(填入相应的字母)。
(2)反应恰好进行到A点时,溶液中存在的金属阳离子是_____________。
(3)B点时,溶液的pH 7(填“>”、“<”或“=”),试用离子方程式说明原因:
。
(4)写出AB段反应的离子方程式: 。
16、取500mLNa2CO3溶液与300mL 1mol/L盐酸反应,在不断搅拌下将碳酸钠溶液逐滴滴入盐酸中与将盐酸逐滴滴入碳酸钠溶液中,所产生气体的物质的量之比为3:2,则碳酸钠溶液的物质的量浓度为( )
A.0.2mol/L B.0.3mol/L C.0.4mol/L D.0.5mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com