
18Θ°”–BaCl2ΚΆNaClΒΡΜλΚœ»ή“ΚaLΘ§ΫΪΥϋΨυΖ÷≥…ΝΫΖίΓΘ“ΜΖίΒΈΦ”œΓΝρΥαΘ§ ΙBa2+άκΉ”Άξ»Ϊ≥ΝΒμΘΜΝμ“ΜΖίΒΈΦ”AgNO3»ή“ΚΘ§ ΙCl-άκΉ”Άξ»Ϊ≥ΝΒμΓΘΖ¥”Π÷–œϊΚΡxmolH2SO4ΓΔymolAgNO3ΓΘΨί¥ΥΒΟ÷Σ‘≠ΜλΚœ»ή“Κ÷–ΒΡc(Na+)/molΓΛL-1ΈΣΓΓΓΓΓΓ ΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°(y-2x)/aΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°(y-x)/a
ΓΓΓΓΓΓ CΘ°(2y-2x)/aΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°(2y-4x)/a
17Θ°ΫΪΚ§0.4molCuSO4ΚΆ0.4molNaClΒΡΥ°»ή“Κ1LΘ§”ΟΕη–‘ΒγΦΪΒγΫβ“ΜΕΈ ±ΦδΚσΘ§‘Ύ“ΜΗωΒγΦΪ…œΒΟΒΫ0.3molΆ≠Θ§‘ΎΝμ“ΜΗωΒγΦΪ…œΈω≥ωΤχΧε(±ξΉΦΉ¥Ωωœ¬)ΒΡΧεΜΐ «ΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°5.6LΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°6.72LΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°13.44LΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°11.2L
16Θ°œ¬Ν–”–ΙΊ Β―ιΒΡ≤ΌΉςΜρœ÷œσ–π ω’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°Ρ≥Υ°»ή“Κ÷–Φ”»κ―ΈΥαΥαΜ·ΒΡBa(NO3)2»ή“ΚΘ§≥ωœ÷ΑΉ…Ϊ≥ΝΒμΘ§‘ρ‘≠»ή“Κ÷–“ΜΕ®¥φ‘Ύ
ΓΓΓΓΓΓ BΘ°”ΟΙΐ¬ΥΒΡΖΫΖ®Ζ÷άκΥ°ΚΆ…ΌΝΩ±ΫΖ”ΒΡΜλΚœΈο
ΓΓΓΓΓΓ CΘ°Α―ΉΑ”–NO2ΚΆN2O4ΜλΚœΤχΧεΒΡ…’ΤΩΘ§Ζ≈»κΒΫ»»Υ°÷–Θ§ΜλΚœΤχΧεΒΡ―’…ΪΫΪ±δ«≥
ΓΓΓΓΓΓ DΘ°ΝρΥαΆ≠ΨßΧεΫαΨßΥ°≤βΕ® Β―ι÷–Θ§ ΔΝρΥαΆ≠ΨßΧεΒΡέαέωΦ”»»ΚσΘ§“Σ»κ‘ΎΗ…‘οΤςΡΎά以Κσ‘Ό≥ΤΝΩ
15Θ°«βΜ·―«Ά≠(CuH) «“Μ÷÷Ρ―»ήΈο÷ Θ§”ΟCuSO4»ή“ΚΚΆΓΑΝμ“Μ÷÷Ζ¥”ΠΈοΓ±‘Ύ40Γφ-50Γφ ±Ζ¥”ΠΩ……ζ≥…ΥϋΘ§CuH≤ΜΈ»Ε®Θ§CuH‘Ύ¬»Τχ÷–Ρή»Φ…’ΘΜΗζ―ΈΥαΖ¥”ΠΡή≤ζ…ζΤχΧεΓΘ“‘œ¬”–ΙΊΥϋΒΡΆΤΕœ¥μΈσΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°’βΓΑΝμ“Μ÷÷Ζ¥”ΠΈοΓ±“ΜΕ®ΨΏ”–ΜΙ‘≠–‘
ΓΓΓΓΓΓ BΘ°CuHΦ»Ω…ΡήΉω―θΜ·ΦΝ“≤Ω…ΉωΜΙ‘≠ΦΝ
ΓΓΓΓΓΓ CΘ°CuH+Cl2=CuCl+HCl(»Φ…’)
ΓΓΓΓΓΓ DΘ°2CuH+2HCl=CuCl2+2H2Γϋ+Cu(≥ΘΈ¬)
14Θ° Β―ι “”Ο«Π–νΒγ≥ΊΉςΒγ‘¥ΒγΫβΚΆ ≥―ΈΥ°÷Τ»Γ¬»ΤχΘ§“―÷Σ«Π–νΒγ≥ΊΖ≈Βγ ±ΖΔ…ζ»γœ¬Ζ¥”ΠΘΚ
ΗΚΦΪΘΚPb+SO42-ΓζPbSO4+2e
’ΐΦΪΘΚPbO2+4H++SO42-+2eΓζPbSO4+2H2O
Ϋώ»τ÷ΤΒΟ¬»Τχ0.050molΘ§’β ±Βγ≥ΊΡΎœϊΚΡΝρΥαΒΡΈο÷ ΒΡΝΩ÷Ν…Ό «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°0.025molΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°0.050molΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°0.10molΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°0.20mol
13Θ°œ¬Ν–ΗςΉιΈο÷ ÷–Α¥»έΒψ”…ΒΆΒΫΗΏΥ≥–ρ≈≈Ν–’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°O2ΓΓ I2ΓΓ HgΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°CO2ΓΓ KClΓΓ SiO2
ΓΓΓΓΓΓ CΘ°NaΓΓ KΓΓ RbΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°SiCΓΓ NaClΓΓ SO2
12Θ°Ρ≥»ή“Κ÷–¥φ‘ΎΫœΕύΒΡK+ΓΔH+ΓΔI-Θ§œ¬Ν–άκΉ”Ω…“‘‘Ύ…œ ω»ή“Κ÷–¥σΝΩΙ≤¥φΒΡ «ΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°Cl-ΓΔNH+4ΓΔNa+ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°H3O+ΓΔCl-ΓΔNO3-
ΓΓΓΓΓΓ CΘ°Na+ΓΔHCO3-ΓΔSO42-ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°HCOO-ΓΔBr-ΓΔNH+4
11Θ°‘ΎΝρΥαΙΛ“Β…ζ≤ζ÷–Θ§ΈΣΝΥ”–άϊ”ΎSO2ΒΡΉΣΜ·Θ§«“Ρή≥δΖ÷άϊ”Ο»»ΡήΘ§≤…”ΟΝΥ÷–Φδ”–»»ΫΜΜΜΤςΒΡΫ”¥Ξ “Θ§Α¥¥ΥΟή±’ΧεœΒ÷–ΤχΧεΒΡΝςœρΘ§‘ρ‘ΎA¥ΠΝς≥ωΒΡΤχΧεΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
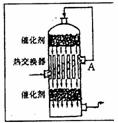
ΓΓΓΓΓΓ AΘ°SO2Θ§N2ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°SO3Θ§O2Θ§N2ΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°SO2Θ§O2Θ§N2ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°SO2Θ§SO3Θ§N2
10Θ°”ΟΕη–‘ΒγΦΪΒγΫβœ¬Ν–ΗςΉι÷–ΒΡ»ΐ÷÷ΒγΫβ÷ »ή“ΚΘ§‘ΎΒγΫβΙΐ≥Χ÷–Θ§»ή“ΚΒΡpH“ά¥ΈΈΣ…ΐΗΏΓΔΫΒΒΆΓΔ≤Μ±δΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°AgNO3,CuCl2,Cu(NO3)2ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°KBrΘ§CuSO4Θ§Na2SO4
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°CaCl2Θ§KOHΘ§NaNO3ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°HClΘ§NHO3Θ§K2SO4
9Θ°“―÷ΣCl-ΓΔFe2+ΓΔH2O2ΓΔI-ΓΔSO2ΨυΨΏ”–ΜΙ‘≠–‘Θ§«“‘ΎΥα–‘»ή“Κ÷–ΒΡΜΙ‘≠–‘“ά¥Έ‘ω«ΩΓΘœ¬Ν–ΗςΖ¥”Π≤ΜΩ…ΡήΖΔ…ζΒΡ «ΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°2Fe2++Cl2=2Fe3++2Cl-ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°H2O2+H2SO4=SO2+O2+2H2OΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°I2+SO2+2H2O=H2SO4+2HI
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com