
(1)配制100 mL 0.10 mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后) →洗涤(并将洗涤液移入容量瓶)→ →摇匀 →将配制好的溶液倒入试剂瓶中,贴上标签。
29.(11分)实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验,请完成下列填空:
 28.(9分)一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)
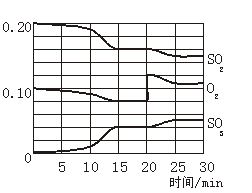
28.(9分)一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g),△H<0。反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:
2SO3(g),△H<0。反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:
(1) 若降低温度,该反应的化学平衡常数 。(填“增大”“减小”或“不变”)
(2)该反应处于平衡状态的时间段为 。
(3)反应进行至20 min时,曲线发生变化的原因是 (用文字表达)。10 min到15 min的曲线变化的原因可能是 (填写编号)。
a. 加了催化剂 b. 缩小容器体积
c. 降低温度 d. 增加SO3的物质的量
(4)维持容器体积不变,向该反应的平衡体系中充入氮气 , 则平衡 ( 填“向左”或“向右”或“不”)移动;维持容器体积不变,向该反应的平衡体系中移走部分混合气体 , 则平衡 ( 填“向左”或“向右”或“不”) 移动。
27、(10分)(1)氯化铁溶于水时易发生水解反应,水解的离子方程式为 。 某同学欲在实验室中配制氯化铁溶液,为了防止其水解,他应采取的配制的方法是: 。
若向氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,并产生无色气体,同时还有红褐色沉淀生成,其原因是
。
(2)向盛有氯化银悬浊液的试管中加入硫化钠溶液,可看到的现象是
,反应的离子方程式为 。
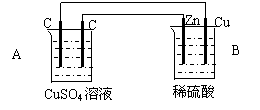 |
⑴判断装置的名称:A池为 B池为
⑵A池中左边石墨棒为 极,电极反应式为
A池中电池总反应式
(3)若工作一段时间后,B池中Cu棒上析出224ml气体(标准状态),则电路中通过
了 摩尔电子,B池中溶液质量 (填“增加”、“不变”或“减少”) g,若反应前后溶液的体积不变,反应后A池溶液的pH为
26、(14分)如图装置中,A、B两池溶液的体积均为200mL,
Cd + 2NiOOH + 2H2O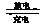 Cd(OH)2
+ 2Ni(OH)2
Cd(OH)2
+ 2Ni(OH)2
有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2 -e― + OH- == NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
卷Ⅱ(非选择题 共50分)
25、镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:
 24、右图两个实验装置是实现化学能和电能
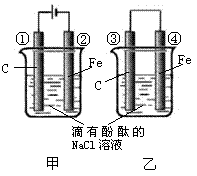
24、右图两个实验装置是实现化学能和电能
相互转化的装置。甲、乙两装置电极附近的
溶液首先变红的电极分别是
A.①③
B.①④
C.②③
D.②④
C.c(CH3COOH)< c(CH3COO-) D.c(CH3COO-)+c(OH-)=0.2mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com