
19£®(ÇàÆÖÒ»)½«0.1 mol/L CH3COOHÈÜÒº¼ÓˮϡÊÍ»ò¼ÓÈëÉÙÁ¿CH3COONa¾§Ìåʱ¶¼»áÒýÆð
¡¡ A£®CH3COOHµçÀë³Ì¶È±ä´ó¡¡ ¡¡¡¡¡¡¡¡B£®ÈÜÒºµÄpHÖµÔö´ó
¡¡ C£®ÈÜÒºµÄµ¼µçÄÜÁ¦¼õÈõ¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡D£®ÈÜÒºÖÐC(H+ )¼õС
19£®(¬ÍåÒ»)¡°Ëá¼îÖÊ×ÓÀíÂÛ¡±ÈÏΪ·²ÊÇÄܹ»¸ø³öÖÊ×Ó(H+)µÄ·Ö×Ó»òÀë×Ó¶¼ÊÇËᣬ·²ÊÇÄܹ»½ÓÊÜÖÊ×ӵķÖ×Ó»òÀë×Ó¶¼ÊǼÎïÖÊËáÐÔ(¼îÐÔ)µÄÇ¿ÈõÈ¡¾öÓÚ·Ö×Ó»òÀë×Ó¸ø³ö(½ÓÊÜ)ÖÊ×ÓÄÜÁ¦µÄ´óС¡£°´ÕÕ¡°Ëá¼îÖÊ×ÓÀíÂÛ¡±£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ(¡¡ )¡£
A.HCO3£ ¼ÈÊÇËáÓÖÊǼNH3¼È²»ÊÇËáÓÖ²»ÊǼî
B.ClO£+H2O HClO+OH£ÊÇËá¼î·´Ó¦
HClO+OH£ÊÇËá¼î·´Ó¦
C.2Na+2H2O¡ú2NaOH+H2¡üÊÇËá¼î·´Ó¦
D.¼îÐÔÇ¿Èõ˳ÐòΪ£ºC2H5O£ > OH£ > C6H5O£
13£® (ÆÖ¶«Ò»)ÔÚÆäËûÌõ¼þ²»±äµÄÇé¿öÏ£¬Ïò0.1 mo/LµÄ°±Ë®ÖÐͨÈëÒ»¶¨Á¿°±Æø£¬ÏÂÁнáÂÛ´íÎóµÄÊÇ(¡¡¡¡ )
(ÆÖ¶«Ò»)ÔÚÆäËûÌõ¼þ²»±äµÄÇé¿öÏ£¬Ïò0.1 mo/LµÄ°±Ë®ÖÐͨÈëÒ»¶¨Á¿°±Æø£¬ÏÂÁнáÂÛ´íÎóµÄÊÇ(¡¡¡¡ )
A£®c(NH3¡¤H2O)±ä´ó ¡¡ ¡¡B£®c(NH4+) ±ä´ó¡¡ C£®pH±ä´ó¡¡ ¡¡¡¡D£®µçÀë³£Êý±ä´ó
7£®(·îÏÍÒ»)ÓÃˮϡÊÍ0.1mol¡¤L-1°±Ë®Ê±£¬ÈÜÒºÖÐËæ×ÅË®Á¿µÄÔö¼Ó¶ø¼õСµÄÊÇ (¡¡ )
¡¡A£®[OH- ]/[NH3¡¤H2O]¡¡¡¡¡¡¡¡¡¡¡¡ B£®[NH3¡¤H2O]£¯[OHÒ» ]
¡¡ C£®[H+]ºÍ[OHÒ» ]µÄ³Ë»ý¡¡¡¡¡¡¡¡¡¡ D£®OHÒ»µÄÎïÖʵÄÁ¿
20£®(ÄÏ»ãÒ»)¶ÔÓÚ0.1 mol/L CH3COOHÈÜÒº´æÔÚµçÀëƽºâ£ºCH3COOH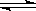 CH3COO£+H+-Q£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ (¡¡ )
CH3COO£+H+-Q£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ (¡¡ )
A£®¼ÓˮϡÊÍ»ò¼ÓÈëÉÙÁ¿CH3COONa¾§Ìåʱ£¬CH3COOHµçÀë³Ì¶È±ä´ó
B£®¼ÓˮϡÊÍ»ò¼ÓÈëÉÙÁ¿CH3COONa¾§Ìåʱ£¬¶¼»áÒýÆðÈÜÒºµÄpHÖµÔö´ó
C£®Éý¸ßζȻò¼ÓˮϡÊÍ£¬ÈÜÒºÖÐc(H+)/c(CH3COOH)ÖµÔö´ó
D£®¼ÓÉÙÁ¿ÉÕ¼îÈÜÒº»ò¼ÓÉÙÁ¿±ù´×ËᣬÈÜÒºÖÐc(H+)/c(CH3COOH)ÖµÔö´ó
14£®(Ê®ËÄУ¶þ)¼×ËáÊÇÒ»ÖÖÒ»ÔªÓлúËá¡£ÏÂÁÐÐÔÖÊ¿ÉÒÔÖ¤Ã÷ËüÊÇÈõµç½âÖʵÄÊÇ¡¡¡¡ (¡¡¡¡ )
¡¡¡¡ A£®¼×ËáÄÜÓëË®ÒÔÈÎÒâ±È»¥ÈÜ
¡¡¡¡ B£®1mol¡¤L-1¼×ËáÈÜÒºµÄpHֵԼΪ2
¡¡¡¡ C£®10mL 1mol¡¤L-1¼×ËáÇ¡ºÃÓë10mL 1mol¡¤L-1NaOHÈÜÒºÍêÈ«·´Ó¦
|
5£®(¬ÍåÒ»)¸ù¾ÝÓйػ¯Ñ§ÔÀí£¬ÏÂÁÐÅжÏÕýÈ·µÄÊÇ(¡¡ )¡£
A.60¡æʱ£¬NaClÈÜÒºµÄPH <7£¬ÔòÈÜÒº³ÊËáÐÔ
B.ÈôÑÎKXÈÜÓÚˮʱÈÜҺζȽµµÍ£¬ÔòKXÒ»¶¨·¢ÉúÁËË®½â
C.ÈôÈõËáHAµÄËáÐÔÇ¿ÓÚÈõËáHB£¬ÔòͬŨ¶ÈÄÆÑÎÈÜÒºµÄ¼îÐÔ:NaA<NaB
D.250Cʱ£¬ÓëͬŨ¶ÈµÄÏ¡ÁòËá·´Ó¦£¬Ð¿Á£µÄËÙÂÊÒ»¶¨±ÈÌúм¿ì
3£®(¬ÍåÒ»)ÒÑÖª25¡æʱ£¬Çâ·úËá(HF)µÄµçÀë³£ÊýKiΪ3.53¡Á10-4£¬ÒÒËá(CH3COOH)µÄµçÀë³£ÊýKiΪ1.75¡Á10-5¡£¹ØÓÚ¸ÃζÈÏ£¬Å¨¶ÈͬΪ0.10mol£¯LÕâÁ½ÖÖËáµÄµçÀë¶È´óСÅжÏÕýÈ·ÊÇ(¡¡ )¡£
A.Çâ·úËáµÄµçÀë¶ÈСÓÚÒÒËáµÄµçÀë¶È¡¡ B.Çâ·úËáµÄµçÀë¶ÈµÈÓÚÒÒËáµÄµçÀë¶È
C.Çâ·úËáµÄµçÀë¶È´óÓÚÒÒËáµÄµçÀë¶È¡¡ D.ÎÞ·¨ÅжÏ
14£®(Ê®ËÄУһ)³£ÎÂÏ£¬Ä³Ë®ÈÜÒºÖÐË®µÄµçÀë¶ÈΪ1.8¡Á10-12%£¬¸ÃÈÜÒº²»¿ÉÄÜÊÇ¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®ÉÕ¼îÈÜÒº¡¡¡¡¡¡¡¡¡¡¡¡ B£®Ì¼ËáÇâÄÆÈÜÒº¡¡¡¡ C£®ÏõËáÈÜÒº¡¡¡¡¡¡¡¡¡¡¡¡ D£®ÁòËáÇâÄÆÈÜÒº
6£®(Ê®ËÄУһ)ÊÒÎÂÏ£¬½«Ð¡ËÕ´òͶÈë×ãÁ¿Ë®ÖУ¬ÏÂÁйý³Ì²»»á·¢ÉúµÄÊÇ¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®Èܽ⡡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®·Ö½â¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£®Àë½â¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®Ë®½â
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com