
5.(普陀二)金属材料在一个国家的国民经济中占有举足轻重的地位。有关金属的叙述正确的是
A.日常使用的金属材料90%以上都是合金
B.金属与盐溶液的反应都是置换反应
C.炼铁和炼钢都需要还原剂作为一种原料
D.镀锌铁皮的镀层损坏后,铁更易腐蚀
13. (普陀一)对以下化学问题的解释中错误的是
A. 工业盐酸显黄色,是由于含有杂质FeCl3
B. 碘化钾溶液久置显黄色,是由于I–被氧化,析出的I2溶于溶液中
C. 浓硝酸显黄色,是由于硝酸见光分解生成的NO2溶于酸液中
D. 炼钢是在高温下利用还原剂除去生铁中的杂质
3.(黄浦二)工业冶炼钨采取的方法是( )
A.热分解法 B.热还原法 C.电解法 D.自然界存在直接得到
17.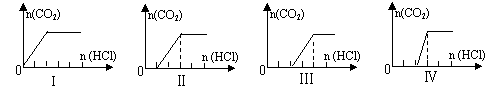 (奉贤二)向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如图:
(奉贤二)向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如图:
则下列分析都正确的组合是:
|
|
溶液组成主要成分 |
对应图象 |
溶液中离子浓度关系 |
|
A |
NaHCO3、Na2CO3 |
Ⅱ |
c(CO32-)
< c(HCO3-) |
|
B |
NaOH 、
Na2CO3 |
Ⅲ |
c(OH-)>c(CO32-) |
|
C |
Na2CO3 |
Ⅳ |
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
|
D |
NaHCO3 |
I |
c(Na+)
= c(HCO3-) |
铁
14、(八校)向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是( )

15.(松江二)氮化钠和氢化钠与水反应的化学方程式如下:Na3N + 3H2O → 3NaOH + NH3,
NaH + H2O → NaOH + H2↑。有关Na3N和NaH的叙述正确的是 ( )
A.离子半径:Na+>N3->H+ B.与水反应都是氧化还原反应
C.与盐酸反应都只生成一种盐 D.加热熔化时,都只破坏离子键
8. (宝山二)将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是 ( )
A.表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠
B. “出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液
C.最后变成碳酸钠粉末 D.该过程的所有化学反应均为氧化还原反应
5.(奉贤一)类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实践的验证。以下类推的结论正确的是:
A.由甲酸可以发生银镜反应可推出其余的羧酸也均能发生银镜反应
B.CO2与SiO2化学式相似,故CO2与SiO2的晶体结构也相似
C.由“2Fe + 3Cl2 → 2FeCl3”反应可推出“2Fe + 3I2 → 2FeI3”反应也能发生
D.Na、K具有强还原性,Na常温下与水剧烈反应,故K常温下也能与水剧烈反应
18. (奉贤二)从下列事实所得出的相应结论正确的是
|
|
实验事实 |
结论 |
|
A |
常温下白磷可自燃,而氮气要在放电条件下才与氧气反应 |
氮气的化学性质比磷稳定 |
|
B |
CO2的水溶液可导电 |
CO2是电解质 |
|
C |
SO2通入到硝酸钡溶液中出现白色沉淀 |
沉淀为硫酸钡 |
|
D |
NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 |
同浓度pH: NaAlO2 < NaHCO3 |
碱金属
18. 下列关于化工生产原理的叙述中,均符合目前工业生产实际的是…………… ( )
A. 氯碱工业中,氢氧化钠在电解槽的阴极区产生
B. 氯气和氢气混合在光照条件下生成氯化氢,用水吸收得到盐酸
C. 合成氨工业中,利用氨易液化,分离出N2、H2循环使用,总体上提高了氨的产率
D. 二氧化硫在接触室被氧化成三氧化硫,三氧化硫在吸收塔内被水吸收制成浓硫酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com