
18£®ÔÚÒ»¶¨Î¶ÈϽ«1molCOºÍ1molH2O(g)ͨÈëÒ»¸öÃܱÕÈÝÆ÷Öз´Ó¦£º
CO(g)+H2O(g)
 ¡¡CO2(g)+H2(g)£¬´ïµ½Æ½ºâºóCO2µÄÎïÖʵÄÁ¿Îª0.6mol£¬ÔÙͨÈë4molH2O(g)´ïµ½Æ½ºâºóCO2µÄÎïÖʵÄÁ¿¿ÉÄÜÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡
¡¡CO2(g)+H2(g)£¬´ïµ½Æ½ºâºóCO2µÄÎïÖʵÄÁ¿Îª0.6mol£¬ÔÙͨÈë4molH2O(g)´ïµ½Æ½ºâºóCO2µÄÎïÖʵÄÁ¿¿ÉÄÜÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡
¡¡A£®µÈÓÚ0.6mol¡¡ B£®µÈÓÚ1mol¡¡ C£®´óÓÚ1mol¡¡ D£®´óÓÚ0.6mol£¬Ð¡ÓÚ1mol
17£®Á½¸öÌå»ýÏàͬµÄÃܱÕÈÝÆ÷A¡¢B£¬ÔÚAÖгäÈëSO2ºÍO2¸÷1mol£¬ÔÚBÖгäÈëSO2ºÍ
O2¸÷2 mol£¬¼ÓÈȵ½Ïàͬζȣ¬ÓÐÈçÏ·´Ó¦2SO2(g)+ O2(g) 2SO3(g)£¬¶Ô´Ë·´Ó¦£¬ÏÂÊö
2SO3(g)£¬¶Ô´Ë·´Ó¦£¬ÏÂÊö
²»ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡ A£®·´Ó¦ËÙÂÊB£¾A¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
B£®SO2µÄת»¯ÂÊB£¾A 
C£®Æ½ºâʱ¸÷×é·Öº¬Á¿B = A¡¡¡¡¡¡¡¡¡¡
D£®Æ½ºâʱÈÝÆ÷µÄѹǿB£¾A
16¡¢ÔÚ25¡æʱ½¨Á¢ÏÂÁÐƽºâ£º2NO2
 ¡¡N2O4£¬Õý·´Ó¦·ÅÈÈ£¬Èô°ÑÉÕÆ¿ÖÃÓÚ100¡æµÄ·ÐË®ÖУ¬ÏÂÁÐÇé¿ö£º¢ÙÑÕÉ«¢Úƽ¾ùĦ¶ûÖÊÁ¿¢ÛÖÊÁ¿¢Üѹǿ¢ÝÃܶÈÖв»±äµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡
¡¡N2O4£¬Õý·´Ó¦·ÅÈÈ£¬Èô°ÑÉÕÆ¿ÖÃÓÚ100¡æµÄ·ÐË®ÖУ¬ÏÂÁÐÇé¿ö£º¢ÙÑÕÉ«¢Úƽ¾ùĦ¶ûÖÊÁ¿¢ÛÖÊÁ¿¢Üѹǿ¢ÝÃܶÈÖв»±äµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡

A.¢Û¢Ý¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡ B.¢Û¢Ü¡¡¡¡ ¡¡¡¡¡¡ C.¢Ú¢Ü¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
D.¢Ù¢Û
15.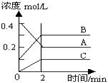 ÓÒͼËùʾΪ8000CʱA¡¢B¡¢CÈýÖÖÆøÌåÔÚÃܱÕÈÝÆ÷Öз´Ó¦Ê±Å¨¶ÈµÄ±ä»¯£¬Ö»´ÓͼÉÏ·ÖÎö²»ÄܵóöµÄ½áÂÛÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
ÓÒͼËùʾΪ8000CʱA¡¢B¡¢CÈýÖÖÆøÌåÔÚÃܱÕÈÝÆ÷Öз´Ó¦Ê±Å¨¶ÈµÄ±ä»¯£¬Ö»´ÓͼÉÏ·ÖÎö²»ÄܵóöµÄ½áÂÛÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡

A£®AÊÇ·´Ó¦Îï¡¡ 
B£®Ç°2 min AµÄ·Ö½âËÙÂÊΪ0.1mol•L-1•min-1¡¡¡¡¡¡¡¡¡¡¡¡¡¡

C£®´ïƽºâºó£¬ÈôÉý¸ßζȣ¬Æ½ºâÏòÕý·´Ó¦·½ÏòÒƶ¯¡¡ 
D£®´ïƽºâºó£¬ÈôÔö´óѹǿ£¬Æ½ºâÏòÄæ·´Ó¦·½ÏòÒƶ¯¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡

14£®Ò»¶¨Ìõ¼þÏ·´Ó¦mA(g)+ nB(g) pC(g)+ qD(g)ÔÚÒ»ÃܱÕÈÝÆ÷ÖнøÐУ¬²âµÃƽ¾ù·´Ó¦ËÙ¶Èv(C)= 2v(B)¡£Èô·´Ó¦´ïƽºâºó±£³ÖζȲ»±ä£¬¼Ó´óÌåϵѹǿʱƽºâ²»Òƶ¯£¬Ôòm¡¢n¡¢p¡¢qµÄÊýÖµ¿ÉÒÔÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
pC(g)+ qD(g)ÔÚÒ»ÃܱÕÈÝÆ÷ÖнøÐУ¬²âµÃƽ¾ù·´Ó¦ËÙ¶Èv(C)= 2v(B)¡£Èô·´Ó¦´ïƽºâºó±£³ÖζȲ»±ä£¬¼Ó´óÌåϵѹǿʱƽºâ²»Òƶ¯£¬Ôòm¡¢n¡¢p¡¢qµÄÊýÖµ¿ÉÒÔÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡

A£®2¡¢6¡¢3¡¢5¡¡¡¡¡¡¡¡ B£®3¡¢1¡¢2¡¢2¡¡¡¡¡¡¡¡
C£®3¡¢1¡¢2¡¢1¡¡¡¡¡¡ ¡¡ D£®1¡¢3¡¢2¡¢2
13. 2A(g) 2B(g)+C(g)£»Õý·´Ó¦ÎüÈÈ£¬´ïƽºâʱ£¬ÒªÊ¹vÕý½µµÍ¡¢c(A)Ôö´ó£¬Ó¦²ÉÈ¡
2B(g)+C(g)£»Õý·´Ó¦ÎüÈÈ£¬´ïƽºâʱ£¬ÒªÊ¹vÕý½µµÍ¡¢c(A)Ôö´ó£¬Ó¦²ÉÈ¡
¡¡ A£®¼Óѹ¡¡¡¡¡¡¡¡
¡¡ B£®¼õѹ ¡¡¡¡¡¡ ¡¡¡¡¡¡C£®¼õСBµÄŨ¶È¡¡¡¡ ¡¡¡¡¡¡¡¡
D£®½µÎ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡

12.ÒÑÖª·´Ó¦A+3B  ¡¡2C+DÔÚij¶Îʱ¼äÄÚÒÔAµÄŨ¶È±ä»¯±íʾµÄ»¯Ñ§·´Ó¦ËÙ¶ÈΪ1mol¡¤L£1¡¤min£1£¬Ôò´Ë¶Îʱ¼äÄÚÒÔCµÄŨ¶È±ä»¯±íʾµÄ»¯Ñ§·´Ó¦ËÙÂÊΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡2C+DÔÚij¶Îʱ¼äÄÚÒÔAµÄŨ¶È±ä»¯±íʾµÄ»¯Ñ§·´Ó¦ËÙ¶ÈΪ1mol¡¤L£1¡¤min£1£¬Ôò´Ë¶Îʱ¼äÄÚÒÔCµÄŨ¶È±ä»¯±íʾµÄ»¯Ñ§·´Ó¦ËÙÂÊΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡

A£®0£®5mol¡¤L£1¡¤min£1¡¡B£®1 mol¡¤L£1¡¤min£1¡¡¡¡C£®2 mol¡¤L£1¡¤min£1 ¡¡D£®3 mol¡¤L£1¡¤min£1
11.½« 4 mol A ÆøÌåºÍ 2 mol B ÆøÌåÔÚ 2 L µÄÈÝÆ÷ÖлìºÏ²¢ÔÚÒ»¶¨Ìõ¼þÏ·¢ÉúÈçÏ·´Ó¦¡¡ 2A(Æø)+B(Æø) 2C(Æø)Èô¾ 2 s(Ãë)ºó²âµÃ C µÄŨ¶ÈΪ 0.6 mol¡¤L£1 £¬ÏÖÓÐÏÂÁм¸ÖÖ˵·¨£º¢Ù ÓÃÎïÖÊ A ±íʾµÄ·´Ó¦µÄƽ¾ùËÙÂÊΪ 0.3 mol¡¤L£1¡¤s£1¢Ú ÓÃÎïÖÊ B ±íʾµÄ·´Ó¦µÄƽ¾ùËÙÂÊΪ 0.6 mol¡¤L£1¡¤s£1¢Û 2 s ʱÎïÖÊ A µÄת»¯ÂÊΪ70%¡¡ ¢Ü 2 s ʱÎïÖÊ B µÄŨ¶ÈΪ 0.7 mol¡¤L£1ÆäÖÐÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
2C(Æø)Èô¾ 2 s(Ãë)ºó²âµÃ C µÄŨ¶ÈΪ 0.6 mol¡¤L£1 £¬ÏÖÓÐÏÂÁм¸ÖÖ˵·¨£º¢Ù ÓÃÎïÖÊ A ±íʾµÄ·´Ó¦µÄƽ¾ùËÙÂÊΪ 0.3 mol¡¤L£1¡¤s£1¢Ú ÓÃÎïÖÊ B ±íʾµÄ·´Ó¦µÄƽ¾ùËÙÂÊΪ 0.6 mol¡¤L£1¡¤s£1¢Û 2 s ʱÎïÖÊ A µÄת»¯ÂÊΪ70%¡¡ ¢Ü 2 s ʱÎïÖÊ B µÄŨ¶ÈΪ 0.7 mol¡¤L£1ÆäÖÐÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡

A£®¢Ù¢Û¡¡¡¡¡¡¡¡¡¡
B. ¢Ù¢Ü¡¡¡¡¡¡¡¡ C. ¢Ú¢Û¡¡¡¡¡¡¡¡ D. ¢Û¢Ü
10.±¾ÌâÁоٵÄËĸöÑ¡ÏîÊÇ4λͬѧÔÚѧϰ¡°»¯Ñ§·´Ó¦ËÙÂʺͻ¯Ñ§Æ½ºâ¡±×¨Ìâºó£¬ÁªÏµ¹¤ÒµÉú²úʵ¼ÊËù·¢±íµÄ¹Ûµã£¬ÄãÈÏΪ²»ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡

A£®»¯Ñ§·´Ó¦ËÙÂÊÀíÂÛÊÇÑо¿ÔõÑùÔÚÒ»¶¨Ê±¼äÄÚ¿ì³ö²úÆ·¡¡¡¡ 
B£®»¯Ñ§Æ½ºâÀíÂÛÊÇÑо¿ÔõÑùʹÓÃÓÐÏÞÔÁ϶à³ö²úÆ·¡¡¡¡ 
C£®»¯Ñ§·´Ó¦ËÙÂÊÀíÂÛÊÇÑо¿ÔõÑùÌá¸ßÔÁÏת»¯ÂÊ
D£®»¯Ñ§Æ½ºâÀíÂÛÊÇÑо¿ÔõÑùʹÔÁϾ¡¿ÉÄܶàµØת»¯Îª²úÆ· 
9.ÔÚÃܱÕÈÝÆ÷ÖнøÐÐÈçÏ·´Ó¦£ºX2(g)+Y2(g)
 2Z(g)£¬ÒÑÖªX2¡¢Y2¡¢ZµÄÆðʼŨ¶È·Ö±ðΪ0.1mol/L¡¢0.3mol/L¡¢0.2mol/L£¬ÔÚÒ»¶¨Ìõ¼þÏ£¬µ±·´Ó¦´ïµ½Æ½ºâʱ£¬¸÷ÎïÖʵÄŨ¶ÈÓпÉÄÜÊÇ ¡¡A£® ZΪ0.3mol/L¡¡¡¡¡¡ ¡¡ B£® Y2Ϊ0.4mol/L¡¡ ¡¡C£® X2Ϊ0.2mol/L¡¡¡¡ ¡¡ D£® ZΪ0.4mol/L
2Z(g)£¬ÒÑÖªX2¡¢Y2¡¢ZµÄÆðʼŨ¶È·Ö±ðΪ0.1mol/L¡¢0.3mol/L¡¢0.2mol/L£¬ÔÚÒ»¶¨Ìõ¼þÏ£¬µ±·´Ó¦´ïµ½Æ½ºâʱ£¬¸÷ÎïÖʵÄŨ¶ÈÓпÉÄÜÊÇ ¡¡A£® ZΪ0.3mol/L¡¡¡¡¡¡ ¡¡ B£® Y2Ϊ0.4mol/L¡¡ ¡¡C£® X2Ϊ0.2mol/L¡¡¡¡ ¡¡ D£® ZΪ0.4mol/L
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com