
5.≤ƒ¡œ÷–∫±º˚µƒ∏þŒ¬ÃÏ∆¯–Œ≥…µƒ‘≠“Ú «
°° A£Æ◊ºæ≤÷π∑Ê≥§∆⁄øÿ÷∆∏√∑∂Œß£¨¥”∂¯‘Ï≥… ™»»µƒ∏þŒ¬ÃÏ∆¯
°° B£Æ Ð∏±»»¥¯∏þ—π≥§∆⁄øÿ÷∆£¨ ¢––œ¬≥¡∆¯¡˜£¨‘Ï≥…ÃÏ∆¯«Á¿ ∫Õ∏þŒ¬
°° C£Æ Ð∂Ú∂˚ƒ·≈µœ÷œÛ”∞œÏ£¨µº÷¬¥Û∑∂Œßƒ⁄∆’±È∏þŒ¬
°° D£Æ Ðî∑Á”∞œÏ£¨¥”Œ˜Ã´∆Ω—Û¥¯¿¥¥Û¡ø ™»»µƒø’∆¯–Œ≥…∏þŒ¬ÃÏ∆¯
4.Œ“π˙∂´ƒœ—ÿ∫£œƒºæ≥£“◊≥ˆœ÷¥Û∑Á°¢±©”ÍÃÏ∆¯£¨∆‰”–πÿµƒÃÏ∆¯œµÕ≥ «
3.‘Ï≥……œ ˆ∫±º˚∏þŒ¬ÃÏ∆¯µƒÃÏ∆¯œµÕ≥ «
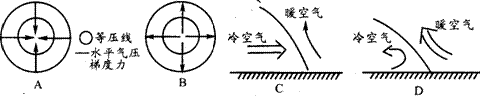 °°
°°
2£Æπÿ”⁄Õº æµÿ«¯≈©“µ…˙≤˙µƒ– ˆ£¨’˝»∑µƒ «
°°°° A.…˙≥§∆⁄≥§ «◊˜ŒÔ≤˙¡ø∏þµƒ÷˜“™‘≠“Ú°°°° B.»»¡ø «≈©“µ…˙≤˙∑¢’πµƒœÞ÷∆“ÚÀÿ
°°°° C.∆Ω‘≠√ʪ˝π„¥Û£¨µ´¡∏ ≥…Ã∆∑¬ µÕ°° °°°°D.¥Œ…˙—ŒºÓªØ «Õ¡»¿∑ ¡¶œ¬Ωµµƒ÷˜“™‘≠“Ú
ƒ≥ƒÍ7‘¬°¢8‘¬º‰£¨Œ“π˙ª™±±µÿ«¯≥÷–¯≥ˆœ÷∏þŒ¬ÃÏ∆¯£¨∆¯Œ¬Õª∆∆¿˙ ∑Õ¨∆⁄◊Ó∏þ÷µ°£º√ƒœ°¢Œ˜∞≤µ»µÿ…ı÷¡≥ˆœ÷¡À40°Êµƒ∏þŒ¬°£¥ÀÕ‚£¨≥§Ω≠÷–œ¬”Œµÿ«¯°¢ª™ƒœ°¢Àƒ¥®µ»µÿ“≤≥÷–¯≥ˆœ÷∏þŒ¬ÃÏ∆¯£¨’‚—˘¥Û∑∂Œßµƒ∏þŒ¬ÃÏ∆¯‘⁄¿˙ ∑…œÕ¨∆⁄ «∫±º˚µƒ°£∂¡œ¬¡–Àƒ∑˘∆¯¡˜–Œ≥…Õº£¨ªÿ¥3-6£∫
1£Æ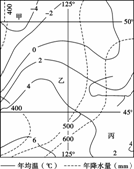 πÿ”⁄Õº æµÿ«¯µƒ– ˆ£¨’˝»∑µƒ «
πÿ”⁄Õº æµÿ«¯µƒ– ˆ£¨’˝»∑µƒ «
°°°° A.∆¯Œ¬£∫º◊£æ““£æ±˚£ªΩµÀÆ£∫º◊£º““£º±˚
°°°° B.÷ÐŒß…Ωµÿª∑»∆£¨µÿ–Œ“‘≈˵ÿŒ™÷˜
°°°° C.“ª∞„∫”¡˜√øƒÍ”–¡Ω¥Œ—¥∆⁄£¨”–µƒ¥Ê‘⁄¡Ë—¥œ÷œÛ
°°°° D.∫”¡˜æ∂¡˜¡ø÷˜“™ÀÊ∆¯Œ¬µƒ±‰ªØ∂¯±‰ªØ
29.»°12.8gµƒNH4Cl∫ÕKClπÃêÏ∫œŒÔ£¨º”ÀÆÕÍ»´»ÐΩ‚∫Û£¨º”»Î50mLµƒNaOH»Ð“∫£¨«°∫√ÕÍ»´∑¥”¶£¨º”»» π…˙≥…µƒ∆¯ÃÂÕÍ»´“ð≥ˆ£¨ ’ºØµΩ±Í◊º◊¥øˆœ¬2.24Lµƒ∆¯Ã£¨ ‘º∆À„πÃêÏ∫œŒÔ÷–KClµƒ÷ ¡ø∫ÕNaOH»Ð“∫µƒŒÔ÷ µƒ¡ø≈®∂»°£
28.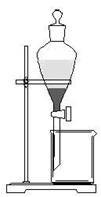 (π≤8∑÷)ƒ≥—ßœ∞–°◊È¥”∫£¥¯÷–÷»°µ•÷ µ‚£¨ µ—È≤Ω÷Ë»Áœ¬£∫
(π≤8∑÷)ƒ≥—ßœ∞–°◊È¥”∫£¥¯÷–÷»°µ•÷ µ‚£¨ µ—È≤Ω÷Ë»Áœ¬£∫
(1) µ—È “±∫…’∫£¥¯°£
(2)Ω´À˘µ√∫£¥¯ª“º”ÀÆ»ÐΩ‚°¢π˝¬À£¨À˘–˵ƒ≤£¡ß“«∆˜ «________________________°£
(3)‘⁄¬À“∫÷–ºÏ≥ˆ¡ÀI-£¨ªπºÏ≥ˆ¡ÀK+£¨ºÏ—ÈK+µƒ≤Ÿ◊˜≤Ω÷Ë «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°£
(4)–°◊ÈÕ¨—ß≤È‘ƒ¡À”–πÿ◊ ¡œ£¨À˚√«æˆ∂®”√H2O2◊ˆ—ıªØº¡£¨∑¥”¶÷–I-◊™ªØŒ™I2£¨H2O2◊™ªØŒ™____________°£
(5)–°◊È”√CCl4ðÕ»°µ‚ÀÆ÷–µƒµ‚£¨‘⁄”“Õºµƒ∑÷“∫¬©∂∑÷–£¨œ¬≤„“∫ÃÂ≥ __________…´£ªÀ˚√«¥Úø™∑÷“∫¬©∂∑ªÓ»˚£¨»¥Œ¥º˚“∫ᘜ¬£¨‘≠“Úø…ƒÐ «_____________________________°£
(6)∏√–°◊È≤ȵ√œýπÿ◊ ¡œ»Áœ¬£∫CCl4µƒ∑–µ„Œ™77.1°Ê£¨I2µƒ∑–µ„113.5°Ê£¨»€µ„Œ™184.4°Ê£¨¥”µ‚µƒCCl4»Ð“∫÷–∑÷¿Î≥ˆµ‚µ•÷ £¨”¶≤…”√µƒ∑Ω∑® «_______(ÃÓ–Ú∫≈)°£
a£Æπ˝¬À°°°° b£Æ…˝ª™°°°° c£Æ’Ù∑¢°°°° d£Æ’Ù¡Û
27. (π≤7∑÷)œ÷”√98%µƒ≈®H2SO4(√Ð∂»Œ™1.84g/cm3)¿¥≈‰÷∆500mL0.2mol£ØLµƒœ°H2SO4«Îªÿ¥œ¬¡–Œ £∫
(1) œ÷∏¯≥ˆœ¬¡–“«∆˜(≈‰÷∆π˝≥Ã÷–ø…ƒÐ”√µΩ)£∫¢Ÿ100 mL¡øÕ≤ ¢⁄10 mL¡øÕ≤ ¢€250 mL…’±≠
¢ÐÕ–≈ÃÃÏ∆Ω ¢ð500 mL»ð¡ø∆ø ¢ÞΩ∫Õ∑µŒπÐ ¢þ≤£¡ß∞Ù
∞¥±ÿ–Ë π”√“«∆˜µƒœ»∫ÛÀ≥–Ú≈≈¡–’˝»∑µƒ «________________°£
A£Æ¢Ð¢€¢þ¢ð¢Þ£ª°° B£Æ¢⁄¢ð¢þ¢Þ£ª°° C£Æ¢Ÿ¢€¢ð¢Þ¢þ£ª°° D£Æ¢⁄¢Þ¢€¢þ¢ð¢Þ
(2)æ≠º∆À„£¨–Ë≈®H2SO4µƒÃª˝Œ™°° °°°°°°°°°°°°°°°£
(3)Ω´À˘≈‰÷∆µƒœ°H2SO4Ω¯––≤‚∂®£¨∑¢œ÷≈®∂»¥Û”⁄0.2mol£ØL°£«Îƒ„∑÷Œˆœ¬¡–ƒƒ–©≤Ÿ◊˜ª·“˝
∆À˘≈‰≈®∂»∆´¥Û(ÃÓ–¥◊÷ƒ∏)°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
A£Æ”√¡øÕ≤¡ø»°≈®¡ÚÀ· ±£¨—ˆ ”¡øÕ≤µƒøÃ∂»°°°°°°°° B£Æ»ð¡ø∆øŒ¥∏…‘Ôº¥”√¿¥≈‰÷∆»Ð“∫
C£Æ≈®¡ÚÀ·‘⁄…’±≠÷–œ° Õ∫Û£¨Œ¥¿‰»¥æÕ¡¢º¥◊™“∆µΩ»ð¡ø∆ø÷–£¨≤¢Ω¯––∂®»ð£ª
D£ÆÕ˘»ð¡ø∆ø◊™“∆ ±£¨”–…Ÿ¡ø“∫ÃÂΩ¶≥ˆ°° E£Æ…’±≠Œ¥Ω¯––œ¥µ”
F£Æ‘⁄»ð¡ø∆ø÷–∂®»ð ±∏© ”»ð¡ø∆øøÃ∂»œþ°°°°°°°°°°°°°°°°
G£Æ∂®»ð∫Û»˚…œ∆ø»˚∑¥∏¥“°‘»£¨æ≤÷√∫Û£¨“∫√Ê≤ªµΩøÃ∂»œþ£¨‘Ÿº”ÀÆ÷¡øÃ∂»œþ°£
26£Æ(π≤5∑÷)”–“ª∆ø»Ð“∫÷ª∫¨Cl-°¢CO32-°¢SO42-°¢Na+°¢NH4+°¢K+°¢Mg2+ ∆þ÷÷¿Î◊”÷–µƒƒ≥º∏÷÷°£æ≠ µ—È£∫
(1)‘≠»Ð“∫  °°∞◊…´≥¡µÌ£ª
°°∞◊…´≥¡µÌ£ª
(2)Ω´(1)À˘µ√»Ð“∫
 °°≤˙…˙ π◊œ…´ Ø»Ô ‘“∫±‰¿∂µƒ∆¯Ã£ª
°°≤˙…˙ π◊œ…´ Ø»Ô ‘“∫±‰¿∂µƒ∆¯Ã£ª
(3)‘≠»Ð“∫÷–º”BaCl2»Ð“∫≤ª≤˙…˙≥¡µÌ£ª
(4)‘≠»Ð“∫÷–º”AgNO3»Ð“∫≤˙…˙∞◊…´≥¡µÌ£¨‘Ÿº”œ°œıÀ·∞◊…´≥¡µÌ≤ª»ÐΩ‚°£
ªÿ¥œ¬¡–Œ £∫
(1) ‘∑÷Œˆ‘≠»Ð“∫÷–“ª∂®∫¨”–µƒ¿Î◊” « °°°°°°°°°°°°£¨“ª∂®≤ª∫¨”–µƒ¿Î◊” « °°°°°°°°°°£¨ ø…ƒÐ∫¨”–µƒ¿Î◊” « °°°°°°°°°°°°°°°°°£
(2)”–Õ¨—ß»œŒ™ µ—È(4)ø…“‘ °¬‘£¨ƒ„»œŒ™ƒÿ£ø(ÃÓ∑˚∫≈£∫A£≠ø…“‘£¨B £≠≤ªø…“‘)°°°°°°°°°° °°
Àµ√˜¿Ì”…°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
25.(π≤6∑÷)Œ“π˙’˛∏ÆŒ™¡Àœ˚≥˝µ‚»±∑¶≤°£¨πÊ∂®‘⁄ ≥—Œ÷–±ÿ–κ”»Î ¡øµƒµ‚À·ºÿ°£ºÏ—È ≥—Œ÷– «∑Òº”µ‚£¨ø…¿˚”√»Áœ¬∑¥”¶£∫ KIO3+5KI+3H2SO4==3K2SO4+ 3I2+ 3H2O
(1)∏√∑¥”¶÷–—ıªØº¡∫Õªπ‘≠º¡µƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™°°°°°° °£
(2)»Áπ˚∑¥”¶÷–◊™“∆0.2molµÁ◊”£¨‘Ú…˙≥…I2µƒŒÔ÷ µƒ¡øŒ™_________________°£
(3)¿˚”√…œ ˆ∑¥”¶ºÏ—È ≥—Œ÷– «∑Òº”µ‚£¨À˘–Ë ‘º¡ «_____________(ÃÓœ¬¡–—°œÓµƒ–Ú∫≈)
¢Ÿµ‚ÀÆ°°°° ¢⁄KI»Ð“∫°°°° ¢€µÌ∑€»Ð“∫°°°° ¢Ðœ°¡ÚÀ·°°°°°° ¢ðAgNO3»Ð“∫
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com