
13.将2mol H2O和2mol CO置于1L容器中,在一定条件下,加热至高温,发生如下可逆反应:2H2O(g)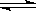 2H2+O2
2H2+O2
2CO+O2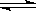 2CO2
2CO2
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是 和 ,或 和 。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为 n(O2)平=a mol, n(CO2)平=b mol。
试求n(H2O)平= 。(用含a、b的代数式表示)
12. 某溶液中发生反应:A
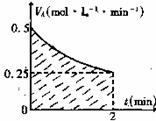
某溶液中发生反应:A 2B+C,VA-t 的关系如右图。已知溶液的体积为2L,起始时体系中只有A,请回答下列问题:
2B+C,VA-t 的关系如右图。已知溶液的体积为2L,起始时体系中只有A,请回答下列问题:
(1)图中阴影部分的面积表示2min内 的减小值,应小于 ;
(2)2min时,B的物质的量浓度的取值范围是
11.对于反应2L(g)+3 M(g)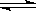 xQ(g)+3R(g),在容积为2L的密闭容器中,将2mol气体L和3mol气体M混合,当反应经2min后达平衡时生成2.4
mol气体R,并测得Q的浓度为0.4mol/L,则x的值为
,L的转化率为
,v(M)=
xQ(g)+3R(g),在容积为2L的密闭容器中,将2mol气体L和3mol气体M混合,当反应经2min后达平衡时生成2.4
mol气体R,并测得Q的浓度为0.4mol/L,则x的值为
,L的转化率为
,v(M)=
10.在恒温、恒容下,当反应容器内总压强不随时间变化时,下列可逆反应一定达到平衡的是
A.A(g)+B(g) C(g)
B.A(g)+2B(g)
C(g)
B.A(g)+2B(g) 3C(g)
3C(g)
C.A(g)+B(g) C(g)+D(g) D.以上都达到平衡
C(g)+D(g) D.以上都达到平衡
9.可逆反应∶2NO2 2NO+O2在密闭容器中反应,达到平衡状态的标志是:①单位时间内生成n molO2的同时生成2n molNO2;②单位时间内生成n molO2 的同时,生成2n mol NO;③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态;④混合气体的颜色不再改变的状态;⑤混合气体的密度不再改变的状态;⑥ 混合气体的平均相对分子质量不再改变的状态
2NO+O2在密闭容器中反应,达到平衡状态的标志是:①单位时间内生成n molO2的同时生成2n molNO2;②单位时间内生成n molO2 的同时,生成2n mol NO;③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态;④混合气体的颜色不再改变的状态;⑤混合气体的密度不再改变的状态;⑥ 混合气体的平均相对分子质量不再改变的状态
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
8.能够充分说明恒温下的密闭容器中反应:2SO2+O2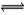 2SO3,已经达到平衡的标志是
2SO3,已经达到平衡的标志是
A.容器中SO2、O2、SO3共存 B.容器中SO2和SO3的浓度相同
C.容器中SO2、O2、SO3的物质的量为2∶1∶2 D.容器中压强不随时间的变化而改变
7.下列哪种说法可以证明反应.N2+3H2 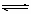 2NH3已达到平衡状态
2NH3已达到平衡状态
A.1个N≡N键断裂的同时,有3个H-H键形成
B.1个N≡N键断裂的同时,有3个H-H键断裂
C.1个N≡N键断裂的同时,有6个N-H键断裂
D.1个N≡N键断裂的同时,有6个N-H键形成
6.在一定条件下,可逆反应2A 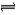 B+3C在下列4种状态中,处于平衡状态的是
B+3C在下列4种状态中,处于平衡状态的是
A.正反应速度 vA=2mol/(L·min) 逆反应速度 vB=2 mol/(L·min)
B.正反应速度 vA=2mol/(L·min) 逆反应速度 vC=2 mol/(L·min)
C.正反应速度 vA=1mol/(L·min) 逆反应速度 vB=1.5 mol/(L·min)
D.正反应速度 vA=1mol/(L·min) 逆反应速度 vC=1.5mol/(L·min)
5.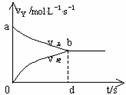 在容积固定的2L密闭容器中,充入X、Y各2mol,发生可逆反
在容积固定的2L密闭容器中,充入X、Y各2mol,发生可逆反
应 X(g)+2Y(g)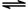 2Z(g)
,并达平衡,以Y的浓度改变表示的反应速
2Z(g)
,并达平衡,以Y的浓度改变表示的反应速
率v正、v逆与时间t的关系如图。则Y的平衡浓度的表达式正确的是
(式中S指对应区域的面积)
A.2-Saob B.2-Sbod C.1-Saob D.1-Sbod
4.在密闭容器中进行如下反应:X2(g)+Y2(g) 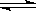 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol·Lˉ1、0.3 mol·Lˉ1、0.2 mol·Lˉ1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是(mol·Lˉ1)
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol·Lˉ1、0.3 mol·Lˉ1、0.2 mol·Lˉ1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是(mol·Lˉ1)
A.Z为0.3 B.Y2为0.4 C.X2为0.2 D.Z为0.4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com