
9、锌与100mL1mol/L盐酸反应的实验中,若设想向溶液中加入少量的①醋酸钠,②溴化铜,③醋酸铜(均为可溶性),并测定生成H2的速率(mL/min),预计三种方案的速率大小是 ( )
A、①>③>② B、③>②>① C、②>③>① D、①>②>③
8、如下图所示的装置,在盛有水的烧坏中,铁圈和银圈的连接处吊着一根绝缘的
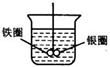 细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.片刻后可观察到的现象是( )
细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.片刻后可观察到的现象是( )
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
7、100 mL浓度为2 mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是 ( )
A.加入适量的6 mol/L的盐酸 B.加入数滴氯化铜溶液 C.加入适量蒸馏水 D.加入适量的氯化钠溶液
6、某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是 ( )
A:正极为Cu,负极为Fe,电解质为FeCl3溶液
B:正极为C,负极为Fe,电解质为Fe(NO3)3溶液
C:正极为Fe,负极为Zn,电解质为Fe2(SO4)3溶液
D:正极为Ag,负极为Fe,电解质为CuSO4 溶液
5、一个原电池的总反应的离子方程式是Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是 ( )
|
|
A |
B |
C |
D |
|
正极 |
Zn |
Cu |
Zn |
Fe |
|
负极 |
Cu |
Zn |
Ag |
Zn |
|
电解质溶液 |
CuCl2 |
H2SO4 |
CuSO4 |
CuCl2 |
4、在用Zn、Cu片和稀H2SO4组成的原电池装置中,经过一段时间工作后,下列说法中正确的是( )
A. 锌片是正极,铜片上有气泡产生 C 电流方向是从锌片流向铜片
B. 溶液中H2SO4 的物质的量减少 D 电解液的pH保持不变
3、把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上 有大量气泡产生,则四种金属的活动性顺序由强到弱为 ( )
A.a>b>c>d B.a>c>d>b C.c>a>b>d D.b>d>c>a
2、下列关于原电池的叙述正确的是 ( )
A:构成原电池的正极和负极必须是两种不同的金属 B:原电池是化学能转变为电能的装置
C:在原电池中,电子流出的一极是负极,该电极被还原 D:原电池放电时,电流的方向是从负极到正极
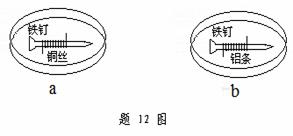
1、(08年重庆理综·12)如题12图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。下列叙述正确的是( )
A.a中铁钉附近呈现红色 B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应D.b中铝条附近有气泡产生
7、 形成原电池的条件
典型例题:
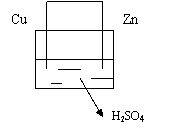 例1:如右图:写出电极反应:正极:
负极:
例1:如右图:写出电极反应:正极:
负极:
总方程式为: 。电子的流向:
电流的流向: 在电解质溶液中H+运动到: 极。
实现的能量转化: 。
上述原电池工作一段时间后,硫酸溶液的pH怎样变化: 。
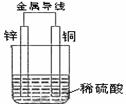
例2:关于如图所示装置的叙述,正确的是( )
A、铜是阳极,铜片上有气泡产生 B、铜片质量逐渐减少
C、电流从锌片经导线流向铜片 D、氢离子在铜片表面被还原
例3:(08年宁夏理综·10)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是( )
A.CH3OH(g)+O2(g)=H2O(1)+CO2(g)+2H+(aq)+2e-
B.O2(g)+4H+(aq)+4e-=2H2O(1)
C.CH3OH(g)+H2O(1)=CO2(g)+6H+(aq)+6e-
D.O2(g)+2H2O(1)+4e-=4OH-
例4:(09年北京顺义)依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池如图所示。
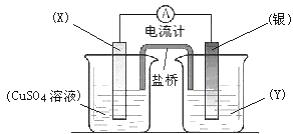
请回答下列问题:
(1)电极X的材料是_________;电解质溶液Y是_________;
(2)银电极为电池的_________极,发生的电极反应为________________________;X电极上发生的电极反应为___________________________;
(3)外电路中的电子是从_________电极流向_________电极。
 强化训练:
强化训练:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com