
8. 洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如
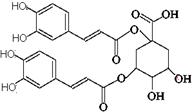
洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如 下图所示,有关洋蓟素的说法正确的是
下图所示,有关洋蓟素的说法正确的是
A.分子中含有4个手性碳原子
B.不能与氯化铁溶液发生显色反应
C.一定条件下能发生酯化反应和消去反应
D.1mol洋蓟素最多可与11molNaOH反应
7.下列化学实验事实解释正确的是
A.过量的铜屑与稀硝酸作用,反应停止后,再加入1mol/L稀硫酸,铜屑又逐渐溶解,是 因为铜可直接与1mol/L稀硫酸反应
因为铜可直接与1mol/L稀硫酸反应
B.铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面形成了一层致密稳定的氧化膜
C.相同物质的量浓度乙酸铅溶液导电能力比乙酸钙弱得多,说明乙酸铅属于非电解质
D.浓NH4Cl溶液处理过的舞台幕布不易着火,是因为处理后幕布质量增加,着火点升高
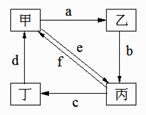
6.下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
物质 编号 |
物质转化关系 |
甲 |
乙 |
丙 |
丁 |
|
① |
 |
Cu[ |
CuO |
CuCl2 |
Cu(NO3)2[来 |
|
② |
Na2CO3 |
NaOH |
NaHCO3 |
CO2 |
|
|
③ |
(NH4)2SO3 |
CaSO3 |
SO2 |
NH4HSO3 |
|
|
④ |
Al(OH)3 |
Al2O3 |
NaAlO2 |
AlCl3 |
A.①②③④ B.①②③ C.①③④ D.②④
5.香花石由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,X、Y、Z为金属元素,Z的最外层电子数与次外层相等, X、Z位于同主族,Y、Z、R、T位于同周期, R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法不正确的是
A.原子半径:Y>Z>R>T
B.气态氢化物的稳定性:W<R<T
C.最高价氧化 物对应的水化物碱性:X>Y>Z
物对应的水化物碱性:X>Y>Z
D.XR2、WR2两化合物中R的化合价相同
4.在下列各组溶液中,离子一定能大量共存的是
A.加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I-
B.常温下,pH=1的溶液:Fe3+、Na+、NO3-、SO42-
C.滴入酚酞试液显红色的溶液:Mg2+、Al3+、Br-、SO42-
D.含0.1mol/LNH4Al(SO4)2·12H2O的溶液:K+、Ca2+、NO3-、OH-
3.用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.3.6g碳与3.36LO2一定条件下恰好完全反应,生成CO分子数一定为0.3 NA
B.6.9g钠与足量的CO2和H2O(g)混合气体充分反应,转移的电子数一定为0.3NA
C.25℃时, 0.15mol/L的Na2CO3溶液中,Na+数目为0.3NA
D.标准状况下,2.24L氯仿中含有C-Cl数目为0.3NA
2. 食盐、蔗糖、醋酸、纯碱、汽油、“84消毒液”等是日常生活中经常使用的物质,下列有关说法或表示正确的是
食盐、蔗糖、醋酸、纯碱、汽油、“84消毒液”等是日常生活中经常使用的物质,下列有关说法或表示正确的是
A.食盐中阴离子的核外电子排布式为:
B.蔗糖与醋酸的最简式相同
C.纯碱与汽油去除油污的原理相同
D.“84消毒液”中有效成分NaClO的电子式为: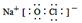
1.节能减排是社会赋予的责任和使命,从衣、食、住、行、用等方面,下列行为不利于低碳生活的是
①用LED半导体节能照明灯代替传统的白炽灯
②购物时提倡用超薄一次性塑料袋
③推广使用一次性筷子
④在农村推广沼 气照明和供热
气照明和供热
⑤用大排量的轿车代替公交车出行
⑥合理节食,减少每天摄入的热量,同时减少脂肪和糖类的摄入量
A.②③④⑤ B.②③④⑥ C.②③⑤ D. ①⑤⑥
33.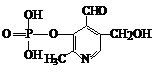
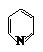 (13分)磷酸吡醛是细胞的重要组成部分,可视为由磷酸形成的酯,其结构式如下。
(13分)磷酸吡醛是细胞的重要组成部分,可视为由磷酸形成的酯,其结构式如下。
已知吡啶( )与苯环性质相似。请回答下列问题:
(1)下面有关磷酸吡醛叙述不正确的是
A.能与金属钠反应 B. 能发生消去反应
C.能发生银镜反应 D. 能使石蕊试液变红
E.1mol该酯与NaOH溶液反应,消耗4molNaOH
F. 吡啶环上只有醛基可以被酸性KMnO4溶液氧化成羧基
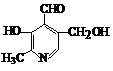 (2)请完成磷酸吡醛在酸性条件下水解的反应方程式:
(2)请完成磷酸吡醛在酸性条件下水解的反应方程式:
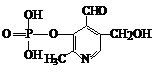
 + H2O
+
+ H2O
+
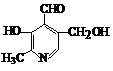 (3)
与足量H2发生加成反应的产物的结构简式为
;
(3)
与足量H2发生加成反应的产物的结构简式为
;
它与银氨溶液发生银镜反应的化学方程式为: 。
32. (15分)德国人哈伯在1909年发明的合成氨反应原理为:
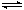 N2(g)+3H2(g)
2NH3(g) 已知298K时:△H=-92.4kJ·mol-1 。请回答:
N2(g)+3H2(g)
2NH3(g) 已知298K时:△H=-92.4kJ·mol-1 。请回答:
(1)在298K时,将10mol N2和30mol H2放入合成塔中,放出的热量小于924kJ的原因是 。
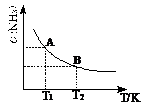 (2)在一定条件下,将1mol N2与3mol H2混合于一个10L密闭容器中,反应达到A平衡时,混合气体中氨占25%,试回答:
(2)在一定条件下,将1mol N2与3mol H2混合于一个10L密闭容器中,反应达到A平衡时,混合气体中氨占25%,试回答:
①N2的转化率αA为 。
②在状态A时,平衡常数KA= (代入数
值的表达式,不写出具体数值);如右图:当温度由T1变化到T2时,
 KA KB(填“>”、“<”或“=”)
KA KB(填“>”、“<”或“=”)
(3)在1998年希腊亚里斯多德大学的Marmellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨,其实验装置如右图,
则正极的电极反应式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com