
6.反应A(g)+3B(g) 2C(g) △H<0,达到平衡后,将气体混合物的温度降低,下列叙述中正确的是( )
2C(g) △H<0,达到平衡后,将气体混合物的温度降低,下列叙述中正确的是( )
A.正反应速率加大,逆反应速率减小,平衡向正反应方向移动
B.正反应速率变小,逆反应速率增大,平衡向逆反应方向移动
C.正反应速率和逆反应速率减小,平衡向正反应方向移动
D.正反应速率和逆反应速率减小,平衡向逆反应方向移动
5.在固定容积的密闭容器中,可逆反应2X +Y(g)  Z(s)已达到平衡,此时升高温度则气体混合物的密度增大。下列叙述正确的是(
)
Z(s)已达到平衡,此时升高温度则气体混合物的密度增大。下列叙述正确的是(
)
A.若X为非气态,则正反应为吸热反应
B.正反应为放热反应,X一定为气态
C.正反应为放热反应,X可能是气态、液态或固态
D.若加入少量的Z,该平衡向左移动
4.已知热化学方程式2SO2(g) + O2(g)
 2 SO3(g) △H =
-Q kJ/mol(Q>0),则下列说法正确的是( )
2 SO3(g) △H =
-Q kJ/mol(Q>0),则下列说法正确的是( )
A.2 mol SO2(g)和1 mol O2(g)所具有的内能小于2 mol SO3(g)所具有的内能
B.将2 mol SO2(g)、1 mol O2(g)置于一密闭容器中充分反应后放出QkJ的热量
C.升高温度,平衡向逆反应移动,上述热化学方程式中的Q值减小
D.如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QkJ,则此过程中有
2 mol SO2(g)被氧化
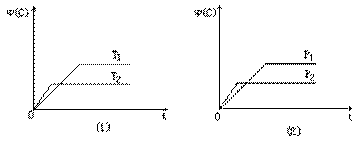
3.可逆反应mA(s)+nB(g) eC(g)+fD(气)反应过程中,当其他条件不变时,C的体积分数j(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是( )
eC(g)+fD(气)反应过程中,当其他条件不变时,C的体积分数j(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是( )
A.达到平衡后,若使用催化剂,C的体积分数将增大
B.当平衡后,若温度升高,化学平衡向逆反应方向移动
C.化学方程式中,n>e+f
D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
2.一定温度下,在固定容积的密闭容器中,可逆反应:mA(g)+nB(g) pCg)+qD(g),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化,②体系的密度不再发生变化,③各组分的物质的量浓度不再改变,④各组分的质量分数不再改变,⑤反应速率vA:vB:vC:vD=m:n:p:q,其中,能说明反应已达到平衡的是( )
pCg)+qD(g),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化,②体系的密度不再发生变化,③各组分的物质的量浓度不再改变,④各组分的质量分数不再改变,⑤反应速率vA:vB:vC:vD=m:n:p:q,其中,能说明反应已达到平衡的是( )
A.只有③④ B.②③④ C.①②③④ D.①②③④⑤
1.有一处于平衡状态的反应X(g)+3Y(g) 2Z(g)
△H<0,为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z(g)
△H<0,为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
A.①③⑤ B.②③⑤ C.②③⑥ D.②④⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com