
23£®(6·Ö)FeS±„ŗĶČÜŅŗÖŠ“ęŌŚČēĻĀĘ½ŗā£ŗFeS(s)  Fe2++S2-”” Ksp=8.1”Į10-17 mol2”¤L-2
Fe2++S2-”” Ksp=8.1”Į10-17 mol2”¤L-2
(1)ĄķĀŪÉĻµÄFeSµÄČܽā¶ČĪŖ”””””””””””””””””””””””””””” ”£
(2)ÓÖÖŖFeS±„ŗĶČÜŅŗÖŠ[H+]Óė[S2-]Ö®¼ä“ęŌŚŅŌĻĀĻŽĮæ¹ŲĻµ£ŗ[H+]2 [S2-]=1.0”Į10-22mol3”¤L-3£¬ĪŖĮĖŹ¹±„ŗĶČÜŅŗĄļ[Fe2+]“ļµ½1mol”¤L-1£¬ĻÖ½«ŹŹĮæFeSĶ¶ČėĘ䱄ŗĶČÜŅŗÖŠ£¬Ó¦µ÷½ŚČÜŅŗÖŠµÄ[H+]ĪŖ__________________________”£
22£®(6·Ö)ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬±ł“×Ėį¼ÓĖ®Ļ”ŹĶ¹ż³ĢÖŠ£¬ČÜŅŗµÄµ¼µēÄÜĮ¦ČēÓŅĶ¼ĖłŹ¾”£Ēė»Ų“š£ŗ
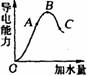 (1)”°O”±µćµ¼µēÄÜĮ¦ĪŖ”°0”±µÄĄķÓÉŹĒ””””””””””””””””””””””””””””””””””
ӣ
(1)”°O”±µćµ¼µēÄÜĮ¦ĪŖ”°0”±µÄĄķÓÉŹĒ””””””””””””””””””””””””””””””””””
ӣ
(2)A”¢B”¢CČżµćpHÓɓ󵽊”µÄĖ³ŠņŹĒ_______________________”£
(3)A”¢B”¢CČżµćµēĄė¶Č×ī“óµÄŹĒ____________________”£
21£®(8·Ö)ĻĀĮŠĪļÖŹ£ŗ¢ŁÄܵ¼µēµÄÓŠ”””””””” ””””””””””£¬¢ŚŹōÓŚµē½āÖŹµÄÓŠ”””” ””””””””””””””£¬¢ŪŹōÓŚ·Ēµē½āÖŹµÄÓŠ”””””””””””””””””””””” £¬¢ÜŹōÓŚĒæµē½āÖŹµÄÓŠ”””””””””””””””””””””” ”£
A£®NaOHČÜŅŗ”””” B£®Cu”””””””” C£®ŅŗĢ¬HCl”””””””” D£®ŅŗĢ¬CH3COOH”””” E£®ÕįĢĒ”””” F£®°±Ęų
G£®CuSO4”””” ””””H£®ŹÆÄ«”””””” I£®Na2O”””” ””””””””J£®ĪŽĖ®ŅŅ“¼
20£®5000CŹ±£¬Ļņ¼×ČŻĘ÷ÖŠ³äČė1molSO3£¬ĻņĻąĶ¬ČŻ»żµÄŅŅČŻĘ÷ÖŠ³äČė1molSO2ŗĶ0.5molO2”£Čō¼×ČŻĘ÷±£³ÖČŻ»ż²»±ä£¬ŅŅČŻĘ÷±£³ÖŃ¹Ēæ²»±ä£¬·Ö±š“ļµ½Ę½ŗā£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ (”””” )
A£®Ę½ŗāŹ±ČŻĘ÷ÄŚµÄŃ¹Ēæ£ŗ¼×>ŅŅ”””””””””” B£®Ę½ŗāŹ±ČŻĘ÷ÄŚµÄŃ¹Ēæ£ŗŅŅ>¼×
C£®Ę½ŗāŹ±ČŻĘ÷ÄŚO2µÄĢå»ż·ÖŹż£ŗŅŅ>¼×”” D£®Ę½ŗāŹ±ČŻĘ÷ÄŚSO3µÄĢå»ż·ÖŹż£ŗ¼×>ŅŅ
µŚ¢ņ¾ķ(·ĒŃ”ŌńĢā£¬¹² 40·Ö)
19£®ČōpH=3µÄĖįČÜŅŗŗĶpH=11µÄ¼īČÜŅŗµČĢå»ż»ģŗĻŗóČÜŅŗ³ŹĖįŠŌ£¬ĘäŌŅņæÉÄÜ”” (”” ””””)
A£®Éś³ÉŅ»ÖÖĒæĖįČõ¼īŃĪ”””””” ””””””””B£®ČõĖįČÜŅŗŗĶĒæ¼īČÜŅŗ
C£®ĒæĖįÓėČõ¼īČÜŅŗ·“Ó¦”””””””””””” D£®Ņ»ŌŖĒæĖįČÜŅŗÓėŅ»ŌŖĒæ¼īČÜŅŗ·“Ó¦
18£®ĻĀĮŠČÜŅŗÖŠÓŠ¹ŲĪļÖŹµÄĮæÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ”””””””” ””””””””””””””””””(”” ””””)
A£®pH=2µÄHAČÜŅŗÓėpH=12µÄMOHČÜŅŗČĪŅā±Č»ģŗĻ£ŗ
c(H+) + c(M+) = c(OH-) + c(A-)
B£®pHĻąµČµÄCH3COONa”¢NaOHŗĶNa2CO3ČżÖÖČÜŅŗ£ŗ
c(NaOH)£¼c(CH3COONa)£¼c(Na2CO3)
C£®ĪļÖŹµÄĮæÅضČĻąµČCH3COOHŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻ£ŗ
c(CH3COO-) +2c(OH-) £¾ 2c(H+) + c(CH3COOH)
D£®0.1 mol”¤L-1µÄNaHAČÜŅŗ£¬ĘäpH=4£ŗc(HA-)£¾c(H+)£¾c(H2A)£¾c(A2-)
17£®ŌŚŅ»¶ØĢå»żpH=aµÄBa(OH)2ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄNaHSO4ČÜŅŗ£¬µ±ČÜŅŗÖŠµÄBa2+ Ē”ŗĆĶźČ«³ĮµķŹ±£¬ÓĆČ„Ba(OH)2ČÜŅŗÓėNaHSO4ČÜŅŗµÄĢå»ż±ČĪŖ1:4£¬ĖłµĆČÜŅŗpHĪŖ11£¬ŌņaÖµµČÓŚ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””” (”” ””””)
A£®10”””””””””””””” B£®11”””””””””””” C£®12”””””” ””””””D£®13
16£®ŅŃÖŖĻĀĮŠ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ¢ŁC(s)+O2(g)=CO2(g)£»”÷H1=-393.5kJ/mol ””””””””””””””””¢ŚCH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)£»”÷H2=-870.3kJ/mol”””””””” ¢ŪH2(g)+1/2 O2(g)=H2O(l)£»”÷H3=-285.8kJ/mol”””” Ōņ·“Ó¦2C(s)+2H2(g)+O2(g)=CH3COOH(l)µÄ”÷HĪŖ”” ””(”””””” )
A£®+488.3kJ/mol”””””” B£®-488.3 kJ/mol”””””” C£®-244.15 kJ/mol”””””” D£®+244.15 kJ/mol
15£®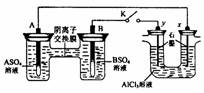 ijĶ¬Ń§°“ÓŅĶ¼ĖłŹ¾µÄ×°ÖĆ½ųŠŠŹŌŃ锣 A”¢BĪŖĮ½ÖÖ³£¼ū½šŹō£¬ĖüĆĒµÄĮņĖįŃĪæÉČÜÓŚ
ijĶ¬Ń§°“ÓŅĶ¼ĖłŹ¾µÄ×°ÖĆ½ųŠŠŹŌŃ锣 A”¢BĪŖĮ½ÖÖ³£¼ū½šŹō£¬ĖüĆĒµÄĮņĖįŃĪæÉČÜÓŚ Ė®”£µ± K ±ÕŗĻŹ±£¬ŌŚ½»»»Ä¤“¦ SO42Ņ»“Ó
Ė®”£µ± K ±ÕŗĻŹ±£¬ŌŚ½»»»Ä¤“¦ SO42Ņ»“Ó ÓŅĻņ×óŅĘ¶Æ”£ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ(”””” )
ÓŅĻņ×óŅĘ¶Æ”£ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ(”””” )
A£®ČÜŅŗÖŠ£¬A2+ÅØ¶Č¼õŠ” 
B£®BµÄµē¼«·“Ó¦£ŗB£2e-=B2+ 
C£®yµē¼«ÉĻÓŠ H2 ²śÉś£¬·¢Éś»¹Ō·“Ó¦
D£®·“Ó¦³õĘŚ£¬xµē¼«ÖÜĪ§³öĻÖ°×É«½ŗד³Įµķ£¬²»¾Ć³ĮµķČܽā
14£®ĻĀĮŠ¹ŲÓŚµē½āÖŹµēĄėµÄŠšŹöÖŠ£¬ÕżČ·µÄŹĒ”””””””””””””””””””””””””””” (”” ””””)
A£®Ģ¼ĖįøĘŌŚĖ®ÖŠČܽā¶ČŗÜŠ”£¬ĘäČÜŅŗµÄµē×čĀŹŗÜ“ó£¬ĖłŅŌĢ¼ĖįøĘŹĒČõµē½āÖŹ
B£®Ģ¼ĖįøĘŌŚĖ®ÖŠµÄČܽā¶ČŗÜŠ”£¬µ«±»ČܽāµÄĢ¼ĖįøĘČ«²æµēĄė£¬ĖłŅŌĢ¼ĖįøĘŹĒĒæµē½āÖŹ
C£®ĀČĘųŗĶ°±ĘųµÄĖ®ČÜŅŗµ¼µēŠŌ¶¼ŗÜŗĆ£¬ĖłŅŌĖüĆĒŹĒĒæµē½āÖŹ
D£®Ė®ÄѵēĄė£¬“æĖ®¼øŗõ²»µ¼µē£¬ĖłŅŌĖ®ŹĒ·Ēµē½āÖŹ
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com