
27.(13分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
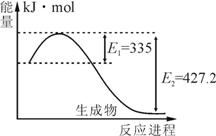 (1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为_________。
(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为_________。
|
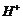 )实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2
)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2 2NH3,则在电化学合成氨的过程中,阴极反应式为_________。
2NH3,则在电化学合成氨的过程中,阴极反应式为_________。
(3)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
△H<0,其化学平衡常数K与t的关系如下表:(已知K=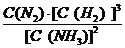 ,C(N2)、C(H2)、C(NH3)分别为平衡浓度)
,C(N2)、C(H2)、C(NH3)分别为平衡浓度)
|
t / K |
298 |
398 |
498 |
…… |
|
K / (mol·L-1)-2 |
4.1×106 |
K1 |
K2 |
…… |
请完成下列问题:
①试确定K1的相对大小,K1_______4.1×106(填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是_______(填序号字母)。
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.2v(N2)(正) = v(H2)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
(4)①NH4Cl溶液呈酸性,这是由于NH4+水解的缘故。则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是___________________。
②某氨水的pH=x,某盐酸的pH=y,x+y=14,且x>11,将上述氨水和盐酸等体积混合后,所得溶液中各种离子的浓度由大到小的顺序为( )
A.C(Cl-)>C(NH4+)>C(H+)>C(OH-)
B.C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C.C(Cl-)>C(NH4+)>C(OH-)>C(H+)
D.C(NH4+)>C(Cl-)>C(H+)>C(OH-)
13.如右图所示,a、b是两根石墨棒,下列叙述正确的是( )
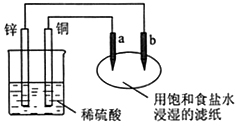 A.a是正极,发生还原反应,b是阴极,发生还原反应
A.a是正极,发生还原反应,b是阴极,发生还原反应
B.装置工作时,稀硫酸溶液中C(H+)变小、C(Cu2+)变大
C.往滤纸上滴加酚酞试液,a极附近颜色变红
D.稀硫酸中硫酸根离子的物质的量不变
第Ⅱ卷(非选择题)
12.维生素E是一种脂溶性维生素,有抗衰老的特殊作用。维生素E有四种类型,其结构简式如图所示[R为(CH2)3CH(CH3)(CH2)3CH(CH3)(CH2)3CH(CH3)2]。
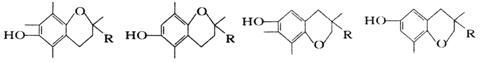
下列说法中,正确的是( )
A.四种维生素E均能与烧碱溶液反应 B.四种维生素E均能与溴水反应
C.四种维生素E互为同分异构体 D.四种维生素E均能在稀硫酸中水解
11.下列实验操作示意图所示的实验操作正确的是( )
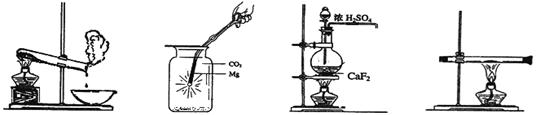
A.加热结晶水合物 B.镁条在二氧化碳里燃烧 C.制备较纯净的HF D.红磷转变成白磷
10.现有M、N、P、E四种元素,有以下反应:(1)在水溶液中,M+N2+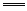 M2++N(2)P+2H2O(l)
M2++N(2)P+2H2O(l)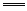 P(OH)2+H2↑(3)N、E相连浸入稀H2SO4中,电极反应:
P(OH)2+H2↑(3)N、E相连浸入稀H2SO4中,电极反应:
N-2e
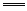 N2+,2H++2e
N2+,2H++2e
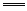 H2↑,判断元素的还原性由强到弱的顺序是( )
H2↑,判断元素的还原性由强到弱的顺序是( )
A.M、N、P、E B.M、N、E、P
C.P、M、N、E D.E、P、M、N
9.下列说法正确的是( )
A.最外层有4个电子的原子都是非金属原子
B.同一主族的两种元素的原子序数之差不可能是44
C.COCl2分子和CCl4分子中所有原子都满足最外层8电子结构
D.同主族金属的原子半径越大熔点越高
8.设NA 代表阿伏加德罗常数的数值,下列说法中正确的是( )
①常温常压下,17g 甲基(―14CH3)所含的中子数为9NA
②常温常压22.4L NO气体的分子数小于NA
③ 64g的铜发生氧化还原反应,一定失去2NA个电子
④常温常压下,100mL 0.5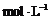 的乙酸溶液中,乙酸的分子数目小于0.05NA
的乙酸溶液中,乙酸的分子数目小于0.05NA
⑤标况时,22.4L二氯甲烷所含有的分子数为NA
⑥常温常压下,1 mol氦气含有的核外电子数为 4NA
A.①② B. ③④ C. ②④ D. ⑤⑥
7.下列各组离子能在指定溶液中,能大量共存的是( )
①无色溶液中:K+,Cl-,Ca2+,CO32‑,SO42‑,NO3-
②pH=11的溶液中:CO32-,Na+,AlO2‑,NO3‑,S2-,SO32-
③水电离的H+浓度c(H+)=10-12mol·L-1的溶液中:Cl-,CO32-,NO3-,NH4+,SO32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使石蕊变红的溶液中:Fe2+,MnO4-,NO3-,Na+,SO42-
⑥中性溶液中:Fe3+,Al3+,NO3-,I‑,Cl‑,S2‑
A.①②⑤ B.①③⑥ C.②④ D.①②④
6.向100
mL 0.250 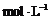 的AlCl3溶液中加入金属钠完全反应,恰好生成只含NaCl和NaAlO2的澄清溶液,则加入金属钠的质量是( )
的AlCl3溶液中加入金属钠完全反应,恰好生成只含NaCl和NaAlO2的澄清溶液,则加入金属钠的质量是( )
A.3.45 g B.2.30 g C.1.15 g D.0.575 g
19.数列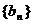 满足
满足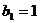 ,
,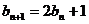 ,若数列
,若数列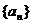 满足
满足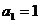 ,
,
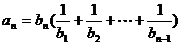
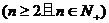 .
.
(1)求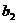 ,
,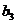 ,
,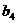 及
及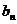 ;
;
(2)证明: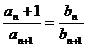
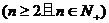 ;
;
(3)求证: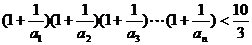 .
.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com