
6. 设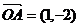 ,
,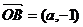 ,
,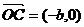 ,
,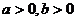 ,
,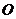 为坐标原点,若
为坐标原点,若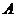 、
、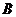 、
、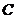 三点共线,则
三点共线,则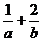 的最小值是( )
的最小值是( )
A. 2 B. 4 C. 6 D. 8
5. “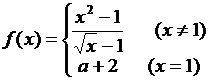 是定义在
是定义在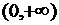 上的连续函数”是“直线
上的连续函数”是“直线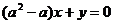 和直线
和直线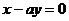 互相垂直”的( )
互相垂直”的( )
A.充分不必要条件 B.必要不充分条件 C.充要条件 D.既不充分也不必要条件
4.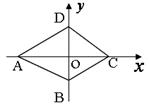 如图,已知四边形
如图,已知四边形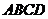 在映射
在映射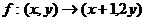 作用下的象集为四边形
作用下的象集为四边形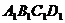 ,若四边形
,若四边形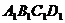 的面积是12,则四边形
的面积是12,则四边形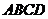 的面积是( )
的面积是( )
A. 9
B.6 C.
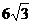 D.12
D.12
3.做了一次关于“手机垃圾短信”的调查,在A、B、C、D四个单位回收的问卷数依次成等差数列,再从回收的问卷中按单位分层抽取容量为100的样本,若在B单位抽取20份问卷,则在D单位抽取的问卷份数是( )
A.30份 B.35份 C. 40份 D.65份
2.若复数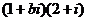 是纯虚数(
是纯虚数(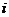 是虚数单位,
是虚数单位,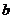 是实数),则
是实数),则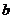 等于( )
等于( )
A.3 B.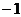 C.
C.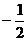 D.2
D.2
1.已知集合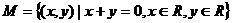 ,
,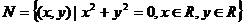 ,
,
则有( )
A.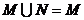 B.
B.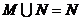 C.
C.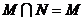 D.
D.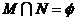
29.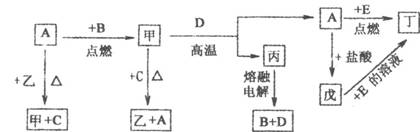 (11分)A、B、C、D、E是中学化学中常见的几种单质,其中A、D是金属,B、C、E常温下是气体;甲、乙、丙、丁、戊为化合物,其中乙在常温下是无色无味液体。它们之间有如下图所示的转化关系(有些产物已经略去):
(11分)A、B、C、D、E是中学化学中常见的几种单质,其中A、D是金属,B、C、E常温下是气体;甲、乙、丙、丁、戊为化合物,其中乙在常温下是无色无味液体。它们之间有如下图所示的转化关系(有些产物已经略去):
(1)写出下列反应的化学方程式:甲 + D_______________________________________。
(2)D与烧碱溶液反应的离子方程式是_________________________________________。
(3)戊→丁的离子方程式是___________________________________________________。
(4)设计一种检验丁溶液中金属离子的方法_________________________________________
______________(答出所加试剂及现象即可)。
(5)等物质的量的A、D与足量盐酸反应在相同条件下产生气体的物质的量之比是_______。
28.(17分)A为只含有C、H、O三种元素的芳香烃衍生物,各物质间的转化关系如下图。
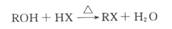 已知:
E为高分子化合物,分子式为(C9H8O2)n;H的分子
已知:
E为高分子化合物,分子式为(C9H8O2)n;H的分子
式为C18H16O6;I中除含有一个苯环外还含有一个六元环。
(1)写出A、E、I的结构简式:A______________;E_____________;I______________。
(2)写出F→G的化学方程式:___________________________________________________。
(3)B→C的反应条件为____________________;A + G→H的反应类型为____________。
(4)有机物A的同分异构体只有两个对位取代基,既能与Fe3+发生显色反应,又能发生水解反应,但不能发生银镜反应。则此类A的同分异构体有4种。例如:
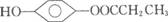
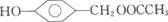
请写出另两种同分异构体______________________________________________________。
27.(18分)Ⅰ.实验室制备Cl2,即使在停止加热后,反应物还会继续反应一段时间。当在收集多瓶Cl2后,常有较多的Cl2逸到空气中去。为了避免Cl2的逸散,并对多余的Cl2随时取用,设计了下图所示的实验装置。
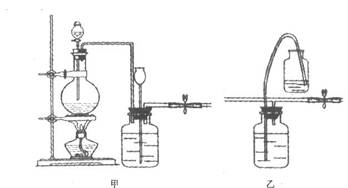
(1)设计甲装置的目的是__________________________________________________。甲装置
_________(填“能”或“不能”)用乙装置代替。
(2)装置乙中盛放的液体是______________________,该装置可看作是一个__________(填某仪器名称)。
Ⅱ.在氮的化合物中,有一类盐叫亚硝酸盐,如亚硝酸钠(NaNO2)等。亚硝酸钠是一种潜在的致癌物质,过量或长期使用会对人产生危害。由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生过被误当食盐使用的事件。已知:HNO2是一种弱酸,不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2;AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白中含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是__________。
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
(2)下列说法中,能用来鉴别NaNO2和NaCl的是____________。
A.测定这两种溶液的pH B.用AgNO3和HNO3两种试剂来鉴别
C.在酸性条件下加入KI淀粉试液来鉴别
(3)把新制氯气通入到NaNO2溶液中,氯水褪色,生成NaNO3和HCl,请写出此反应的离子方程式___________________________________________________。
(4)为了测定某样品中NaNO2的含量,可以使用标准KMnO4溶液进行滴定,试回答:KMnO4在滴定过程中作_____________(填“氧化剂”或“还原剂”),该滴定过程_________(填“要”或“不要”)另加指示剂。
(5)已知HNO2的酸性比醋酸略弱,某同学在家中进行鉴别NaNO2和NaCl的实验,但他家中只有浓醋酸,请问该实验能否成功?________(填“能”或“不能”),请说明理由_____
_____________________________________________________________________________。
(以化学方程式形式来表示)。
26.(14分)有短周期元素A、B、C,原子序数依次增大。A、B、C三种元素原子最外层电子数之和比C的次外层电子数少2,它们的质子数之和不超过M电子层最多容纳的电子数。将它们分别与氧元素结合,均可生成两种氧化物,A的氧化物有D和E,D的含氧量比E高;B的氧化物有F和G,G有毒;C的氧化物有H和I,H能和E发生化合反应。
(1)I中含有的化学键类型为__________________________;D的名称为_______________。
(2)F过量在世界环境中能引起______________,F的结构式为________________。
(3)写出:F和I反应的化学方程式_______________________________________________;
过量的F与C的氧化物的水化物反应的离子方程式________________________________。
(4)与C在同一周期的某非金属元素R,位于m主族,则其形成的气态氢化物的化学式为_________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com