
6、设NA为阿伏加德罗常数的数值,下列说法正确的是
A.16gCH4中含有4NA个C-H键
B.1mol·L-1NaCl溶液含有NA个Na+
C.1mol Cu和足量稀硝酸反应产生 NA个NO分子
D.常温常压下,22.4L CO2中含有 NA个CO2分子
5、在一定温度下,在100mL某一元弱酸HA的溶液中,含有该弱酸的分子数为5.42×1020个,并测得该溶液的c(H+)=10-3mol/L。在该平衡体系中,这种一元弱酸的电离度约为: A.9%; B.10%; C.3%; D.0.1%;
4、16O和18O是氧元素的两种核素,下列说法正确的是
A.16O2与18O2互为同分异构体
B.16O与18O核外电子排布方式不同
C.16O与18O中子数相同
D.16O和18O是同一种元素的不同原子
3、下列方法能使电离平衡H2O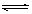 H+ + OH
H+ + OH -向右移动,且使溶液呈酸性的是
-向右移动,且使溶液呈酸性的是
A.向水中加入少量硫酸氢钠固体 B.向水中加入少量硫酸铝固体
C.向水中加入少量碳酸钠固体 D.将水加热到10 0℃,使水的pH=6
0℃,使水的pH=6
2、用酸滴定碱时,滴定前读酸式滴定管读数时,仰视读数,滴定结束时读数正确,这样会使测得的碱溶液的浓度
A. 偏高 B. 偏低 C. 不受影响 D. 不能确定
1、下列状态下,不能导电的电解质是
A.液态氯化氢 B.熔融食盐 C.稀硫酸 D.氯水
26.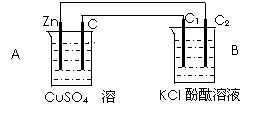 (14分)按下图装置进行实验,并回答下列问题
(14分)按下图装置进行实验,并回答下列问题
⑴判断装置的名称:A池为_______ B池为______
⑵锌极为______极,电极反应式为______________
铜极为______极,电极反应式为______________
石墨棒C1为_____极,电极反应式为__________
石墨棒C2为_____极,附近发生的实验现象为_____________
⑶当C2极析出224mL气体(标准状态)时,锌的质量变化(增加或减少)____、_____g,CuSO4溶液的质量变化了(增加或减少了)_____、____g
江苏省江都中学2009-2010学年第二学期期末考试
25. (10分)CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
⑴有效“减碳”的手段之一是节能。下列制氢方法最节能的是 。(填字母序号)
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O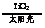 2H2↑+O2↑
2H2↑+O2↑
 D.天然气制氢:CH4+H2O
D.天然气制氢:CH4+H2O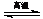 CO+3H2
CO+3H2
⑵CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 molCO2和3 mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
ΔH=-49.0 kJ/mol,测得CO2 和CH3OH(g)的浓度随时间变化如上图所示。
CH3OH(g)+H2O(g)
ΔH=-49.0 kJ/mol,测得CO2 和CH3OH(g)的浓度随时间变化如上图所示。
①从3 min到10 min,v(H2)= mol/(L·min)-1。
②能说明上述反应达到平衡状态的是 (选填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1︰1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
⑶新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为 (只要求写一种)。
 ⑷在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。某研究性学习小组探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 时,催化剂对汽车尾气的催化效果最好。(填a、b、c、d)
⑷在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。某研究性学习小组探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 时,催化剂对汽车尾气的催化效果最好。(填a、b、c、d)
24.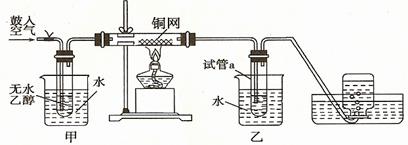 (10分)某实验小组用下列装置进行乙醇催化氧化的实验。
(10分)某实验小组用下列装置进行乙醇催化氧化的实验。
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式 。
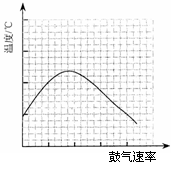 ⑵在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进
⑵在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进
行,说明该乙醇催化反应是 反应。进一步研究表明,
鼓入空气的速率与反应体系的温度关系曲线如图所示。
试解释出现图中现象的原因: 。
⑶甲和乙两个水浴作用不相同。甲的作用是 ;乙的作
用是 。
⑷若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。要除去该物质,可在混合液中加入 (填写字母)。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
然后,再通过 (填试验操作名称)即可除去。
23.(6分)以乙烯为原料合成化合物C的流程如下所示:
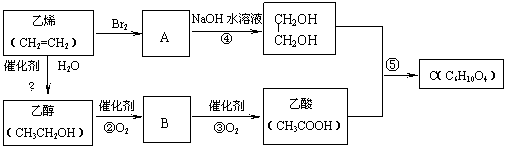
⑴反应①⑤的反应类型分别为 、 。
⑵写出反应③和⑤的化学方程式:③ ;⑤ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com