
34.I.恒温、恒压下,在一个可变容积的容器中发生如下发应:
[答案](1)样品重,砝码轻(2)防止空气中的CO2和水气进入U型管中(3)偏高
(4)把反应产生的CO2全部导入U型管中(5)判断反应产生的CO2是否全部排出,并被U型管中的碱石灰吸收(6)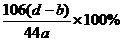 (7)答案略。
(05山东)
(7)答案略。
(05山东)
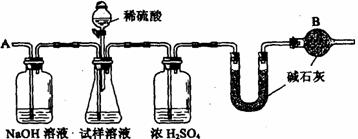
主要实验步骤如下:①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入6mol?L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为dg
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果 (填高、偏低或不变)
(4)步骤⑤的目的是
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验法。
33.已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。

上述方案是否合理? 。请简要说明理由:
① ;② 。
[答案](1) 2Na2O2+2SO2=2Na2SO3+O2
(2) 取白色固体,加稀硫酸,产生能使品红溶液褪色的气体。
(3) 不合理;稀硝酸能将亚硫酸钡氧化为硫酸钡;如果反应后的固体中还残留Na2O2,它能溶于水后能将亚硫酸根氧化成硫酸根 (04江苏化学)
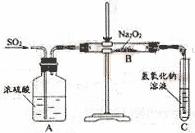 32.有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。请回答下列问题:
32.有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。请回答下列问题:
(1) 第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是: 。
(2) 请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3。 。
(3) 第2小组同学认为Na2O2与SO2反应生成了Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:
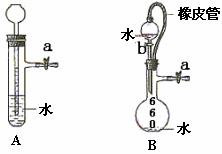 31.根据下图及描述,回答下列问题:
31.根据下图及描述,回答下列问题:
(1)关闭图A装置中的止水夹a后,从长颈漏斗向试管口注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) 。
判断理由: 。
(2)关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) ,判断理由:
[答案](1) 不漏气;由于不漏气,加水后试管内气体体积减小,导致压强增大,长颈漏斗内的水面高出试管内的水面。
(2)无法确定;由于分液漏斗和烧瓶间有橡皮管相连,使分液漏斗中液面上方和烧瓶中液面上方的压强相同,无论装置是否漏气,都不影响分液漏斗中的液体滴入烧瓶。 (04内蒙海南)
30.(1)无水乙酸又称冰醋酸(熔点
(2)要配制浓度约为2 mol?L-1 NaOH溶液100mL,下面的操作正确的是 (填代号)。
A. 称取
B. 称取
C. 称取
D. 用100 mL量筒量取40 mL 5 mol?L-1NaOH溶液,倒入250 mL烧杯中,再用同一量筒取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
[答案](1)略 (2)A、D
29.A、B、C、D是四种可溶的化合物,分别由阳离子K+、Ba2+、Al3+、Fe3+和阴离子OHˉ、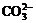 、
、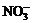 、
、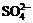 两两组合而成,它们的溶液发生如下反应:
两两组合而成,它们的溶液发生如下反应:
A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失。
C与D反应生成有色沉淀。
B与C反应生成白色沉淀。
写出它们的化学式:
A: B: C: D:
[答案] Ba(OH)2;Al2(SO4)3;K2CO3;Fe(NO3)3 (04广东化学)
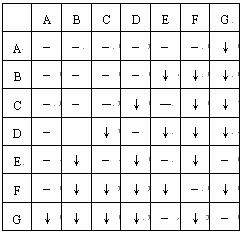 28.有A、B、C、D、E、F、G7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl3、Ca(NO3)2和Ba (OH )2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。试回答下面问题。
28.有A、B、C、D、E、F、G7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl3、Ca(NO3)2和Ba (OH )2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。试回答下面问题。
(
(2) 写出其余几种物质的化学式。B: ,
C: ,D: ,E: ,F: 。
[答案]⑴ KCl,AgNO3。混合时只生成一种沉淀的是KCl,生成的是AgCl,所以A是KCl,G是AgNO3。 ⑵ B:Na2SO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com