
5.接触法制硫酸生产过程中,假如进入接触室的原料气为100m3,反应后体积减少为92m3,已知原料气中SO2、O2、N2的体积比为20:15:65,则SO2的转化率为 ( )。
A.90% B.80% C.70% D.60%
4.在容积相等的甲乙两个密闭容器中,分别都充入2mol SO2和1mol O2,使它们在相同温度下发生反应2SO2(g)+O2(g) 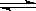 2SO3(g)。设在反应过程中,甲容器保持体积不变,乙容器保持压强不变,达到平衡后,如甲容器中SO2的转化率为25%,则乙容器中SO2的转化率应当是
( )。
2SO3(g)。设在反应过程中,甲容器保持体积不变,乙容器保持压强不变,达到平衡后,如甲容器中SO2的转化率为25%,则乙容器中SO2的转化率应当是
( )。
A.25% B.< 25% C.>25% D.无法判断
3.对于可逆反应2SO2(g)+O2(g) 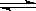 2SO3(g)
,ΔH=
-98.3kJ/mol。下列说法中正确的是
( )。
2SO3(g)
,ΔH=
-98.3kJ/mol。下列说法中正确的是
( )。
A.达到平衡时,反应物和生成物的浓度一定相等
B.达到平衡时,反应物和生成物的物质的量保持不变
C.加入催化剂,可以提高SO2的转化率
D.升高温度,可以提高SO2的转化率
2.大气污染是环境污染的一个重要方面,常见的大气污染分一次污染物和二次污染物。二次污染物在物理、化学因素或生物作用下发生变化,或与环境中的其它物质发生反应,生成新的污染物。如2NO + O2=2NO2,则NO2就是二次污染物,由NO2导致的污染就是NO的二次污染。下列物质①SO2 ②NO ③NO2 ④HCl ⑤CO2不易导致二次污染的是
( )。
A.①②③④⑤ B.①③⑤ C.④⑤ D.只有④
1.“绿色化学”(Green Chemistry)的目标是研究和寻找能充分利用的无毒害原料,最大限度地节约能源,在化工生产各个环节都实现净化和无污染的反应途径。下列各项属于“绿色化学”的是 ( )
A.处理废弃物 B.治理污染点 C.减少有毒物质 D.杜绝污染源
2.汽车尾气(含有烃类、CO、SO2、NO等物质)是空气主要污染源。治理的方法之一是在汽车的排气管上装一个“催化转化器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1) 写出CO与NO反应的化学方程式
(2) “催化转化器”的缺点是在一定程度上提高空气的酸度,其原因是
(3)控制城市空气污染的方法可以有( )
A.开发新能源 B.使用电动车 C.植树造林 D.戴上呼吸面具
思维方法: 。
展望高考:
【巩固练习】
课堂反馈
1.我国城市环境污染中的大气污染主要是( )
A.N2 Cl2 CO2 酸雨 B.SO2 NO2 CO 烟尘
C.NH3 CO2 NO 雾 D.HCl SO2 N2 粉尘
思维方法: 。
展望高考:
 [例2]某工厂处理含二氧化硫废气时采用“将二氧化硫转化为硫酸铵”的方法。该厂初步处理后的废气中氧气的体积分数为10%,二氧化硫的体积分数为0.2%。使该废气在400℃时以5m3/h的速率通过催化剂层与速率为20L/h的氨气混合,再喷水使之发生反应,2NH3+H2SO4
[例2]某工厂处理含二氧化硫废气时采用“将二氧化硫转化为硫酸铵”的方法。该厂初步处理后的废气中氧气的体积分数为10%,二氧化硫的体积分数为0.2%。使该废气在400℃时以5m3/h的速率通过催化剂层与速率为20L/h的氨气混合,再喷水使之发生反应,2NH3+H2SO4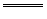 NH4)2SO4将得到的溶液在结晶装置中处理,可得到硫酸铵晶体。将气体都折合为标准状况下进行计算:
NH4)2SO4将得到的溶液在结晶装置中处理,可得到硫酸铵晶体。将气体都折合为标准状况下进行计算:
(1) 该工厂为什么将废气以5m3/h的速率与速率为20L/h的氨气混合为最佳配比(用计算说明 )?
(2) (2)若该厂每天排放10000m3这种废气,按上述方法该厂每月(30天)计算可得到硫酸铵多少 吨?消耗氨气多少m3??
解题思路: 。
易错点: 。
【考题再现】
5. 水污染:
(1) 成因:
(2) 危害:
(3) 治理:
【例题解析】
[例1]关于酸雨的下列分析正确的是( )
A.因空气中无催化剂,SO2不能转化成SO3,酸雨中只含H2SO3
B.SO2在空气中有条件形成SO3,所以酸雨中含H2SO4
C.酸雨是无法避免的
D.H2SO4形成的酸雨比H2SO3危害大
解题思路: 。
易错点: 。
4. 酸雨:
(1) 酸雨的概念:
(2) 酸雨的危害:
(3) 控制酸雨的措施:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com