
②N2(g)+3H2(g)
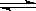 2NH3(g), ΔH < 0;
2NH3(g), ΔH < 0;
①A(s)+B(g) 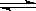 C(g), ΔH < 0;
C(g), ΔH < 0;
3.以下可逆反应中,达到平衡后,通过升高温度可提高反应物转化率的是 ;通过增大压强可提高反应物转化率的是 ;改变压强,转化率不变的是 。
2.冶金工业上为降低硫的氧化物对空气的污染,常用CO在500℃、铝矾土催化下还原SO2,处理烟道废弃回收硫,写出该反应的化学方程式 。
1.硫酸工业常用 收SO3,是为了避免 ;在生产过程中为了提高原料的利用率,常用 、 。
9.酸雨形成的主要原因是 ( )
A.汽车排出大量尾气 B.自然界中硫化物分解
C.工业上大量燃烧含硫燃料 D.制硫酸厂排出大量尾气
课外作业
8.下列关于接触法制硫酸的叙述中,不正确的是 ( )
A. 黄铁矿粒在沸腾炉中燃烧快,反应完全,提高了原料的利用率
B. 炉气净化的目的是防止催化剂中毒
C. 热交换器的目的是利用反应放热,预热SO2和O2,冷却反应生成的SO2
D. 吸收塔用水吸收SO3,因为SO3在水中溶解度大,吸收完全
7.治理“三废”保护环境的最主要的方法是 ( )
A.减少污染严重的工厂 B.把三废埋入深洞
C.提高人们的认识 D.变废为宝,综合利用
 A. mol B. mol C. mol D. mol
A. mol B. mol C. mol D. mol
6.在一定条件下,某密闭容器发生如下反应:2SO2(g)+O2(g) 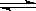 2SO3(g)
, H=
-98.3kJ/mol,反应达到平衡后SO2、O2、SO3的物质的量之比为3:2:5,保持其它条件不变,升温后重新达到平衡,SO3、O2的物质的量分别为2α mol和α mol,则此时容器内SO2的物质的量应为
( )。
2SO3(g)
, H=
-98.3kJ/mol,反应达到平衡后SO2、O2、SO3的物质的量之比为3:2:5,保持其它条件不变,升温后重新达到平衡,SO3、O2的物质的量分别为2α mol和α mol,则此时容器内SO2的物质的量应为
( )。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com