
2、氧化铝的两性:
Al2O3+6HCl=2AlCl3+3H2O Al2O3+2NaOH=2NaAlO2+H2O
1、Al既可与酸反应,又可与碱反应 铝是一种金属元素,但由于氢氧化铝的两性,使铝单质既能和酸反应生成铝盐,又能和碱反应生成偏铝酸盐。 (1) Al与酸反应:2Al+6H+=2Al3++3H2↑ (2) Al与碱反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 反应过程:2Al+6H2O=2Al(OH)3+3H2↑(用NaOH去膜后的Al发生此反应) Al(OH)3+NaOH=NaAlO2+2H2O,二式加和得总反应式。
3、氢氧化铝
(1)制取
(2)Al(OH)3的两性
(3)Al(OH)3不稳定:
[投影]答案:]一、铝及重要化合物之间的转化关系
2、氧化铝的两性:
1、Al既可与酸反应,又可与碱反应 铝是一种金属元素,但由于氢氧化铝的两性,使铝单质既能和酸反应生成铝盐,又能和碱反应生成偏铝酸盐。 (1) Al与酸反应:
(2) Al与碱反应:
反应过程:
7、现有一定量含有Na2O杂质的Na2O2试样.请从下图中选用适当 应物只有CaCO3固体,
6摩尔/升,盐酸和蒸馏水).
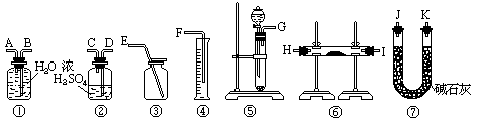
请填写下列空白: (1)写出实验中Na2O2和Na2O分别发生反应的化学方程式______________。 (2)应选用的装置是(只要求写出图中装置的标号)______________________。 (3)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略)_________。 8、取一定量的Na2CO3、NaHCO3和Na2SO4混合物与250mL 1.00mol·L-1过量盐酸反应,生成2.016L CO2(标准状况),然后加入500mL 0.100mol·L-1Ba(OH)2溶液,得到沉淀的质量为2.33g,溶液中过量的碱用10.0mL 1.00ml·L-1盐酸恰好完全中和。计算混合物中各物质的质量。 参考答案:1、D 2、A 3、D 4、A 5、A 6、BC 7、
(1) 2Na2O2+2H2O=4NaOH+O2↑ Na2O+H2O=2NaO
(2) ⑤①④
(3) (G)接(A)(B)接(F)
方法2
(1) 2Na2O2+2CO2=2Na2CO3+O2 Na2O+CO2=Na2CO3
(2) ⑤②⑥⑦①④
(3) (G)接 (D)(C) 接 (H)(I)[或(I)(H)] 接(J)(K) (或(K)(J)) 接(A)(B) 接(F)
8、混合物中Na2SO4的质量=
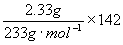 g·mol-1=1.42g
设混合物中Na2CO3和NaHCO3的物质的量分别为x和y,
反应中放出的CO2物质的量=
g·mol-1=1.42g
设混合物中Na2CO3和NaHCO3的物质的量分别为x和y,
反应中放出的CO2物质的量= 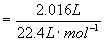 =0.0900mol
与Na2CO3、NaHCO3反应的盐酸的物质的量为:
0.250L×1.00mol·L-1-0.500L×0.100mol·L-1×2+0.0100L×1.00 mol·L-1=0.160mol
=0.0900mol
与Na2CO3、NaHCO3反应的盐酸的物质的量为:
0.250L×1.00mol·L-1-0.500L×0.100mol·L-1×2+0.0100L×1.00 mol·L-1=0.160mol
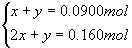
[归纳整理]写出相应化学方程式或离子方程式:
6、关于Na2CO3和NaHCO3性质的有关叙述正确的是
A.在水中溶解性:Na2CO3<NaHCO3
B.热稳定性:Na2CO3>NaHCO3
C.与酸反应的速度:Na2CO3<NaHCO3
D.Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3
5、除去小苏打溶液中少量苏打的方法是
A.加热 B.加NaOH C.通CO2气体 D.加盐酸
4、用于呼吸用具上和潜水艇中作为氧气的来源的物质是
A.Na2O2 B.NaHCO3 C.SO3(固) D.KMnO4
3、下列叙述中正确的是
A.Na2O与Na2O2都能与水反应生成碱,它们都是碱性氧化物
B.Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2
C.Na2O有氧化性,Na2O2只有还原性
D.Na2O能继续被氧化成Na2O2,Na2O2比Na2O稳定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com