
7ΓΔΙΏ–‘÷ΤΒΦœΒΆ≥“―ΙψΖΚ”Ο”ΎΒ·Βά ΫΒΦΒ·ΙΛ≥Χ÷–Θ§’βΗωœΒΆ≥ΒΡ÷Ί“Σ‘ΣΦΰ÷°“Μ «Φ”ΥΌΕ»ΦΤΘ§Φ”ΥΌΕ»ΦΤΒΡΙΙ‘λ‘≠άμ Ψ“βΆΦ»γΆΦΥυ ΨΘ§―ΊΒΦΒ·≥ΛΕ»ΖΫœρΑ≤ΉΑΒΡΙΧΕ®ΙβΜ§ΗΥ…œΧΉ“Μ÷ ΝΩΈΣmΒΡΜ§ΩιΘ§Μ§ΩιΝΫ≤ύΖ÷±π”κΨΔΕ»œΒ ΐΈΣkΒΡΒ·Μ…œύΝ§Θ§ΝΫΒ·Μ…¥Π”ΎΉ‘»Μ≥ΛΕ»Θ§Μ§Ωι…œ”–÷Η’κΘ§Ω…Ά®Ιΐ±ξ≥Ώ≤β≥ωΜ§ΩιΒΡΈΜ“ΤΘ§»ΜΚσΆ®ΙΐΩΊ÷ΤœΒΆ≥Ϋχ––÷ΤΒΦΘ§…ηΡ≥ΕΈ ±ΦδΡΎΒΦΒ·―ΊΥ°ΤΫΖΫœρ‘ΥΕ·Θ§÷Η’κœρΉσΤΪάκOΒψΒΡΨύάκΈΣSΘ§‘ρ’βΕΈ ±ΦδΡΎΒΦΒ·ΒΡΦ”ΥΌΕ»Γ≠Γ≠Γ≠Γ≠(ΓΓ)
 A. ΖΫœρœρΉσΘ§¥σ–ΓΈΣ
A. ΖΫœρœρΉσΘ§¥σ–ΓΈΣ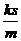
B. ΖΫœρœρ”“Θ§¥σ–ΓΈΣ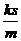
C. ΖΫœρœρΉσΘ§¥σ–ΓΈΣ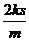
D. ΖΫœρœρ”“Θ§¥σ–ΓΈΣ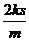
6ΓΔ÷ ΝΩΈΣm1ΚΆm2ΒΡΝΫΗωΈοΧεΘ§”…Ψ≤÷ΙΩΣ Φ¥”Ά§“ΜΗΏΕ»œ¬¬δΘ§‘ΥΕ·÷–Υυ ήΉηΝΠΖ÷±πΈΣf1ΚΆf2Θ§»γΙϊΈοΧεm1œ»¬δ‘ΎΒΊΟφΘ§Ρ« «“ρΈΣΓ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠(ΓΓ)
A. m1 >m2ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ B. f1 <f2
C. 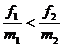 ΓΓΓΓΓΓD.
ΓΓΓΓΓΓD.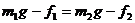
5ΓΔ»γΆΦΘ§÷ ΝΩΈΣmΒΡΈοΧεAΖ≈÷Ο‘Ύ÷ ΝΩΈΣMΒΡΈοΧεB…œΘ§B”κΒ·Μ…œύΝ§Θ§ΥϋΟ«“ΜΤπ‘ΎΥ°ΤΫΟφ…œΉωΦρ–≥’ώΕ·Θ§’ώΕ·Ιΐ≥Χ÷–AΓΔB÷°ΦδΈόœύΕ‘‘ΥΕ·Θ§…ηΒ·Μ…ΒΡΨΔΕ»œΒ ΐΈΣkΘ§Β±ΈοΧεάκΩΣΤΫΚβΈΜ÷ΟΒΡΈΜ“ΤΈΣx ±Θ§AΓΔBΦδΒΡΡΠ≤ΝΝΠΒΡ¥σ–ΓΒ»”ΎΓ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠(ΓΓ)
A. 0ΓΓ
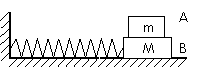 B. kx
B. kx
C. 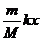
D.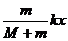
4ΓΔ»γΆΦΥυ ΨΘ§”–“ΜΝΨΤϊ≥Β¬ζ‘ΊΈςΙœ‘ΎΥ°ΤΫ¬ΖΟφ…œ‘»ΥΌ«ΑΫχΘ§ΆΜ»ΜΖΔœ÷“βΆβ«ιΩωΘ§ΫτΦ±…≤≥ΒΉω‘»ΦθΥΌ‘ΥΕ·Θ§Φ”ΥΌΕ»¥σ–ΓΈΣaΘ§…η÷–Φδ“Μ÷ ΝΩΈΣmΒΡΈςΙœAΘ§‘ρA ήΤδΥϋΈςΙœΕ‘ΥϋΒΡΉς”ΟΝΠΒΡ¥σ–Γ «Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠(ΓΓ)
A. m(g+a)ΓΓΓΓ
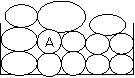 B. maΓΓΓΓ
B. maΓΓΓΓ
C. 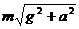 ΓΓΓΓ
ΓΓΓΓ
D.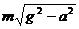
3ΓΔ“ΜΟϊ―ß…ζΈΣΝΥΧε―ι≥§÷ΊΚΆ ß÷ΊΒΡΗ–ΨθΘ§¥”“Μ¬Ξ≥ΥΒγΧίΒΫ °Έε¬ΞΘ§”÷¥” °Έε¬Ξœ¬ΒΫ“Μ¬ΞΘ§ΥϊΒΡΗ–Ψθ «Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠(ΓΓ)
A. …œ¬Ξ ±œ»≥§÷ΊΘ§»ΜΚσ’ΐ≥Θ
B. …œ¬Ξ ±œ» ß÷ΊΘ§»ΜΚσ’ΐ≥ΘΘ§ΉνΚσ≥§÷Ί
C. œ¬¬Ξ ±œ» ß÷ΊΘ§»ΜΚσ’ΐ≥Θ
D. œ¬¬Ξ ±œ» ß÷ΊΘ§»ΜΚσ’ΐ≥ΘΘ§ΉνΚσ≥§÷Ί
2ΓΔ»γΆΦΥυ ΨΘ§ΝΫΗω÷ΊΒΰ‘Ύ“ΜΤπΒΡΜ§ΩιΘ§÷Ο”ΎΙΧΕ®ΒΡ«ψΫ«ΈΣΠ»ΒΡ–±Οφ…œΘ§Μ§ΩιAΚΆΜ§ΩιBΒΡ÷ ΝΩΖ÷±πΈΣmΚΆMΘ§AΚΆBΦδΡΠ≤ΝœΒ ΐΈΣΠΧ1Θ§B”κ–±ΟφΦδΒΡΡΠ≤ΝœΒ ΐΈΣΠΧ2Θ§ΝΫΜ§ΩιΕΦ¥”Ψ≤÷ΙΩΣ ΦΘ§“‘œύΆ§ΒΡΦ”ΥΌΕ»―Ί–±Οφœ¬Μ§Θ§‘Ύ’βΗωΙΐ≥Χ÷–A ήΒΡΡΠ≤ΝΝΠΓ≠Γ≠Γ≠Γ≠(ΓΓ)
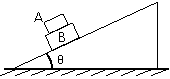 A. Β»”ΎΝψ
A. Β»”ΎΝψ
B. ΖΫœρ―Ί–±Οφœρœ¬
C.¥σ–ΓΒ»”ΎΠΧ2mgcosΠ»
D.¥σ–ΓΒ»”ΎΠΧ1mgcosΠ»
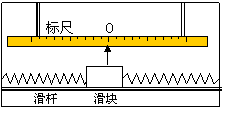
1ΓΔ»γΆΦΥυ ΨΘ§…ΐΫΒΜζΡΎΒΡΥ°ΤΫΉάΟφ…œΘ§”Ο«αΒ·Μ…Ν§Ϋ”“ΜΗω÷ ΝΩΈΣmΒΡΈοΧεΘ§Β±…ΐΫΒΜζ“‘ΥΌΕ»Vœρœ¬Ήω‘»ΥΌ‘ΥΕ·Θ§Α―Β·Μ…ά≠≥ΛX ±Θ§ΈοΧε«ΓΚΟΡή‘ΎΉάΟφ…œΨ≤÷ΙΘ§»τΆΜ»ΜΖΔœ÷ΈοΧεœρ”“‘ΥΕ·Θ§‘ρ…ΐΫΒΜζΒΡ‘ΥΕ·Ω…Ρή «Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠Γ≠(ΓΓ)
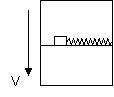 A. ±Θ≥÷‘≠ά¥‘»ΥΌ‘ΥΕ·
A. ±Θ≥÷‘≠ά¥‘»ΥΌ‘ΥΕ·
B. œρœ¬ΉωΦ”ΥΌ‘ΥΕ·
C. œρ…œΉωΦ”ΥΌ‘ΥΕ·
D.“―ΆΘ÷Ι≤ΜΕ·
«Ω»θΒγΫβ÷ ΒΡΒγάκΚΆ»ή“ΚΒΡΥαΦν–‘ «άζΡξΗΏΩΦΒΡ»»ΒψΡΎ»ίΘ§÷ς“Σ”–ΘΚΔΌ±»ΫœΡ≥–©Έο÷ ΒΦΒγ–‘ΒΡ«Ω»θΘΜΔΎ«Ω»θΒγΫβ÷ ΒΡ≈–Εœ”κ±»ΫœΘΜΔέΆβΫγΧθΦΰΕ‘»θΒγΫβ÷ ΒγάκΤΫΚβΒΡ”ΑœλΦΑΒγάκΤΫΚβάμ¬έΒΡ”Π”ΟΘΜΔή»ή“ΚΥαΦν–‘(ΜρpH¥σ–Γ)ΒΡ≈–ΕœΘΜΔί”–ΙΊ»ή“ΚpHΒΡΦΤΥψΓΘ≥ΘΦϊΒΡΧβ–Ά÷ς“Σ «―Γ‘ώΧβΘ§ΒΪ“≤”–“Μ≤ΩΖ÷± ¥πΧβΘ§’β“≤Χεœ÷ΝΥΗΏΩΦΟϋΧβΒΡ“Μ÷÷«ςœρΘΚ”…÷Σ Ε–ΆœρΡήΝΠ–ΆΒΡΉΣ±δΘ§Ά§ ±“ΣΉΔ“β”κΤδΥϊ≤ΩΖ÷÷Σ ΕΒΡΝΣœΒΓΘΫβ¥π¥ΥάύΧβΡΩΒΡΙΊΦϋ «“Σ’ΐ»ΖάμΫβ”–ΙΊΒΡΗ≈ΡνΘ§Μαάϊ”ΟΜ·―ßΤΫΚβάμ¬έΖ÷Έω―–ΨΩ»θΒγΫβ÷ ΒΡΒγάκ«ιΩωΘΜ“άΨί”–ΙΊ»ή“ΚpHΦΤΥψΧβΡΩάύ–ΆΧΊΒψΘ§–Έ≥…’ΐ»ΖΒΡΫβΧβΖΫΖ®ΥΦ¬ΖΓΘ
¥”ΫϋΦΗΡξΒΡΗΏΩΦ ‘ΧβΖ÷Έωά¥Ω¥Θ§≥ωœ÷ΝΥ“‘Ή÷ΡΗ±μ Ψ»ή“ΚΒΡpHΘ§“―÷ΣΜλΚœ«ΑΚσ»ή“ΚΒΡΧεΜΐ«σΜλΚœΚσpHΘ§¥ΥάύΧβΗϋΦ”ΆΜ≥ωΝΥ‘Υ”Ο ΐ―ßΙΛΨΏά¥ΫβΨωΜ·―ßΈ ΧβΒΡΡήΝΠΘ§”Π“ΐΤπ÷Ί ”ΓΘ»ή“ΚΒΡpHΦΤΥψΧβ…ηΧθΦΰΩ…«ß±δΆρΜ·Θ§’ΐœρΓΔΡφœρΥΦΈ§ΓΔ ΐΉ÷”κΉ÷ΡΗΫΜΧφ≥ωœ÷Θ§”κ…ζΈοΥαΦνΤΫΚβœύΫαΚœΜρ‘Υ”Ο ΐ―ßΙΛΨΏΫχ––ΆΤάμΒ» ‘Χβ‘ΎΓΑ3+XΓ±ΉέΚœ≤β ‘÷–≥ωœ÷Ω…Ρή–‘ΦΪ¥σΘ§’ΙΆϊΫώΚσΜα“‘ΧνΩ’Μρ―Γ‘ώΒΡ–Έ Ϋ≥ωœ÷Θ§ΧβΡΩΡ―Ε» ÷–Θ§ΆΤάμ–‘Μα”–Υυ‘ω«ΩΓΘ
Θέάΐ1Θί Β―ι±μΟςΘ§“ΚΧ§ ±Θ§¥ΩΝρΥαΒΡΒΦΒγ–‘«Ω”Ύ¥ΩΥ°ΓΘ“―÷Σ“ΚΧ§ΒγΫβ÷ ΕΦΡήœώΥ°Ρ«―υΉ‘…μΒγάκΕχΫ®ΝΔΒγάκΤΫΚβ(Φ¥œώH2O+H2O===H3O++OHΘ≠Ρ«―υ)Θ§«“‘Ύ“ΜΕ®Έ¬Ε»œ¬ΕΦ”–ΗςΉ‘ΒΡάκΉ”Μΐ≥Θ ΐΓΘΈ ‘Ύ25Γφ ±Θ§¥ΩΝρΥαΒΡάκΉ”Μΐ≥Θ ΐKΚΆΥ°ΒΡάκΉ”Μΐ≥Θ ΐKWΙΊœΒΈΣ
A.KΘΨKWΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ B.K=KW
C.KΘΦKWΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ D.ΈόΖ®±»Ϋœ
ΫβΈωΘΚΫΪ¥ΩΝρΥαάύ±»”ΎΥ°’“≥ω¥ΩΝρΥαΒΡΒγάκΤΫΚβ «Ϋβ¥ΥΧβΒΡΙΊΦϋΓΘ
άύ±»”ΎΥ°Θ§¥ΩΝρΥαΒΡΒγάκΤΫΚβΩ…Ε®ΈΣΘΚH2SO4+H2SO4 H3SO
H3SO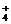 +HSO
+HSO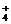
‘ρΤδάκΉ”Μΐ≥Θ ΐKW=c(H3SO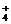 )ΓΛc(HSO
)ΓΛc(HSO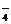 )ΓΘΗυΨίΧβ“βΘ§¥ΩΝρΥαΒΡΒΦΒγ–‘«Ω”ΎΥ°Θ§‘ρΩ…¥÷¬‘ΒΊ»œΈΣΝρΥα÷–άκΉ”≈®Ε»¥σ”Ύ¥ΩΥ°÷–άκΉ”ΒΡ≈®Ε»Θ§Φ¥KΘΨKWΓΘ
)ΓΘΗυΨίΧβ“βΘ§¥ΩΝρΥαΒΡΒΦΒγ–‘«Ω”ΎΥ°Θ§‘ρΩ…¥÷¬‘ΒΊ»œΈΣΝρΥα÷–άκΉ”≈®Ε»¥σ”Ύ¥ΩΥ°÷–άκΉ”ΒΡ≈®Ε»Θ§Φ¥KΘΨKWΓΘ
¥πΑΗΘΚA
Θέάΐ2Θί(2002Ρξ»ΪΙζάμΉέΘ§9)‘Ύ»Υ‘χΫ®“ι”ΟAG±μ Ψ»ή“ΚΒΡΥαΕ»(acidity grade)Θ§AGΒΡΕ®“εΈΣAG=lgΘέc(H+)/c(OHΘ≠)ΘίΓΘœ¬Ν–±μ ω’ΐ»ΖΒΡ «
A.‘Ύ25Γφ ±Θ§»τ»ή“Κ≥ ÷––‘Θ§‘ρpH=7,AG=1
B.‘Ύ25Γφ ±Θ§»τ»ή“Κ≥ Υα–‘Θ§‘ρpHΘΦ7,AGΘΦ0
C.‘Ύ25Γφ ±Θ§»τ»ή“Κ≥ Φν–‘Θ§‘ρpHΘΨ7Θ§AGΘΨ0
D.‘Ύ25Γφ ±Θ§»ή“ΚΒΡpH”κAGΒΡΜΜΥψΙΪ ΫΈΣAG=2(7Θ≠pH)
ΫβΈωΘΚ±ΨΧβΩΦ≤ιΝΥΕ‘»ή“ΚΥαΦν–‘ΒΡ»œ ΕΘ§Ε‘pHΓΔAGΕ®“εΒΡάμΫβΚΆΙΊœΒ ΫΒΡΆΤΒΦΓΘΡήΖ¥”≥―ß…ζΕ‘ ΐ‘ΥΥψΒΡ ΐ―ßΜυ¥ΓΓΘ–¬Ψ…÷Σ ΕΒΡ»ΎΚœΓΔΦλ≤β―ß…ζ”Π±δΡήΝΠ «ΗΏΩΦΟϋΧβΒΡΖΔ’Ι«ς Τ÷°“ΜΓΘ
ΗυΨί»ή“Κ÷–ΘέH+Θί”κΘέOHΘ≠ΘίΒΡœύΕ‘¥σ–ΓΘ§ά¥ΨωΕ®»ή“ΚΒΡΥαΦν–‘ΓΘ”÷¥”pHΚΆAGΒΡΕ®“ε―Α’“ΝΫ’ΏΒΡΙΊœΒ ΫΓΘ
A.AG=lg(ΘέH+ΘίΘ·ΘέOHΘ≠Θί)=lg1=0
B.≥ Υα–‘Θ§ΘέH+ΘίΘΨΘέOHΘ≠ΘίΘ§AGΘΨlg1=0
C.≥ Φν–‘Θ§ΘέH+ΘίΘΦΘέOHΘ≠ΘίΘ§AGΘΦlg1=0
D.25Γφ ±Θ§pH+pOH=pKW=14
AG=lgΘέH+ΘίΘ≠lgΘέOHΘ≠Θί=Θ≠pH+14Θ≠pH=14Θ≠2pH=2(7Θ≠pH)
¥πΑΗΘΚD
6.»ή“ΚpHΒΡΦΤΥψ
ΥαΑ¥ΥαΘ§ΦνΑ¥ΦνΘ§Ά§«ΩΜλΚœ‘Ύ÷°ΦδΓΘ
“λ«ΩΜλΚœΩ¥ΙΐΝΩΘ§ΈόœόœΓ Ά7ΈΣœόΓΘ
5.«ΩΥα(pH1)”κ«ΩΦν(pH2)ΜλΚœ≥ ÷––‘ ±Θ§Εΰ’ΏΧεΜΐ”κpHΒΡΙΊœΒΙφ¬…
(1)»τpH1+pH2ΘΫ14Θ§‘ρV(Υα)ΓΟV(Φν)ΘΫ1ΓΟ1
(2)»τpH1+pH2ΘΨ14Θ§‘ρV(Υα)ΓΟV(Φν)ΘΫ10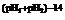 ΓΟ1
ΓΟ1
(3)»τpH1+pH2ΘΦ14Θ§‘ρV(Υα)ΓΟV(Φν)ΘΫ1ΓΟ10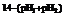
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com