
3、等价分子(EQ):寻找合成子的等价分子,是学习和掌握合成子法的第二个关键。下表给出常见合成子的等价分子。

2、合成子(Synthon):合成子是切断得到的分子碎片。根据共价键断裂的方式-均裂和异裂,合成子可以是自由基型,也可以是离子型。但由于切断是人为的操作,并非真实的过程,因此合成子并非真实存在实体,只是合成子方法的一种概念或操作手段而已。
均裂 异裂

但要注意:尽管合成子并非真实存在,但形成这个共价键的反应类型却由合成子所决定:自由基型合成子代表自由基反应,离子型合成子代表离子型反应(亲电反应或亲核反应)。由于离子型反应是常用的合成反应,所以合成子一般采用离子型。
合成子法是针对目的分子(TM)的合成进行原料和路线分析的一种可以具体操作的方法,它主要由切断、合成子、等价分子、官能团转换、官能团保护等具体步骤。
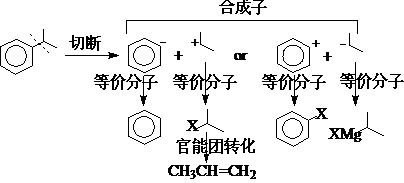
1、切断位置的选择:
原则上任何位置都可以切断,但为了获得最佳合成路线,需要对切断位置做出选择。切断位置的选择规律是合成子法最重要的内容。
切断位置选择的基本规律:
(1)双键优先切断-最后生成,避免保护;
(2)杂原子优先切断-变成两个TM;
(3)靠中央切断-获得最短的合成路线;
(4)利用对称性切断-简化原料种类;
(5)靠支链、侧链切断-获得形状简单的原料;
更细致的规律在单、双官能团化合物中介绍。
5、卤代烃-有机合成的“桥梁”
重要的合成方法都以卤代烃为原料或者中间体。熟悉各种卤代烃的制备,是有机合成的基础!
(1)一卤代烃的制备:
以烯烃为原料:

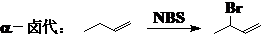
以ROH为原料:
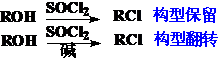
以酸为原料:

(2)二卤代烃:
同碳二卤代烃(偕二卤):
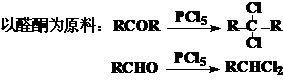
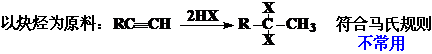
邻二卤代烃:以烯烃为原料:
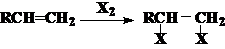
1,3-二卤代烃:
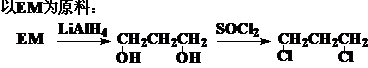
1,4-二卤代烃:
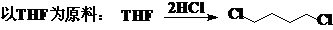
(3)卤乙烯型或芳香族卤代烃:只限于Grignard试剂
以烯烃为原料:
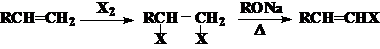
以芳烃为原料:直接卤代-符合定位规则
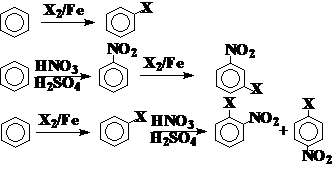
通过重氮盐-制备不符合定位规则的芳香族卤代烃
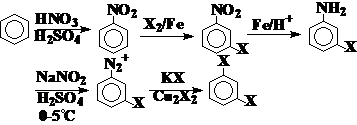
第二节、有机合成路线设计-合成子法
5、EM和EAA合成法-甲基酮和酸的合成
EM(丙二酸二乙酯)和EAA(乙酰乙酸乙酯)都属于Z-CH-Z’型含活泼亚甲基的化合物,具有共同的特点:
①在碱性条件下是优秀的亲核试剂,可以参与亲核取代和亲核合成反应:
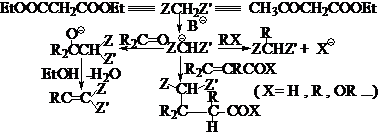
②EM和EAA型化合物水解之后,分别得到丙二酸和乙酰乙酸型化合物,这两类化合物具有共同的特征:对热不稳定,受热易分解脱羧,分别生成酸和甲基酮:
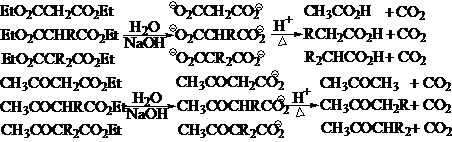
原料分析的基本模型:
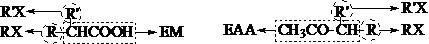
讨论:①试剂EtONa / EtOH(用其它的RONa和ROH可逆导致酯交换发生)。
②作为亲核取代,除卤代烃外,RX也可以是酰卤、a-氯代酸酯和a-氯代醛酮:
卤代烃:烯丙型 > CH3X > 伯RX > 仲RX
而氯乙烯、氯苯,叔RX,桥头RX等类型的卤代物及所有的RF都不能使用(为什么?)。
酰卤:可以在分子中引入酰基RCO-,从而生成二酮或酮酸;a-卤代酸酯可以再分子中引入羧甲基。
③作为亲核加成,EM和EAA可以与醛酮缩合,在分子中引入C=C,生成a,b-不饱和酸和a,b-不饱和醛酮:
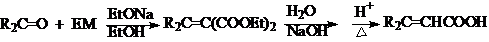
a,b-不饱和酸
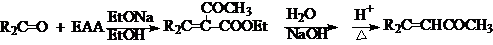
a,b-不饱和酮(醛)
④作为Micheal加成,EM和EAA可以与a,b-不饱和醛酮和酯在b-位缩合,生成二元酸、二元酮和酮酸等双官能团化合物:
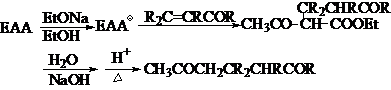
1,5-二酮
合成举例1、
原料分析: TM
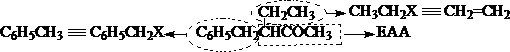
合成路线:

合成举例2、
原料分析: TM
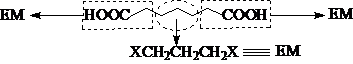
合成路线:
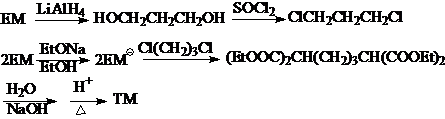
合成举例3、
原料分析:
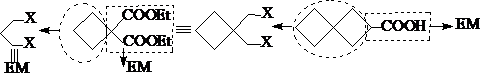
合成路线:

3、Grignard试剂-醇的合成
Grignard试剂(格氏试剂)是有机化学史上第一个金属有机试剂(V.Grignard获得1912年诺贝尔化学奖),主要用于合成各种个样的醇,也是典型的串联反应体系。如果考虑到:醇羟基可以转化为任何其它的官能团,那么Grignard试剂可以用于任何单官能团化合物的合成。如:
RCH2OH ® RCH2X ® RCHO® RCOOX; R2CHOH ® R2C=O
RCH2OH ® R’CH=CH2 ® RCH3
Grignard试剂的制备和性质
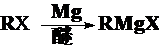
格氏试剂是优良的亲核试剂,可以参入亲核加成和亲核取代反应。
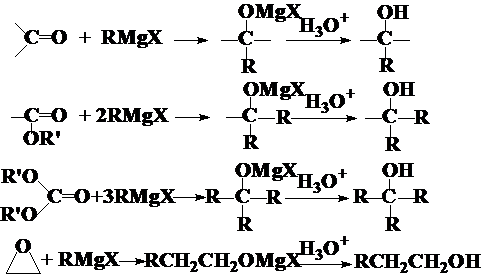
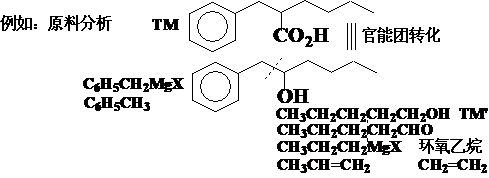
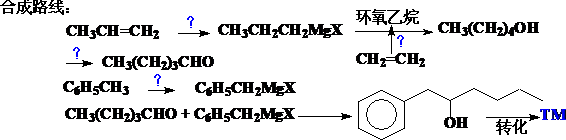
一般情况下,乙醚回流(33°C)的条件就可以满足反应的需要,对于不活泼的卤代烃(如卤乙烯型、卤苯型),则需要更高的反应温度,可以选用正丁醚或者四氢呋喃(THF,>80°C)。
制备Grignard试剂使用的溶剂,必须无水、无醇、无过氧化物,通常称为绝对乙醚,需要专门处理。
生成的Grignard试剂实际上是RMgX乙醚配合物的乙醚溶液,分子的存在形式还不十分确
2、Williammson反应-醚的合成
醚的合成有两种方法:
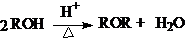
但这种方法只适用于低级单醚(R=R≤C6),既不适用于高级单醚-收率低,也不适用于混醚-生成混合物。而Williammson反应没有此类限制:
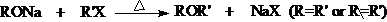
这实际上是典型的亲核取代反应,除了受到RX活性的制约之外,还必然受到消除反应的制约。一般认为:氯乙烯型(CH2=CHX和C6H5X类)和桥头类氯代烃由于活性太差,不能发生Williammson反应;而叔卤代烷在碱性(RONa是强碱)条件下,几乎完全发生消除反应,所以不能用于Williammson反应;其它卤代烷的选择也要考虑消除反应和取代活性的两种因素,对原料做出适当的选择。
选择R’X的顺序是: 苄基卤 > 烯丙型 > CH3X > 伯卤代烷 > 仲卤代烷
而叔卤代烷、CH2=CHX、C6H5X、桥头卤不能选作Williammson反应的原料。
合成举例1、
原料分析: TM
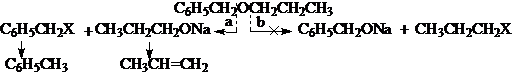
合成路线:
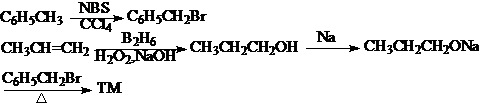
在有机化学中,有些反应对有机合成特别重要,应当给予足够的重视。
1、Wittig反应-烯烃的合成
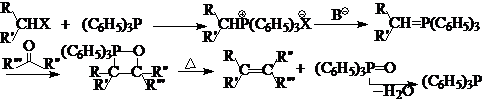
原料:含有a-H的卤代烷-烯丙型、伯、仲、a-卤代酸酯等;
醛酮-醛的活性大于酮。
试剂:三苯基膦(C6H5)3P反应后变成三苯基氧磷(C6H5)3P=O,催化加氢脱水以后又
变成三苯基瞵,可以反复使用并不消耗。目的产物烯烃由卤代烷和醛酮的碳链构成。
碱B-既可以用强碱(如RONa),也可以用弱碱(如R2NH)。
选择性:Wittig试剂只能与醛酮的C=O缩合(醛的活性大于酮),不能与羧酸及其衍生物中的C=O缩合;Wittig反应主要受热力学控制,因此生成的烯烃以反式为主。
串联反应及其特点:一条合成路线常常包括若干步反应,如果每步反应都不需要分离纯化,那么整个合成路线可以在同一个反应器中连续进。这种不需要分离纯化、可以在同一个反应器中连续进行的若干个反应的组合称为串联反应。
串联反应的优点非常突出:①省去每步反应分离纯化的消耗(时间、精力、试剂、溶剂、能量等),导致总收率和经济效益的大幅度提高;②绝大部分有机反应都会直接导致混合体系(主要产物、副产物、未消耗殆尽的原料和试剂、溶剂、催化剂等),怎样把需要的化合物分离纯化出来往往是十分困难的,尤其当主副产物是同分异构体、理化性质差别很小的情况下,分离纯化则更为困难。因此有机合成的困难往往并不来自反应,而来自分离纯化,如果找不到适当的分离纯化方法,不仅会导致收率和效益大幅度降低,有时甚至会导致整个合成路线的失败。正是由于这种原因,串联反应越来越受到化学化工界的关注和重视,成为有机合成和有机化工领域中发展的热点。
原料分析模型:
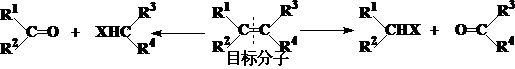
合成举例1、
原料分析:
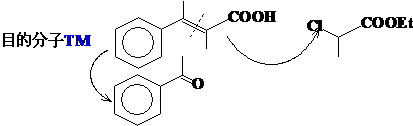
合成路线:(请完成)
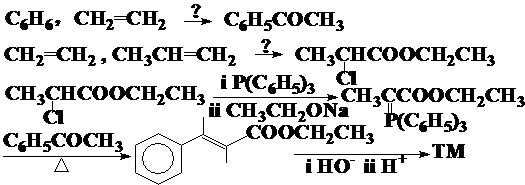
有机合成以合成新的化合物为主要目标。它是有机化学为经济建设和科技发展服务最直接的途径,也是有机化学教学过程中,学习和掌握有机化合物的基本性质和基本反应、培养教育对象的创新能力的重要手段。因此它在有机化学领域中占有最重要的地位,在整个化学学科中,也是最活跃、发展最快的领域之一。
有机合成的
主要任务:用原料的碳链作为建筑材料,构建目的分子的碳链(大楼的主体);
次要任务:其一是:官能团的转换(没有的需要导入,多余的需要消去,不合适的需要变换)。所以把它看作是次要任务,是因为从基本反应出发,所有的官能团之间都存在适当的转换路线(可以一步完成,也可能需要几步完成),因此从理念上必须坚信:所有的官能团之间都可以相互转换!只有树立这种理念,才能把所有碳链相同(碳原子数目和碳链形状相同)的分子看作是等价的,这对于学习和掌握有机合成的基本思路是十分关键的!如:C6H5COOH 、C6H5COOR’ 、C6H5COX 、C6H5CHO 、C6H5CH2OH 、C6H5CH2X C6H5CH2NH2 的碳链都与C6H5CH3相同,因此它们之间的关系只是官能团的转换。遇到这种情况,必须立即想到它们都可以用甲苯C6H5CH3转化而来。
其二是:官能团保护。官能团保护在两种情况下需要使用:①易于破坏但又需要保留的官能团;②控制多官能团化合物的化学反应选择性。所以把它看作是次要任务,是因为官能团保护都有固定的方法和保护范围(或条件)。
官能团保护常常需要与反应选择性结合考虑,因此首先要熟悉选择性的有关概念。反应的选择性分为三个层次,每个层次又分为三个级别:
层次 级别
化学选择性 专一性
反应的选择性 区域选择性 选择性
立体选择性 非选择性
只有生化反应才在三个层次上都具有专一性。生化反应所具有的高速、温和和专一性是化学反应的最高镜界,也是化学化工追求的最终目标。当然,生化反应的这些特点,都与酶(生化反应的催化剂)相关,因此,模拟酶的催化功能成为近代化学领域中研究的一个热点。
6、Cope重排和Claisen重排
Cope重排:属于1,5-二烯分子骨架的重排
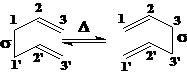
例如:
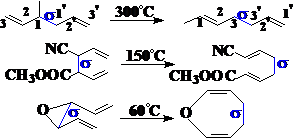
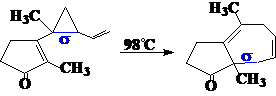
Claisen重排: C-O之间的s-单键的迁移,包括:
烯丙基乙烯醚的重排:

烯丙基芳基醚的重排:

如果邻位被占,烯丙基将通过2次迁移,迁移至对位,恢复原来的形状:

例如:
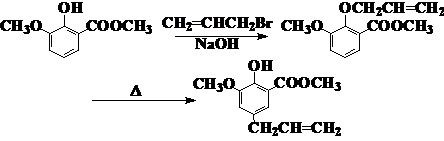
Cope重排和Claisen重排都属于3,3-s-迁移,过渡态为六元环,按FMO理论讨论如下:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com