
题目列表(包括答案和解析)
3.下列有关细胞癌变的叙述,正确的是
A.基因突变导致的各种细胞癌变均可遗传
B.石棉和黄曲霉素是不同类型的致癌因子
 C.人体的免疫系统对癌变细胞具有清除作用
C.人体的免疫系统对癌变细胞具有清除作用
D.癌变细胞内酶活性降低导致细胞代谢减缓
2.下列发生了细胞分化且能体现体细胞全能性的生物学过程是
A.玉米种子萌发长成新植株
B.小鼠骨髓造干细胞形成各种血细胞
C.小麦花粉经离体培养发育志单倍体植株
D.胡萝卜根韧皮部细胞经组织培养发育成新植株
1.下列与激素作用无关的实例是
A.草莓果实自然发育成熟 B.人舌尖触到蔗糖时感觉甜
C.自然生长的雪松树冠呈塔形 D.饥饿时人体血糖仍维持正常水平
34.(10分)(注意:在试题卷上作答无效)
人类在非秃顶和秃顶受常染色体上的等位基因(B,b)控制,其中男性只有基因型为BB
时才表现为非秃顶,而女性只有基因型为bb时才表现为非秃顶。控制褐色眼(D)和蓝色眼(d)的基因也位于常染色体上,其表现型不受性别的影响。这两对等位基因独立遗传。
回答问题:
(1)非秃顶男性和非秃顶女性结婚,子代所有可能的表现型为 。
(2)非秃顶男性和秃顶女性结婚,子代所有可能的表现型为 。
(2)一位父亲为秃顶蓝色眼而本人为秃顶褐色眼的男性与一位非秃顶蓝色眼的女性结婚。这位男性的基因型为 或 ,这位女性的基因型为 或 。若两人生育一个女儿,其所有可能的表现为 。
33.(11分)(注意:在试题卷上作答无效)
为探究不同条件对叶片中淀粉合成的影响,将某植物在黑暗中放置一段时间,耗尽叶片中的淀粉,然后取生理状态一致的叶片,平均分成8组,实验处理如下表所示。一段时间后,检测叶片中有无淀粉,结果如下表。

回答问题
(1)光照条件下,组5叶片通过 作用产生淀粉;叶肉细胞释放出的氧气来自于 的光解。
(2)在黑暗条件下,叶片能进行有氧呼吸的组别是 。
(3)组2叶片中合成淀粉的原料是 ,直接能源物质是 ,后者是通过 产生的。与组2相比,组4叶片无淀粉的原因是
(4)如果组7 的蒸馏水中只通入N2,预期实验结果是叶片中 (有、无)淀粉。
31.(10分)(注意:在试题卷上作答无效)
某同学从温度为55~65的泉水中筛选出能合成脂肪酶的细菌,并从该细菌中提取了脂肪酶。回答问题:
(1)测定脂肪酶活性时,应选择 作为该酶作用的物质,反应液中应加入 溶液以维持其酸碱度稳定。
(2)要鉴定该酶的化学本质,可将该酶液与双缩脲试剂混合,若反应液呈紫色,则该没的化学本质为
(3)根据细菌的生活环境,简要写出稳定该酶催化作用最适。温度的实验思路
(32)(11分)(注意:在试卷上作答无效)
回答下列与生态学有关问题;
(1)某人将未经检疫的外来鱼类和水草大量引进某水域生态系统后,导致生物多样性下降。从种间关系的角度分析,引起这种不良后果的原因是本地原有物种和外来物种之间可能存在着 、 、
的关系。
(2)某相对稳定的水域生态系统中主要有甲、乙、丙、丁、戊 5个种群,各种群生物体内某重金属的含量如下表。已知水中的该重金属被生物体吸收后难以通过代谢排出体外。假设在这5个种群构成的食物网中,消费者只能以其前一个营养级的所有物种为食。
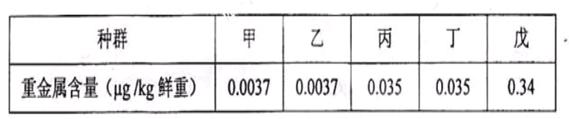
据表中数据绘出该生态系统的食物链。
30.(15分)(注意:在试题卷上答题无效)
金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
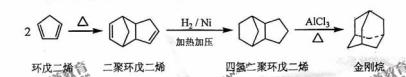
请回答下列问题:
(1)环戊二烯分子中最多有 个原子共平面;
(2)金刚烷的分子式为 ,其分子中的CH2基团有 个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
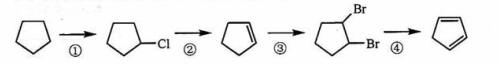
其中,反应①的产物名称是_______________,反应②的反应试剂和反应条件是___________,反应③的反应类型是_________________;
(4)已知烯烃能发生如下反应:
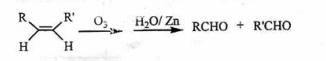
请写出下列反应产物的结构简式:
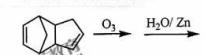 __________________________________;
__________________________________;
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基(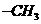 ,
,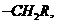
 )或烯基侧链经高锰酸钾酸性溶液氧化地羧基],写出A所有可能的结构简式(不考虑立体结构):
)或烯基侧链经高锰酸钾酸性溶液氧化地羧基],写出A所有可能的结构简式(不考虑立体结构):
。
29.(15分)(注意:在试题卷上作答无效)
请回答下列实验室中制取气体的有关问题。
(1)下图是用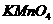 与浓盐酸反应制取适量氯气的简易装置。
与浓盐酸反应制取适量氯气的简易装置。
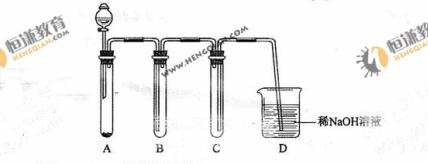
装置B、C、D的作用分别是:
B
C
D
(2)在实验室欲制取适量NO气体。
1下图中最适合完成该试验的建议装置是 (填序号):
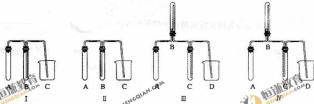
②根据所选的装置完成下表(不需要的可不填):
|
|
应加入的物质 |
所起的作用 |
|
A |
|
|
|
B |
|
|
|
C |
|
|
|
D |
|
|
③简单描述应观察的实验现象 。
28.(15分)(注意:在试卷上作答无效)
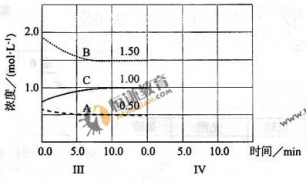
反应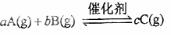
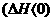 在等条件下进行。改变其他反应条件,在Ⅰ、 Ⅱ、 Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
在等条件下进行。改变其他反应条件,在Ⅰ、 Ⅱ、 Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)反应的化学方程式中,a:b:c为______________;
(2)A的平均反应速率υⅠ (A)、υⅡ (A) 、υ Ⅲ(A)从大到小排列次序为________________;
(3)B的平衡转化率αⅠ (B)、αⅡ (B) 、α Ⅲ(B)中的最小的是_________,其值是______________;
(4)由第一次平衡到第二次平衡,平衡移动的方向是______________________,采取的措施是______________________________;
(5)比较第Ⅱ阶段反应温度(T2)和第 Ⅲ 阶段反应温度(T3)的高低: T2______T3 (填“>” “<” “=”)判断的理由是_______ ____
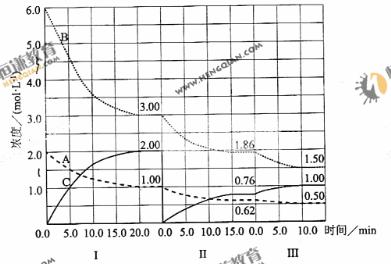
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示第IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C)。
27.(15分)(注意:在试题卷上作答无效)
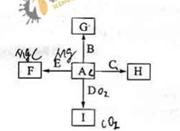
下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:
①
反应 能放出大量的热,该反应曾应用于铁轨的焊接;
能放出大量的热,该反应曾应用于铁轨的焊接;
②
D是一种常见的温室气体,它和E可以发生反应: F中E元素的质量分数为60%。
F中E元素的质量分数为60%。
回答问题:
(1)1中反应的化学方程式为______________________________
(2)化合物I的电子式为______________,它的空间构型是________________
(3)1.6g 溶于盐酸,得到的溶液与铜粉完全反应,计算至少需要铜粉的质量(写出离子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程为______________________________,
反应后溶液与过量化合物I反应的离子方程式为_____________________.
(5)E 在I中燃烧观察到的现象是______________________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com