
化学计算
考点聚焦
1、高考中化学计算主要包括以下类型:①有关相对原子质量、相对分子质量及确定分子式的计算;②有关物质的量的计算;③有关气体摩尔体积的计算;④有关溶液浓度(质量分数和物质的量浓度);⑤利用化学方程式的计算;⑥有关物质溶解度的计算;⑦有关溶液pH值与氢离子浓度、氢氧根离子浓度的简单计算;⑧有关燃烧热的简单计算;⑨以上各种化学计算的综合应用。
2、常见题型为计算选择题,计算填空题、实验计算题、计算推断题和综合计算题,而计算推断题和综合计算题,力求拉开学生的层次。
3、近年高考化学计算题主要有以下特点:
(1)注意速算巧解
一般在第Ⅰ卷中会出现五到七个左右要计算的量很少或者根本不需要计算的试题。其命题意图是考查对化学知识的理解、掌握和运用。重点考查学生运用题给信息和已学相关知识进行速算巧解的能力。
(2)起点高、落点低
这方面主要是第Ⅱ卷中的计算题。试题常以信息给予题的形式出现,但落点仍是考查基本计算技能。
(3)学科渗透,综合考查
主要考查各种数学计算方法的运用、物理学科中的有效数字及语文学科的阅读能力。
(4)综合计算题的命题趋势是理论联系实际,如以生产、生活、环境保护等作为取材背景编制试题,考查视野开阔,考查学生用量的观点把握化学知识、原理、过程等。
4、学生化学计算题失分的主要原因
 1、审题不够仔细;
1、审题不够仔细;
2、基础不够扎实;
3、思考不够全面;
八个“不够” 4、思维不够灵敏;
5、运算不够准确;
6、格式不够规范;
7、表达不够清楚;
8、时间不够充裕。
化学计算是学生必须掌握的基本技能之一。而思维能力较差的学生就是害怕计算,其原因是:一、对计算所依托的基本化学原理和性质不熟悉;二、对基本的计算技能掌握不到位;三、思维不灵活,不会审题,不会寻找解题的突破口,不会分析问题,也就不会解决问题。要求教师加强解题策略相关知识的教学;加强学科问题解决的研究。
1. 将Wg铁、氧化铁和氧化铜组成的混合物粉未放入100mL 4.4mol/L盐酸中,反应完全后得氢气896mL(标况),生成的溶液中只有FeCl2、HCl和
分析:解答此题的关键,是审清题意,找出等量关系,选准突破口。首先确定由生成溶液中的盐酸可知反应后的
解法一:
Cu的物质的量 mol
mol
CuO的质量=0.02×80=1.6(g)
设混合物中Fe2O3的物质的量为x。


 CuCl2 +
Fe = FeCl2 +Cu
CuCl2 +
Fe = FeCl2 +Cu
0.02mol 0.02mol
根据反应耗用盐酸的量列方程求解

Fe2O3的质量 (g)
(g)
Fe的质量 (g)
(g)
解法二:
设混合物中含铁的物质的量为 ,Fe2O3的物质的量为
,Fe2O3的物质的量为
根据氧化还原反应中的电子守恒


2H+――H2得电子的物质的量0.04×2(mol)
CuO――Cu得电子的物质的量0.02×2(mol)

根据 守恒列方程
守恒列方程

解方程组

Fe的质量
Fe2O3的质量
2. 某化工厂用NH3制备NH4NO3。已知NH3制NO的产率是96%;NO制HNO3的产率是92%,HNO3与NH3反应生成NH4NO3。则制HNO3所用去NH3的质量占总耗NH3的质量的百分比是多少?(不考虑生产上的其它损耗)
分析:根据反应

由于生产中NO2与H2O反应生成HNO3和NO,不断地补充空气使NO多次被氧化成NO2,被水吸收,最后比较完全转化HNO3,因此,第三步反应在考虑到循环反应后可用下式表示:

由以上四个反应可得最初反应物与最终产品的关系式:
4NH3~4NO~4NO2~4HNO3
设生产 耗用NH3为x吨,生产NH4NO3耗用NH3 y吨
耗用NH3为x吨,生产NH4NO3耗用NH3 y吨

生产HNO3耗用NH3的质量百分比
答:略。
3. 金属锡的纯度可以通过下述方法分析:将试样溶于盐酸,反应的化学方程式为:Sn+2HCl=SnCl2+H2 再加入过量的FeCl
再加入过量的FeCl 溶液,发生如下反应:SnCl2+2FeCl
溶液,发生如下反应:SnCl2+2FeCl =SnCl4+2FeCl2最后用已知浓度的K2Cr2O7溶液滴定生成Fe2+,反应的化学方程式为:
=SnCl4+2FeCl2最后用已知浓度的K2Cr2O7溶液滴定生成Fe2+,反应的化学方程式为: 现有金属锡试样
现有金属锡试样
分析:该题是应用关系式法解多步反应的综合计算。根据题目所给出的三个化学反应,得出Sn与K2Cr2O7的物质量的关系。


答:略。
巩固联系
4. 在100mL 36.5%的浓盐酸(密度为
分析:任何溶液在稀释时,溶液和溶剂的量都要发生变化,但溶质的量不变,据此可以得到稀释下列各种浓度的溶液计算公式。
百分比浓度溶液的稀释公式:
浓溶液的质量×浓溶液的浓度 = 稀溶液的质量×稀溶液的浓度
mol尔浓度的溶液稀释公式:
浓溶液的浓度×浓溶液的体积(L) = 稀溶液的浓度×稀溶液的体积
同一溶质的两种不同浓度的溶液混合时,混合溶液的浓度介于溶液之间,混合液跟两原溶液中溶质、溶液量的基本关系是:
(1)混合液中所含溶质的总量等于两原溶液的溶质质量之和。
(2)混合溶液的质量等于两原溶液的质量之和,但体积不等于两原溶液的体积之和(当两原溶液很稀时,通常把混合液的体积近似地看做两原溶液的体积之和。)
在应用上述关系进行复杂的混合溶液计算时,可先算出混合溶液的总质量和溶质的总质量,然后再求出混合溶液的浓度。
设需加入VmL 2mol/L的盐酸
混合液中溶质的总物质的量

混合溶液的总体积:

混合液的物质的量浓度:

答:略
5. 氯气通入氨水中发生下列反应: L氯、氮混合气(90%Cl2、10%的N2)通入浓氨水实验测得逸出气体在标况下为
L氯、氮混合气(90%Cl2、10%的N2)通入浓氨水实验测得逸出气体在标况下为
分析:设有xg氮气被氧化
由方程式可得出:


答:略。
6. 将5.000gNaCl、NaBr、CaCl2的混合物溶于水,通入氯气充分反应,然后把溶液蒸干并灼烧,得残留物
分析:根据题意可列出下图示,帮助审清题意,找出思路和解法。

根据图示可分析:
(1)CaCO3的质量为

(2)混合物中通入Cl2

(3)NaCl的质量
(4)各组分的百分含量


7.向含0.02mol Al3+的明矾溶液中,逐滴加入0.1mol/L的Ba(OH)2溶液时,产生沉淀的质量y(g)与Ba(OH)2溶液的体积x(mL)的关系如图所示。求图中:
V1=
V2=
m1=
m2=
分析:本题要从分析图中所体现的产生沉淀的质量与加入Ba(OH)2体积的函数关系求出V1、V2和m1、m2的值。
从图中可以看出,当加入V1mL的Ba(OH)2时,可得沉淀m
(1)含有0.02mol Al3+的明矾溶液中含有0.04mol的SO42-。
当加入V1mL Ba(OH)2时,

(2)当加入V2mL Ba(OH)2溶液时,


8.某金属R
分析:设R的原子量为m,两种金属氯化物的分子式分别为RClx和RCly

 ………①
………①

 ………②
………②

讨论:(1)当 不合理
不合理
(2)当 合理
合理
(3)当 不合理
不合理

9. 混合两种未知物的溶液,生成
分析:能使石灰水变浑浊且无刺激性气味的气体应是CO2,故
设碳酸盐的分子式为MCO3

 此二价金属为Ca。
此二价金属为Ca。
 滤液蒸干后得
滤液蒸干后得
 此气态氧化物的mol尔质量为:
此气态氧化物的mol尔质量为:
 (g/mol)
(g/mol)
分解产物的mol尔比:
H2O∶RxOy ∶
∶ 0.05∶0.025
0.05∶0.025 2∶1
2∶1
 分解产物为H2O和气态氧化物,分解温度为
分解产物为H2O和气态氧化物,分解温度为
 此盐只能是NH4NO3
此盐只能是NH4NO3
设其分解产物为H2O和NxOy
则对NxOy而言有
则
讨论, 均为正整数,且只可能是1或2,
均为正整数,且只可能是1或2,
(1)若
(2)若
由此可肯定此盐为NH4NO3,热分解产物为H2O和N2O。
 未知物是
未知物是

10. 两种烃的混合气体20mL,跟过量的氧气混合点燃,当产物通过浓H2SO4时,体积减小30mL,通过碱石灰后的体积又减少40mL(以上均换算成标准状况的体积),问该混合物的组成可能有几种?在各种可能组成中,每种烃各是多少?
分析:气态烃的碳原子数都小于4。20mL混合烃完全燃烧生成40mL CO2和30mL水蒸气,可知1mol混合烃平均含2mol C原子和3mol H原子,从而推知,该混合烃只能是C2H6和C2H2或C2H4和C2H2的混合物。
讨论:
(1)若混合烃含有x mL C3H6,则含有(20-x)mL C2H2

由题意可知:

C2H2:20-5=15(mL)
(2)若混合烃含有y mL C2H4,则含有 ,
,

 可能有两种组合
可能有两种组合
11. 现有氧化铜和碳粉的混合物共Amol,将它在隔绝空气条件下加热,反应完全后,冷却,得到残留固体。
(1)写出可能发生反应的化学方程式
(2)若氧化铜在混合物中的量的比值为
问:x为何值时,残留固体为何种物质?写出残留固体的物质的量与x值之间 的关系。将结果填入下表。
残 留 固 体
x值
分 子 式
物质的量
分析:(1)首先写出有关的化学反应方程式,根据化学方程式中有关物质间的物质的量的关系,分析当CuO恰好完全反应时,x值是多少?

按①式反应,x值为 时,反应物恰好反应;按②式反应,x值为
时,反应物恰好反应;按②式反应,x值为 时,反应物恰好完全反应。
时,反应物恰好完全反应。
(2)当 时,CuO过量,按C的量计算。
时,CuO过量,按C的量计算。

剩余CuO的物质的量
(3)当 不足量,按CuO的量计算,生成铜的量为Ax。
不足量,按CuO的量计算,生成铜的量为Ax。
(4)当 时,C过量,按②式中的CuO的量计算,生成铜为Ax,剩余C的物质的量为:
时,C过量,按②式中的CuO的量计算,生成铜为Ax,剩余C的物质的量为:

将所得结果的有关数值填入下表:
x 值
残 留 固 体
分 子 式
物 质 的 量

Cu
CuO
A(3x-2)

Cu
Ax(或 A)
A)

Cu
Ax

Cu
Ax(或 )
)

Cu
C
Ax
A(1-2x)
12.

(1)C中发生的反应,其化学方程式是 。已知原C中的气体为单一气体,它是 。(若有多种可能答案,需一一列出。)将反应后C筒中的气体,用水吸收后,气体体积,减小一半,则与水反应前C中的气体是 。(若有多种答案需一一列出。)
(2)若实验开始前A、C中的气体体积(换算成标况)分别为
分析:本题要求学生将分子量、物质的量、气体摩尔体积、化学方程式计算与元素及其化合物的性质结合起来,根据试题给出的条件,进行分析、推理和论证。
(1)由C筒中发生的化学现象气体由无色变为红综色,可判断C中发生的化学反应为:2NO+O2=2NO2;又根据C筒中的气体反应后并无体积变化,可知C中为NO,由B管进入C中气体为纯O2,反应后O2并未过量。与水反应后,气体体积减半,已知与水反应前C筒中的气体为NO2和NO的混合气。
(2)设与水反应前C筒中NO2的体积为 ,NO为
,NO为  ,根据题意列方程组:
,根据题意列方程组:

 由B管进入C筒中的
由B管进入C筒中的
若

对照试题所给出的已知气体中没有一种气体的mol尔质量等于或大于

讨论:(1)若A中的气体全部是CO2(即进入C的O2全部由CO2和Na2O2反应而得。)根据反应方程式 反应生成O2的体积为
反应生成O2的体积为 (L)这与进入C筒中O2的体积不符。(
(L)这与进入C筒中O2的体积不符。(
(2)若A中的气体是CO2和O2的混合气。设A中CO2和O2的体积分别为 。
。
根据题意
解题:

 该结果与题设条件相符,所以A中的气体是CO2和O2的混合气体。
该结果与题设条件相符,所以A中的气体是CO2和O2的混合气体。
A中的气体的质量 。
。
13. 向
分析:解题的关键是抓住
设
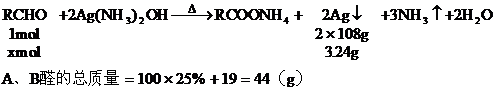

混合醛的平均分子量
设A醛、B醛分子式分别为 ,则A、B的分子量分别为14n+16、14n+30
,则A、B的分子量分别为14n+16、14n+30

14. 今有分子组成相差1个碳原子和若干个氢原子的两种单烯烃的混合物,若取该单烯烃混合物的质量为
(1)试确定原混合烃中两种单烯烃的分子组成。
(2)为了使该混合烃对氧气的密度≥
分析:
(1)取单烯烃混合物为
∴混合烃的平均分子量≤42
∴该混合烃的组成C2H4和C3H6
(2)该混合烃的平均分子量≥33.6(1.05×32)
设混合烃中C3H6为x mol,C2H4为y mol
则 
解得 
又∵燃烧产物增加的物质的量由C3H6燃烧所致

∴ 
∴C2H4的物质的量≥0.4
∴
15. 镁条在空气中燃烧生成氧化镁和氮化镁。将燃烧后的产物溶解在60毫升浓度为2.0mol/升的盐酸中,再用20毫升0.5mol/升NaOH溶液中和多余的盐酸,然后在此溶液中加过量的碱,把氨全部蒸出来,用稀HCl吸收,稀HCl增重
分析:此题涉及反应较多,如按常规计算非常复杂,如巧用电荷守恒法可使计算大为简化。
该题反应变化的图式:
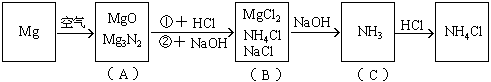
在图(B)中,根据电荷守恒,有下列关系:

16. 饱和烃A和不饱和烃B在常温下均为气体,其中A含C原子数多于B。
(1)将A、B按一定比例混合。
A的分子式
B的分子式
VA∶VB
(2)1mol该混合气体恰好能使含0.4mol溴的CCl4溶液完全褪色,推断上述组合中符合该条件的A与B的分子式并填入下表
A的分子式
B的分子式
分析:(1)本题是用计算推理方法确定混合烃的组成。

也可用十字交叉来解:

其它组合可依此类推,于是得到:
组合的编号
A的分子式
B的分子式

①
C4H10
C2H4
4∶1
②
C4H10
C2H2
4∶1
③
C4H10
C3H6
3∶2
④
C4H10
C3H4
3∶2
(2)
A的分子式
C4H10
C4H10
B的分子式
C2H2
C3H6
17. 有不同浓度的NaOH溶液各取100mL分别通入SO2
分析:SO2与NaOH溶液反应,可能有三种情况:NaOH过量,所得固体为Na2SO3和NaOH的混合物;SO2部分过量,所得固体为Na2SO3和NaHSO3的混合物;SO2极大过量所得固体为NaHSO3,因此本题应首先确定固体的成分。
(1)应用极值法先确定两个极值
a:设SO2与NaOH完全作用生成Na2SO3

b:设SO2极大过量,最终产物为NaHSO3

(2)讨论确定产物
a:因 ,所以b g固体为Na2SO3和NaHSO3的混合物
,所以b g固体为Na2SO3和NaHSO3的混合物
b:因 所以
所以
(3)计算
a:第一种情况,设生成Na2SO3为xmol,NaHSO3为ymol

b:第二种情况:因NaOH过量,所以H2SO2完全反应。设参加反应的NaOH为amol,生成Na2SO3为bmol,过量的NaOH为Cmol

18. 已知Cl-与Ag+,每次新生成的AgCl中又有10%见光分解成单质和Cl2,Cl2又可在水溶液中歧化成HClO3和HCl,而这样形成的Cl-又与剩余的Ag+作用生成沉淀,这样循环往复,直到最终。现有含1.1molNaCl的溶液,向其中加入足量AgNO3。求最终能生成多少克难溶物(Ag和AgCl)?若最后溶液体积为
[解析]此题为运用数列知识解决化学问题的试题。发生反应为
Ag++Cl-=AgCl↓,2AgCl===2Ag+Cl2,3Cl2+3H2O=HClO3+5HCl由题意可知n(AgCl):n(Ag)=9:1,由2AgCl――Cl2――1/3HClO可知1molAgCl可转化为HClO31/6mol,因此n(AgCl):n(Ag):n(HClO3)=9:1:1/6=54:6:1,总反应方程式为
60Ag++55Cl-+3H2O=54AgCl↓+6Ag↓+ClO3-+6H+,从而求出m(难溶物)=
19. Na2S2O3•5H2O(俗称海波)是照相业常用的一种定影剂,常采用下法制备:将亚硫酸钠溶液与硫粉混合共热,生成硫代硫酸钠Na2SO3+S=Na2S203,滤去硫粉,再将滤液浓缩、冷却,即有Na2S2O3•5H2O晶体析出,该法制得的晶体中常混有少量Na2SO3和Na2SO4的杂质。
为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,分别加入相同浓度的H2SO4溶液20mL,充分反应后滤出硫,并将滤液微热(假定生成的SO2全部逸出),测得有关实验数据如下(标准状况):
第一份
第二份
第三份
样品的质量/g
12.60
18.90
28.00
二氧化硫的体积/L
1.12
1.68
2.24
硫的质量/g
1.28
1.92
2.56
(1)样品与硫酸可能发生反应的离子方程式为 ;
(2)根据上表数据分析,该样品 (填选项字母);
A、只含有Na2S203
B、含有Na2S203和Na2S03
C、含有Na2S203 、Na2S03,和Na2S04三种成分
(3)试计算,该样品中各成分的物质的量之比?
(4)所加硫酸溶液的物质的量浓度为 ;
(5)若将
试讨论:当a在不同取值范围时,SO2的体积b,并请在下图中画出b随a的变化的曲线。
b(L)
 6.72
6.72
 5.60
5.60
 4.48
4.48
 3.36
3.36
 2.24
2.24








 1.12
1.12
0 0.01 0.02 0.03 0.04 0.05
[解析]这是一道综合题,题中涉及了混合物反应的计算,过量问题的计算、计算推断、数据缺省型的计算、范围讨论计算及数形结合计算等。
答案:(1)略。由表中数据分析可知第一份、第二份样品进行实验时H2SO4足量,从而求算得出(2)C和(3)n(Na2S2O3):n(Na2SO3):n(Na2SO4)=4:1:1.
(4)由表中数据分析可知第三份实验中H2SO4量不足,求出C(H2SO4)=5.0mol/L。
(5)m样品/m1=
图象为
b(L)
 6.72
6.72



 5.60
5.60
 4.48
4.48
 3.36
3.36
 2.24
2.24








 1.12
1.12
0 0.01 0.02 0.03 0.04 0.05
20.硫铁矿高温下空气氧化产生二氧化硫:4FeS2+11O2→8SO2+2Fe2O3
设空气中N2、O2的含量分别为0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:
(1)1.00mol FeS2完全氧化,需要空气的体积(标准状况)为 L
(2)
(3)用空气氧化FeS2产生的气体混合物中,O2的含量为0.0800,计算SO2的含量。
(4)设FeS2氧化产生的气体混合物为
① 写出a和b的关系式
② 在右图中画出a和b的关系曲线(FeS2氧化时,空气过量20%)
说明:为方便作图,纵坐标用13b表示

命题意图:主要考查对元素化合物知识与生产实际的联系,考查学生严密的分析能力、和逆向思维能力及完整的解综合试题的能力,该题是图、数结合的由若干小题组合的综合计算,逐题深入,灵活性强,意在考查学生分析问题和解决问题的实际能力。
解析:(1)4FeS2 → 11O2
4 11 所需O2体积为:
1 mol  mol
mol

(2)11O2 → 8SO2
11 8
 L
y y=
L
y y=

生成的气体体积为:
(3)设SO2为X(体积分数),
11O2 → 8SO2
11 8
 x
x
O2的总体积为:( +0.0800) ; N2的总体积为:
+0.0800) ; N2的总体积为: (
( +0.0800);若混合气体的总体积为1,则N2的总体积也可表示为:1-0.0800-X
+0.0800);若混合气体的总体积为1,则N2的总体积也可表示为:1-0.0800-X
所以有:4×(11×X/8+0.0800)=1-0.0800-X
X=0.0923
(4)①FeS2氧化产生的气体混合物为 ,N2为 4(
,N2为 4( )L,固有:4(
)L,固有:4( )+ a + b =100 解之得:
)+ a + b =100 解之得:
13b=200-
②由一次函数列表为:
横坐标(a)L
20
10
3
纵坐标13b
0
100
170

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com