
题目列表(包括答案和解析)
3.设NA为阿伏加德罗常数,下列叙述中错误的是七彩教育网
A.在标准状况下,22.4L空气中约有NA个气体分子
B.1mol 白磷分子(P4)中含有的非极性键数目为6 NA
C.1mol D318O+离子中含有的中子数为13 NA
D.含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2︰3
2.下列变化过程中无化学键断裂或生成的是
A.石墨转化为金刚石 B.NaCl晶体溶于水
C.干冰升华 D.氮的固定
1.下列说法中,正确的说法有几句:
①所有基态原子的核外电子排布都遵循构造原理;②同一周期从左到右,元素的第一电离能、电负性都是越来越大;③所有的化学键和氢键都具有相同的特征:方向性和饱和性;④所有的配合物都存在配位键,所有含配位键的化合物都是配合物;⑤所有含极性键的分子都是极性分子;⑥所有离子化合物中都含有离子键。
A.无 B.1句 C.2句 D.3句
3、判断元素的原子序数与相近的稀有气体大的元素判法,元素的原子序数与相应的稀有气体原子序数相减,所得的差值确定该元素所在的主族序数,相应稀有气体所在周期的下一周期即为该元素所在周期。
 如某主族元素的原子序数为37,37号元素与相近的稀有气体是36,相差37-36=1,又36号稀有在第4周期,所以,37号元素周期中位于第五周期,第ⅠA族。
如某主族元素的原子序数为37,37号元素与相近的稀有气体是36,相差37-36=1,又36号稀有在第4周期,所以,37号元素周期中位于第五周期,第ⅠA族。
2、判断元素的原子序数与相近的稀有气体小的元素判法。元素的原子序数与相应的独有气体原子序数相减,所得的差确定法元素所在的主族序数,相应有气体所在周期。
如某主族元素的原子序数为35,试确定该元素在周期表中位置,35号元素与相近的稀有气体是36,相差为36-35=1,而36号稀有气体在第每周期。所以,35号元素在元素周期表中位于第4周期第ⅦA族。
1、熟记稀有气体元素的原子序数及周期数。
原子序数:2 · 10 · 18 · 36 · 54 · 86 · 118
周 期 数:一 · 二 · 三 · 四 · 五 · 六 · 七
2、由原子序数可写出相应的原子结构简图,进而判定该元素在元素周期表中的位置。
如判断20号元素周期表中位置。
20号元素的原子结构简图为+20 2 8 8 2
在元素周期表中位置第四周期,第ⅡA族
1、直接由原子结构简图速判法。
由原子结构简图可知该元素的电子层数和最外层电子数。对主族元素而言,其电子层数就是该元素在元素周期表中的周期序数;其最外层上的电子数就是该元素在周期表中的族序数。由该元素在周期表中的周期和族决定元素的位置。
如某主族元素的原子结构示意图为
+35 2 8 18 7
根据它有个电子层,最外层上有7个电子,又是主族元素,所以它在元素周期中位于第4周期,第ⅦA族。
11.A.CHCl3 B.CHClF2 C.CF2==CF2
D.
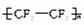 ?
?
B→C:2CHClF2 CF2==CF2+2HCl
CF2==CF2+2HCl
C→D nCF2==CF2
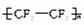

10.2NaCl+2H2O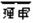 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
H2+Cl2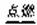 2HCl
2HCl
CH≡CH+HCl CH2==HCl
CH2==HCl
nCH2CHCl
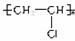
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com