
题目列表(包括答案和解析)
1、风化:风化是指在室温和干燥空气里,结晶水合物失去一部分或全部结晶水的现象。风化是一个化学变化过程。例如,日常生活中碱块(Na2CO3·10H2O)变成碱面(Na2CO3),就是风化现象。(自然岩石的风化是指岩石与空气、水、二氧化碳等物质长期作用,发生了复杂的化学反应,形成了许多大小不等的岩石碎块或砂粒的作用。)
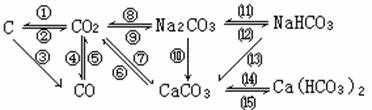
①_____________________________________
②_____________________________________
③_____________________________________
④_____________________________________
⑤_____________________________________
⑥_____________________________________
⑦_____________________________________
⑧_____________________________________
⑨_____________________________________
⑩_____________________________________
⑾_____________________________________
⑿_____________________________________
⒀_____________________________________
⒁_____________________________________
⒂_____________________________________
5、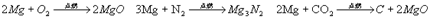 ,
,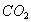 在空气中含量太少,
在空气中含量太少,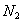 虽然含量高,但化学性质不活泼,而
虽然含量高,但化学性质不活泼,而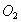 化学性质活泼,所以MgO多
6、依据
化学性质活泼,所以MgO多
6、依据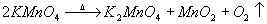 原理,多产生的
原理,多产生的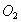 只可能来自
只可能来自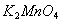 或
或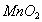 ,或二者都分解放氧
,或二者都分解放氧 答:只取
答:只取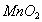 加强热,没有
加强热,没有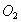 产生,而同样条件下
产生,而同样条件下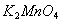 可放出
可放出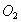


46].(1)在酸性溶液中PbO2、NaBiO3是强氧化剂,都能把Cl-氧化成Cl2。写出反应的方程式。
(2)应在什么介质中制备PbO2、NaBiO3?写出反应方程式。
45].将NaBiO3固体(黄色、微溶)加入到MnSO4和H2SO4的混合液中加热。固体溶解,溶液显紫色(反应生成的Bi3+无色)。请写出该反应的离子方程式并注明氧化剂、还原剂。
44].工业上制备的硫磺是将硫铁矿和焦炭的混合物放在炼硫炉中,并在有限的空气中燃烧制得的。请配平方程式:FeS2+C+O2-Fe3O4+CO+S。
43].以最小整数比配平下列反应方程式:
RuS2+KClO3+HCl-RuO4+RuCl3+H2S+S+KCl
42].N2H4在一定条件下热分解,产生NH3、N2和H2,设反应后混合气体密度为原来的x(同温同压下)。
(1)如果产生NH3和N2物质的量比为2︰1,写出N2H4分解的化学方程式;
(2)如果x=7/13,写出N2H4分解的化学方程式;
(3)确定x的取值范围: ;
(4)计算产生的混合气体中NH3、N2和H2的体积含量。(给出推理、计算过程)
41].S2O在碱性条件下发生的歧化反应如下:
S2O+OH-→S2-+S2O42-+SO32-+H2O
该反应包含两个独立的歧化反应,它们的离子方程式分别为 、 。如果这两个独立的歧化反应是等物质的量发生的,则按上述S2O的总歧化反应的配平的离子方程式为 。
40].配平Cl2+AgF+H2O-AgClO3+AgCl+HF+O2时有无穷多组系数,如5,10,5-1,9,10,1或7,14,7-1,13,14,2;……。若H2O前面的系数为11,写出配平后的系数 若a,b,c……为任意自然数,试用字母配平方程式,并能反映出所有情况:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com