
题目列表(包括答案和解析)
4.将标准状况下的11.2 L甲烷和22.4 L氧气混合点燃,恢复到原状况后,气体的体积为( )
A.11.2 L B.22.4 L C.33.6 L D.44.8 L
[解析]选A。CH4+2O2 CO2+2H2O,因此11.2 L甲烷与22.4 L氧气恰好完全反应生成11.2 L的CO2气体,故选A。
点燃
3.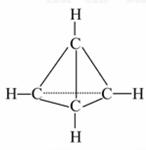 (2010·宣城同步检测)已知一种
(2010·宣城同步检测)已知一种
有机物的分子式为C4H4,分子结构如
图所示,若将该有机物与适量的氯气
混合光照,则生成的卤代烃的种类共
有( )
A.2种 B.4种 C.5种 D.6种
[解析]选B。据C4H4分子结构可知分子中4个碳原子形成正四面体结构,所以分子完全对称,因此C4H3Cl、C4H2Cl2、C4HCl3、C4Cl4分子均只有一种结构,故生成的卤代烃一共有4种。
2.下列叙述错误的是( )
A.通常情况下,甲烷跟强酸、强碱、强氧化剂不起反应
B.甲烷化学性质比较稳定,不能被任何氧化剂氧化
C.甲烷跟氯气反应无论生成CH3Cl、CH2Cl2、CHCl3还是CCl4,都属于取代反应
D.甲烷的四种取代物都难溶于水[解析]选B。CH4的性质比较稳定,通常情况下,不与强酸、强碱、强氧化剂反应,而不是不能被任何氧化剂氧化,A正确,B错误;CH4在光照条件下与Cl2发生 取代反应,生成4种有机产物,它们是CH3Cl、CH2Cl、CHCl3和CCl4,且均难溶于水,故C、D均正确。
取代反应,生成4种有机产物,它们是CH3Cl、CH2Cl、CHCl3和CCl4,且均难溶于水,故C、D均正确。
1.下列气体中不含甲烷的是( )
A.天然气 B.水煤气 C.油田气 D.沼气
[解析]选B。甲烷是天然气、油田气和沼气的主要成分,而水煤气的主要成分是CO和H2。
10.(1)据《科技消息报》报道:由于废气排放致使地球南极上空的a层出现了400多万平方公里的空洞,有害宇宙线长驱直入,把b分解,密度较小的氢就会逃逸到宇宙空间,剩下的氧最终会使土壤c,从而使地球人类正在重蹈火星的覆辙。根据以上叙述,回答问题。
①填充:a____b____c_____。
②写出a与b对应的化学方程式:a_________b_________。
(2)据《中国环境报》报道:从一份科技攻关课题研究结果显示,我国酸雨区已占国土面积的40%。研究结果还表明,酸雨对我国农作物、森林等影响区域大。
如图是研究酸雨成因的学生实验用的“催化棒”。用两根外面套有玻璃管的粗导线穿过橡皮塞并固定于粗玻璃管中,在其中一端用电热丝连接起来,即制成“催化棒”。

实验时,先接通直流电源,使电热丝红热,然后将红热的电热丝伸入装有SO2和空气的集气瓶中,瓶中立即出现_____ 现象,再往其中加入盐酸酸化的氯化钡溶液,又出现______现象。
请回答:
①以上实验中可得出酸雨成因的化学原理是_________。
②目前一座中等城市每年用煤约300万吨,其含硫量如按1%计算,则每年排放SO2多少吨?若此二氧化硫有60%转化为硫酸,相当于生成多少吨98%硫酸?
③为了防治酸雨,降低煤燃烧时向大气排放的SO2,工业上将生石灰和含硫煤混合后使用。请写出燃烧时,有关“固硫”(不使硫的化合物进入大气)反应的化学方程式______,并比较此法与将“石灰石粉未与含硫煤混合”使用防治酸雨的方法,哪个更好些?答_________(填“生石灰法”或“石灰石法”)
④如每隔一段时间测定某份雨水(酸雨)样品的pH,请作出有关时间与酸雨pH变化的曲线图。
⑤国际上最新采用“饱和亚硫酸钠溶液吸收法”,请写出有关反应的化学方程式______。
9.假设SO2接触氧化过程产生的热量有70%可以利用,请问生产100 t 98%的硫酸在接触氧化过程中能节约多少能量。(已知ΔH= -98.3kJ/mol)
8.取1g含SiO2和FeS2的矿石样品,在氧气中充分燃烧,残余固体质量为0.84g,用这种矿石100吨,可以制得98%的H2SO4多少吨?(设生产过程中硫损失2%)
7.含FeS280%的硫铁矿,煅烧时损失硫5%,SO2氧化成SO3时利用率为98%,问生产1 t 98%的硫酸,需要这种硫铁矿多少t?
6.硫酸最古老的生产方法是:把绿矾装入反应容器中加强热,会流出油状物,并放出有刺激性气味的气体,反应容器中的固体变为红色。这个变化过程可用两个化学方程式表示: , 。
5.接触法制硫酸的原料是 ,生产过程的化学反应原理是: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com