
题目列表(包括答案和解析)
4. 下列过程属于熵增加的是( )
A.一定条件下水由气态变为液态 B.高温高压条件下氮气和氢气合成氨气
 C.碳酸铵受热分解 D.CO点燃时生成CO2
C.碳酸铵受热分解 D.CO点燃时生成CO2
3.在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A) υ(B)、υ(C)(mol·L-1·s-1)表示,且有如下所示关系:υ(B)=3υ(A);3υ(C)=2υ(B)。则此反应可表示为( )
A.2A+3B=2C B.A+3B=2C C.3A+B 2C D.A+3B
2C D.A+3B 2C
2C
2.下列过程需要通电才能进行的是( )
① 电离 ② 电解 ③ 电镀 ④ 电化学腐蚀
A.① ② B.② ④ C.② ③ D.全部
1.为了建设环境友好型社会,节能减排将成为我国政府目前工作的重点,因此节约能源与建设新能源是摆在当前的一个课题。针对这一现象,某化学学习研究性小组提出如下方案,你认为不够科学合理的是( )
A.采用电解水法制取氢气作为新能源 B.完善煤液化制取汽油的技术
C.研制推广以乙醇为燃料的汽车 D.进一步提高石油加工工艺
14.中药秦皮中含有的七叶内酯属于香豆素类,具有显著的消炎作用,是抗痢疾杆菌的有效成分。其结构简式如下:
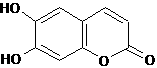
(1)七叶内酯的含氧官能团的名称为 。
(2)七叶内酯可以发生的反应类型有 (填序号)。
a.加成反应 b.取代反应 c.消去反应
(3)香豆素类物质常被看做是肉桂酸的衍生物。工业上可用物质A制备肉桂酸和肉桂醇。反应关系如下:
|
|
|


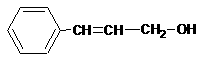
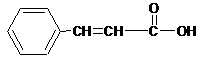
肉桂醇 肉桂酸
A的结构简式为 。
(4)七叶内酯与足量氢氧化钠稀溶液充分反应。化学方程式为
。
12. 25℃时, 已知反应:CO2(g) + H2(g) CO (g) + H2O
(g) △H = + 41 kJ/mol。回答下列问题:
25℃时, 已知反应:CO2(g) + H2(g) CO (g) + H2O
(g) △H = + 41 kJ/mol。回答下列问题:
(1)该反应属于 反应(“放热”或“吸热”), 判断依据是
(2)能判断该反应是否已达平衡状态的依据是 (填序号)。
a.混合气体中n(CO)不变 b. v消耗(CO2) = v生成(CO)
c.混合气的总物质的量不变 d. 容器中压强不变 e. c(CO)= c(H2O)
(3)一定条件下的密闭容器中,反应达到平衡,要提高CO2的转化率,可以采取的措施是________(填序号)。
a.向体系中通入CO2 b.降低温度
c.向体系中通入惰性气体 d.向体系中通入H2 e.加入催化剂
(4)25℃时,已知: 2C(石墨) + O2 (g) = 2CO(g) △H1 = -222 kJ/mol
H2(g) + 1/2O2(g) = H2 O (g) △H2 = -242 kJ/mol
结合题中信息,写出石墨与氧气反应生成1mol CO2的热化学方程式
。
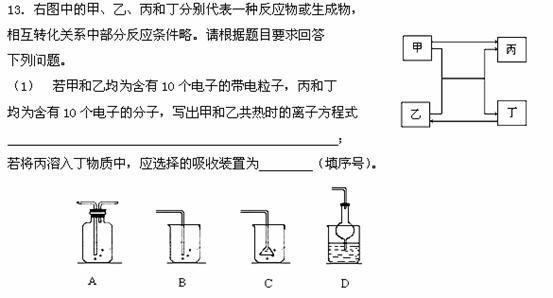
(2)若甲和乙均为含有18个电子的共价化合物,丁为黄色固体,
则甲的电子式为 ,甲中含有的化学键类型有 (填序号)。
A 离子键 B极性共价键 C 非极性共价键
(3)若甲是含有10个电子的化合物,乙是含有18个电子的单质分子,写出甲和乙反应的化学方程式 ;当乙发生反应时,转移0.1mol电子,则标况下有 L单质气体乙参加反应。
(4)若甲、乙均由两种元素组成,且含有一种相同元素,甲是含有10个电子的分子,乙是含有18个电子的分子,甲、乙发生化学反应的实验现象为
。 (5)若甲和丁为非金属单质,乙和丁为非金属氧化物,则甲和丁可能为
、
(5)若甲和丁为非金属单质,乙和丁为非金属氧化物,则甲和丁可能为
、
(列出常见的两组的名称)。
(6)若甲、乙中均含有常见金属元素,甲为单质,乙中两元素原子的质量比为21:8,则甲、乙发生反应的化学方程式为 。
11. 在400 ℃、101 kPa时,NO2(g)+CO(g) NO(g) + CO2(g)反应过程的能量变化如下图所示。
在400 ℃、101 kPa时,NO2(g)+CO(g) NO(g) + CO2(g)反应过程的能量变化如下图所示。
|
|
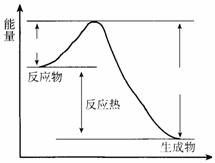
反应过程
(1)该反应是 (填“吸热”或“放热”)反应。
(2)该反应的热化学方程式为 。
(3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的
是 (填序号)。
|
a.浓度 |
b.压强 |
|
c.温度 |
d.催化剂 |
10. 一定条件下,对可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08
mol/L,则下列
一定条件下,对可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08
mol/L,则下列
判断不合理的是
A.c1:c2=1:3
B.平衡时,Y 和Z的生成速率之比为2:3
C.X、Y的转化率相等
D.c1的取值范围为0﹤c1﹤0.14 mol/L
 第Ⅱ卷 (非选择题 共60分)
第Ⅱ卷 (非选择题 共60分)
本卷共4小题,共60分。
9.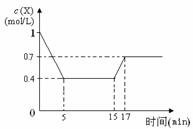
 一定条件下,向密闭容器中加入1 mol/L X发生反应:3X(g) Y(g) + Z(g) △H<0,反应到5min时达到平衡,在15min时改变某一条件,到17min时又建立新平衡,X的物质的量浓度变化如图,下列说法中不正确的是
一定条件下,向密闭容器中加入1 mol/L X发生反应:3X(g) Y(g) + Z(g) △H<0,反应到5min时达到平衡,在15min时改变某一条件,到17min时又建立新平衡,X的物质的量浓度变化如图,下列说法中不正确的是
A.0-5 min时,该反应的速率为v(X)=0.12 mol/(L·min)
B.15 min时改变的条件可能是减小压强
C.15 min时改变的条件可能是升高温度
D.从初始到17 min时,X的转化率为30 %
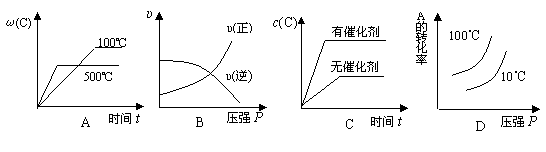
8.对于可逆反应:2A(g)+B(g)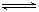 2C(g) △H<0,下列各图正确的是
2C(g) △H<0,下列各图正确的是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com