
题目列表(包括答案和解析)
13.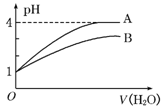 常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000
常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000
倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是
A.A酸比B酸的电离程度小 B. A是强酸,B是弱酸
C.B酸比A酸容易电离
D.pH=1时,B酸的物质的量浓度比A酸大
12.在由水电离产生的c(H+)=1×10-14mol·L-1的溶液中,一定可以大量共存离子组是
A.K+、Na+、SO42-、CO32- B. K+、Ba2+、Cl-、NO3-
C.Na+、Mg2+、Cl-、NO3- D. NH4+、Al3+、Br-、SO42-
11. 在一定条件下,有可逆反应2SO2(g) + O2(g) 2SO3 (g) ΔH < 0。当单独改变下列条件后,有关叙述中错误的是 A.体积不变,加入氩气,压强增大, v正、v逆都增大
在一定条件下,有可逆反应2SO2(g) + O2(g) 2SO3 (g) ΔH < 0。当单独改变下列条件后,有关叙述中错误的是 A.体积不变,加入氩气,压强增大, v正、v逆都增大
B.加入催化剂,v正、v逆都发生变化,且变化的倍数相同
C.压缩体积,增大压强时,v正、v逆都增大
D.降低温度时,v正、v逆都减小
10.下列式子书写正确的是
A.用FeCl3溶液腐蚀铜线路板:Cu + Fe3+ = Cu2+ + Fe2+
B.120℃时,1 mo1甲烷完全燃烧放出890.3kJ,则甲烷燃烧的热化学方程式可表示为:
CH4 + 2O2 = CO2 + 2H2O △H=-890.3kJ·mol-1
C.NH4Cl溶于水时的电离方程式:NH4Cl= NH4+ + Cl-
D.锌铜原电池负极的电极反应方程式:H+ + e- = H2↑
9.对于温度与反应方向的关系,下列判断一定不正确的是
A. △H<0 ,△S>0,所有温度下反应自发进行
B. △H<0 ,△S<0,低温下反应自发进行
C. △H>0 ,△S>0,所有温度下反应自发进行
D. △H>0 ,△S<0,所有温度下反应不能自发进行
8. 在一定温度下,某体积不变的密闭容器中,反应A2(g)+B2(g) 2AB(g)达到平衡的标志是
在一定温度下,某体积不变的密闭容器中,反应A2(g)+B2(g) 2AB(g)达到平衡的标志是
A.混合气体的密度不变
B.容器内的总压强不随时间变化
C.混合气体的平均摩尔质量不变
D.单位时间内生成2n mol的AB,同时生成n mol的B2
7.氯化钠是一种重要的化工原料。下列表述中正确的是
A.NaCl的电子式为
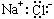 B.NaCl是强电解质
B.NaCl是强电解质
C.工业上把电解熔融氯化钠称之为氯碱工业
D.用侯氏制碱法制备纯碱时发生了氧化还原反应
6. 在N2+3H2 2NH3的平衡体系中,当分离出NH3时,下列说法正确的是
在N2+3H2 2NH3的平衡体系中,当分离出NH3时,下列说法正确的是
A.正反应速率增大 B.平衡向逆反应方向移动 C.正反应速率等于逆反应速率 D.氢气的转化率变大
5.在一支25 mL的酸式滴定管中盛入0.1 mo1·L-1 HCl溶液,其液面恰好在5 mL的刻度处。若把滴定管中的溶液全部放入锥形瓶中,然后以0.1 mo1·L-1NaOH溶液进行中和,则所需NaOH溶液的体积
A.等于20mL B.等于5mL C.大于20mL D.小于20mL
4.下列化学式能真实表示物质分子组成的是
A.SiO2 B.NaOH C.C60 D. C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com