
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
1ΓΔΖα12Θ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
AΘ°»τΥα–‘HA>HBΘ§‘ρœύΆ§ΧθΦΰœ¬Θ§»ή“ΚΒΡpH¥σ–ΓΈΣNaA>NaB
BΘ°œύΆ§ΧθΦΰœ¬Θ§ΫΪpH=11ΒΡNaOH»ή“ΚΚΆΑ±Υ°Ζ÷±πœΓ Ά≥…pH=9ΒΡ»ή“ΚΘ§ΥυΦ”Υ°ΒΡΧεΜΐ«Α’Ώ¥σ
CΘ°pH=3ΒΡ¥ΉΥα”κpH=11ΒΡNaOH»ή“ΚΒ»ΧεΜΐΜλΚœ ±Θ§»ή“Κ÷–άκΉ”≈®Ε»ΒΡ¥σ–ΓΥ≥–ρ «ΓΓ c(Na+)>c(CH3COO-) >c(OH-) >c(H+)
DΘ°0.1mol/LΒΡΡ≥Εΰ‘Σ»θΥα―ΈNa2A»ή“Κ÷–Θ§c(Na+)=2[c(HA‑)+c(A2-)+c(H2A)]
9ΓΔΈς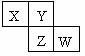 9Θ°XΓΔYΓΔZΓΔWΨυΈΣΕΧ÷ήΤΎ‘ΣΥΊΘ§ΥϋΟ«‘Ύ÷ήΤΎ±μ÷–œύΕ‘ΈΜ÷Ο»γΆΦΥυ ΨΓΘ»τY‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «ΡΎ≤ψΒγΉ” ΐΒΡ3±ΕΘ§œ¬Ν–ΥΒΖ®÷–¥μΈσΒΡ «
9Θ°XΓΔYΓΔZΓΔWΨυΈΣΕΧ÷ήΤΎ‘ΣΥΊΘ§ΥϋΟ«‘Ύ÷ήΤΎ±μ÷–œύΕ‘ΈΜ÷Ο»γΆΦΥυ ΨΓΘ»τY‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «ΡΎ≤ψΒγΉ” ΐΒΡ3±ΕΘ§œ¬Ν–ΥΒΖ®÷–¥μΈσΒΡ «
AΘ°‘≠Ή”ΑκΨΕΘΚW>Z>Y>X
BΘ°YΒΡΤχΧ§«βΜ·ΈοΒΡΈ»Ε®–‘ΫœZΒΡ«Ω
CΘ°WΒΡΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘ΫœZΒΡ«Ω
DΘ°ΥΡ÷÷‘ΣΥΊΒΡΒΞ÷ ÷–Θ§ZΒΡ»έΓΔΖ–ΒψΉνΗΏ
±±Ψ© –Ης≥««χΕΰΡΘΜ·―ß―Γ‘ώΧβΝΖœΑΝυ(ΒγΫβ÷ ΓΔΜ·―ßΤΫΚβ)
8ΓΔ≥γ5Θ°œ¬Ν–Έο÷ Ζ÷άκΙΐ≥Χ÷–…φΦΑΙ≤ΦέΦϋΕœΝ―ΒΡ «
AΘ°”Ο…χΈωΖ®≥ΐ»ΞΒμΖέΫΚΧε÷–ΒΡ…ΌΝΩNaCl
BΘ°”Ο±ΞΚΆ ≥―ΈΥ°œ¥»ΞCl2÷–ΒΡ…ΌΝΩHCl
CΘ°”ΟCCl4ίΆ»ΓΒβΥ°÷–ΒΡΒβ
DΘ°”Ο…ΐΜΣΖ®≥ΐ»ΞNaCl÷–Μλ”–ΒΡ…ΌΝΩΒβ
7ΓΔ≥·12Θ°œ¬±μΈΣ≤ΩΖ÷“Μ¬»¥ζΆιΒΡΫαΙΙΦρ ΫΚΆ“Μ–©–‘÷ ΐΨί
|
–ρΚ≈ |
ΫαΙΙΦρ Ϋ |
Ζ–Βψ/Γφ |
œύΕ‘ΟήΕ» |
|
ΔΌ |
CH3Cl |
Θ≠24.2 |
0.9159 |
|
ΔΎ |
CH3CH2Cl |
12.3 |
0.8978 |
|
Δέ |
CH3CH2CH2Cl |
46.6 |
0.8909 |
|
Δή |
CH3CHClCH3 |
35.7 |
0.8617 |
|
Δί |
CH3CH2CH2CH2Cl |
78.44 |
0.8862 |
|
Δό |
CH3CH2CHClCH3 |
68.2 |
0.8732 |
|
ΔΏ |
(CH3)3CCl |
52 |
0.8420 |
œ¬Ν–Ε‘±μ÷–Έο÷ ”κ ΐΨίΒΡΖ÷ΈωΙιΡ…¥μΈσΒΡ «
A.ΓΓΓΓ Έο÷ ΔΌΔΎΔέΔίΜΞΈΣΆ§œΒΈο
B.ΓΓΓΓΓΓ “Μ¬»¥ζΆιΆ§Ζ÷“λΙΙΧεΒΡΖ–ΒψΥφΉ≈÷ßΝ¥ΒΡ‘ωΕύΕχ…ΐΗΏ
C.ΓΓΓΓΓΓ “Μ¬»¥ζΆιΒΡΖ–ΒψΥφΉ≈ΧΦ ΐΒΡ‘ωΕύΕχ«ς”Ύ…ΐΗΏ
D.ΓΓΓΓ “Μ¬»¥ζΆιΒΡœύΕ‘ΟήΕ»ΥφΉ≈ΧΦ ΐΒΡ‘ωΕύΕχ«ς”ΎΦθ–Γ
6ΓΔ≥· 8Θ°ΥΡ÷÷‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–œύΕ‘ΈΜ÷ΟΈΣΓΓ Τδ÷–WΒΡ“Μ÷÷‘≠Ή” «3618WΘ§‘ρœ¬Ν–≈–Εœ¥μΈσΒΡ «
AΘ°‘≠Ή”ΑκΨΕXΘΦYΘΦZ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓBΘ°ΤχΧ§«βΜ·ΈοΈ»Ε®–‘XΘΨYΘΨZ
CΘ° ΤχΧ§«βΜ·ΈοΜΙ‘≠–‘XΘΨYΘΨZΓΓΓΓΓΓ DΘ°ΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΒΡΥα–‘XΘΨYΘΨZ
5ΓΔ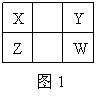 ΚΘ7Θ°“―÷ΣXΓΔYΓΔZΓΔWΥΡ÷÷ΕΧ÷ήΤΎ‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΒΡœύΕ‘ΈΜ÷Ο»γΆΦ1Υυ ΨΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓ
ΚΘ7Θ°“―÷ΣXΓΔYΓΔZΓΔWΥΡ÷÷ΕΧ÷ήΤΎ‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΒΡœύΕ‘ΈΜ÷Ο»γΆΦ1Υυ ΨΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓ
AΘ°Z‘ΣΥΊΒΡ‘≠Ή”ΑκΨΕΩ…Ρή±»Y‘ΣΥΊΒΡ–Γ
BΘ°Z‘ΣΥΊΒΡΉνΗΏΜ·ΚœΦέΩ…Ρή±»Y‘ΣΥΊΒΡΗΏ
CΘ°WΒΡΤχΧ§«βΜ·ΈοΒΡΈ»Ε®–‘“ΜΕ®±»YΒΡ«Ω
DΘ°ZΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·ΈοΒΡΥα–‘“ΜΕ®±»WΒΡ«Ω
4ΓΔ–ϊ9Θ°”“±μΈΣ‘ΣΥΊ÷ήΤΎ±μ«ΑΥΡ÷ήΤΎΒΡ“Μ≤ΩΖ÷Θ§œ¬Ν–”–ΙΊRΓΔWΓΔXΓΔYΓΔZ Έε÷÷‘ΣΥΊΒΡ–π ω÷–Θ§’ΐ»ΖΒΡ «
AΓΓ ≥Θ―Ιœ¬Έε÷÷‘ΣΥΊΒΡΒΞ÷ ÷–WΒΞ÷ ΒΡΖ–ΒψΉνΗΏ
BΓΓ YΓΔZΚΆWΒΡ“θάκΉ”ΑκΨΕ“ά¥Έ‘ω¥σCΓΓ XΒΡ«βΜ·Έο±»Ά§Ήε‘ΣΥΊΒΡ«βΜ·ΈοΒΡΖ–ΒψΒΆ
DΓΓ Z‘ΣΥΊΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·ΈοΥα–‘Ήν«Ω
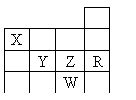
3ΓΔΖα11Θ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
AΘ°÷Μ”–Ζ«Ϋπ τΡή–Έ≥…Κ§―θΥαΚΆΚ§―θΥα―ΈBΘ°ΔωAΉε‘ΣΥΊΒΡ«βΜ·Έο÷–Έ»Ε®–‘ΉνΚΟΒΡΘ§ΤδΖ–Βψ“≤ΉνΗΏ
 CΘ°Ά§“Μ÷ςΉεΒΡ‘ΣΥΊΘ§‘≠Ή”ΑκΨΕ‘Ϋ¥σΤδΒΞ÷ ΒΡ»έΒψ‘ΫΗΏ
CΘ°Ά§“Μ÷ςΉεΒΡ‘ΣΥΊΘ§‘≠Ή”ΑκΨΕ‘Ϋ¥σΤδΒΞ÷ ΒΡ»έΒψ‘ΫΗΏ
DΘ°≥ΐœΓ”–ΤχΧεΆβΒΡΖ«Ϋπ τ‘ΣΥΊΘ§ΕΦΡή–Έ≥…≤ΜΆ§ΦέΧ§ΒΡΚ§―θΥα
2ΓΔΖα6Θ°œ¬Ν––π ω÷–Θ§’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
AΘ°Εΰ―θΜ·ΙηΚΆΗ…±υΨßΧε»έΜ· ±ΥυΩΥΖΰΒΡΉς”ΟΝΠάύ–ΆœύΆ§
BΘ°Ζ÷Ή”ΨßΧε÷–“ΜΕ®Κ§”–Ι≤ΦέΦϋΘ§άκΉ”ΨßΧε÷–“ΜΕ®Κ§”–άκΉ”Φϋ
CΘ°άκΉ”ΨßΧεΕΦ ««ΩΒγΫβ÷
DΘ°Φλ―ιΒμΖέ «Ζώ“―Ψ≠»Ϊ≤ΩΥ°Ϋβ ±ΓΔΩ…»Γ…ΌΝΩ―υΤΖΘ§œρΤδ÷–Φ”»κ“χΑ±»ή“ΚΘ§Υ°‘ΓΦ”»»Θ§»τΡή…ζ≥…“χΨΒΥΒΟςΒμΖέ“―Ψ≠»Ϊ≤ΩΥ°Ϋβ
1ΓΔΕΪ9Θ°ΕΧ÷ήΤΎ‘ΣΥΊAΓΔBΓΔC‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§AΓΔCΆ§÷ςΉεΘ§B‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐΒ»”ΎA‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐΒΡ“ΜΑκΘ§«“»ΐ÷÷‘ΣΥΊ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ÷°ΚΆΈΣ15ΓΘœ¬Ν––π ω’ΐ»ΖΒΡ «
AΘ°≥ΘΈ¬œ¬BΒΞ÷ ≤Μ”κAΒΞ÷ Ζ¥”ΠΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°ΙΛ“Β…œ≤…”Ο»»ΜΙ‘≠Ζ®“±ΝΕB
CΘ°AΒΡ«βΜ·ΈοΒΡΖ–ΒψΗΏ”ΎCΒΡ«βΜ·ΈοΓΓΓΓ DΘ°BΒΡ―θΜ·Έο÷ΜΡή»ή”ΎΥα
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com