
5.关于晶体的下列说法正确的是
A.任何晶体中,若含有阳离子就一定有阴离子。
B.原子晶体中只含有共价键。
C.原子晶体的熔点一定比金属晶体的高。
D.离子晶体中只含有离子键,不含有共价键。
4.电子排布在同一能级时,总是
A.优先单独占据不同轨道,且自旋方向相同
B.优先单独占据不同轨道,且自旋方向相反
C.自由配对,优先占据同一轨道,且自旋方向相同
D.自由配对,优先占据同一轨道,且自旋方向相反
3.下列分子中,既含有极性键又含有非极性键的是
A.CO2 B.H2O C.Br2 D.H2O2
2.元素电负性随原子序数的递增而增强的是
A.Na, K, Rb B.N, P, As C.O, S, Cl D.Si, P, Cl
1.以下能级符号不正确的是
A.3s B.3p C.3d D.3f
22.(10分)
(1)请结合水的结构与性质,回答以下关于水的问题:
①水分子在特定条件下容易结合一个H+形成水合氢离子(H3O+),该过程中所形成的共价键为 (选填下面选项序号)。
A.极性键 B.非极性键 C.配位键 D.氢键
在H3O+中,3个O-H键是 (填完全相同、不相同)的。
②给水施加一个弱电场,可使其在常温常压下结冰,称为“热冰”。下列物质熔化时,克服的微粒间的作用与“热冰”熔化时所克服的作用类型完全相同的是
A.金刚石 B.干冰 C.食盐 D.固态氨
(2)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。则体心立方晶胞和面心立方晶胞中实际含有的铁原子个数之比为 ,铁原子的配位数(与一个原子等距离且距离最近的原子数)之比为 。
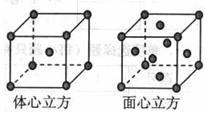
(3)超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛,AlN晶体与金刚石类似(其晶胞结构如右图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内),每个Al原子与 个N原子相连,与同一个Al原子相连的N原子构成的空间构型为 。
(4)AlN样品中常含有碳和A12O3杂质,为测定AlN的质量分数,称取10.00 g样品,加入足量的NaOH溶液,生成NaAlO2和NH3,生成的NH3恰好被75 mL 1 mol/L-1硫酸溶液吸收为硫酸铵。则样品中AlN的质量分数= 。
20.(7分)
一定温度下,在容积为2 L的密闭容器中通入一定量的气体A发生反应,A和生成物B(气体)的物质的量随时间变化的曲线如下图所示。
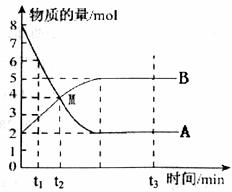
(1)此反应的化学方程式为
(2)tl到t2时刻,以A的浓度变化表示的平均反应速率为:
(3)下列叙述中能说明上述反应达到平衡状态的是 ;(选填编号)
A.反应中A与B的物质的量之比为1:1 (即图中M点)
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1 molA,同时生成2 mol B
D.A的质量分数在混合气体中保持不变
19.(10分)
用酸性氢氧燃料电池电解饱和氯化钠溶液的装置如下图所示(a、b为石墨电极)。下列说法中正确的是
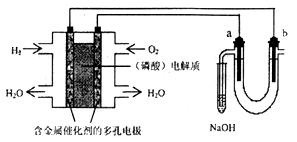
(1)燃料电池是利用燃料和氧化剂之间发生的氧化还原反应,将 能直接转化为 能的化学电源。该电池工作时,正极反应式为: 。
(2)电解时,b电极为 极,产生的气体为 (写化学式)。
(3)试管中NaOH的作用为(用离子方程式表示): 。
(4)忽略能量损耗,当电池中消耗0.02 g H2 时,电解池中会产生 g H2。
18.(8分)
“西气东输”是西部开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,二者的体积比为l:l。已知1 mol CO气体完全燃烧生成CO2气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量;l mol CH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学方程式
(2)若l mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量 890 kJ。(填>、=、<)
(3)忽略水煤气中其他成分,燃烧等体积的甲烷和水煤气,所得热量之比约为 。
(4)请依据以上数据和计算结果,说出以天然气代替水煤气作为燃料的两个优点:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com