
5. 若AgOH是强碱,则AgOH(aq) Ag+ + OH–完全电离,所以只要测饱和AgOH溶液的pH值就可以决定AgOH是强碱还是弱碱。从Ksp可知,[OH–] = 10–4,即pH = 10,若测得pH = 10就是强碱,若测得pH < 10,则为弱碱。
4. HCl + HAc H2Ac+ + Cl– (HAc中) ∴ [HAc] ≡ c
K = [H2Ac+][Cl–]/[HCl] 且[H2Ac+] ≈ [Cl–]
∴ [H2Ac+] ≈ [Cl–] = {K·[HCl]}1/2
= (2.8×10–9×1.0×10–4)1/2 = 5.29×10–7 (mol∙dm–3)
又由于[H2Ac+][Ac–] = 3.6×10–15
∴ [Ac–] = 3.6×10–15/5.29×10–7 = 6.80×10–9 (mol∙dm–3)
3. 2H2SO4(l) H3SO4+ + HSO4–
K = [H3SO4+][HSO4–]、且[H3SO4+] = [HSO4–],[H2SO4](l) ≡常数,
∴ [H3SO4+]=[HSO4–] = (2.8×10–4)1/2 = 1.67×10–2 (mol·dm–3)
2. (1) BF3、酸: HF + BF3 HBF4 H+ + BF4–
(2) SbF5、酸: HF + SbF5 HSbF6 H+ + SbF6–
(3) H2O、碱:HF + H2O H3O+F– H3O+ + F–
(4) CH3COOH、碱: CH3COOH + HF CH3COOH2+ + F–
(5) C6H6、碱: + HF + F–
1. (1) H2CrO4 (HO)2CrO2 m = 2, pK1 = –3
(2) HBrO4 (HO)BrO3 m = 3, pK1 = –8
(3) HClO (HO)Cl m = 0, pK1 = 7
(4) H5IO6 (HO)5IO m = 1, pK1 = 2
(5) HSO3F (HO)SO2F m = 3, pK1 = –8
(6) H3AsO4 (OH)3AsO m = 1, pK1 = 2
5. (1)
Pb + PbO2 + 4H+ + 2SO42–  2PbSO4
+ 2H2O
2PbSO4
+ 2H2O
负极: Pb + SO42– – 2e  PbSO4
PbSO4
正极: PbO2 + 4H+ + SO42– + 2e
 PbSO4
+ 2H2O
PbSO4
+ 2H2O
(2) Li + LiMn2O4  Li2Mn2O4
Li2Mn2O4
负极: Li – e  Li+
Li+
正极: LiMn2O4 + Li+ + e  Li2Mn2O4
Li2Mn2O4
(3) 锂离子占有O2–离子围成的正四面体空隙,所以配位数是4;锰离子占有O2–离子围成的正八面体空隙,所以配位数为6。
4. (1)
PdCl2·2H2O + CO  Pd* +
CO2 + 2HCl + H2O
Pd* +
CO2 + 2HCl + H2O
(*由于还原出来的Pd颗粒很小,可以完全吸收可见光,所以呈黑色)
(2) Pd + 2CuCl2·2H2O
 PdCl2·2H2O
+ 2CuCl + 2H2O
PdCl2·2H2O
+ 2CuCl + 2H2O
(3) 4CuCl + O2 + 4HCl +
6H2O  4CuCl2·2H2O
4CuCl2·2H2O
3. (1) Ag2Se
4AgCl + 3Se + 6NaOH  2Ag2Se↓
+ Na2SeO3 + 4NaCl+ 3H2O
2Ag2Se↓
+ Na2SeO3 + 4NaCl+ 3H2O
(2) 溶于水的物质有Na2SeO3、NaCl以及过量的NaOH和Na2Se。
(3) 由于Se过量,所以生成的Na2Se过量,当AgCl完全转化成Ag2Se后,还有Na2Se剩余,而3Se+ 6NaOH  2Na2Se
+ Na2SeO3+ 3H2O,因此A中(Ag2Se)的Se不足原料中的2/3。
2Na2Se
+ Na2SeO3+ 3H2O,因此A中(Ag2Se)的Se不足原料中的2/3。
2.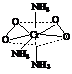 (1) Cr : N : H : O(原子个数比)= (31.1/53.00) : (25.1/14.00)
: (5.4/1.008) : (38.4/16.00)=1 : 3 : 9 : 4,A的化学式为CrO4(NH3)3。
(1) Cr : N : H : O(原子个数比)= (31.1/53.00) : (25.1/14.00)
: (5.4/1.008) : (38.4/16.00)=1 : 3 : 9 : 4,A的化学式为CrO4(NH3)3。
A的一种可能的结构式如右图所示。
(2) +4;
(3)不稳定;
(4) (NH4)2CrO4
+ 3H2O2 + NH3  CrO4(NH3)3
+ O2 + 4H2O
CrO4(NH3)3
+ O2 + 4H2O
1. (1)
CuH [注:这是因为纤维矿ZnS中Zn : S = 1 :
1,∴中Cu : H也应该1 : 1。CuH也可以用4CuI + LiAlH4 4CuH + LiI + AlI3来制备。]
4CuH + LiI + AlI3来制备。]
(2) 4CuSO4 + 3H3PO2
+ 6H2O  4CuH + 3H3PO4
+ 4H2SO4
4CuH + 3H3PO4
+ 4H2SO4
(3) 2CuH + 3Cl2  2CuCl2
+ 2HCl
2CuCl2
+ 2HCl
(4) CuH + 2HCl  HCuCl2
+ H2
HCuCl2
+ H2
(若不是浓盐酸,则2CuH + 2HCl  CuCl2
+ Cu + 2H2)
CuCl2
+ Cu + 2H2)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com