
21.某化学兴趣小组的课题是测定工业产品氯化铵的纯度(假定其杂质不与甲醛发生反应),其测定拟采用“甲醛法”,反应离子方程式为:4NH4++6HCHO→(CH2)6N4+4H++6H2O。现称取1.5g该样品溶于水,加入足量的甲醛溶液,然后加水配成100 mL溶液。取出10 mL,滴入酚酞后再逐滴滴入0.1 mol/L的NaOH溶液,当滴到25 mL时溶液呈粉红色,且在半分钟内不褪色,则该样品中氯化铵的质量分数是
A.65% B.78.2% C.89.2% D.92.3%
20. 将 CaCl2和CaBr2的混合物13.400g溶于水配成500.00mL溶液,再通入过量的Cl2,完全反应后将溶液蒸干,得到干燥固体11.175g。则原配溶液中,c(Ca2+)∶c(Cl-)∶c(Br‑)为
A.3∶2∶1 B.1∶2∶3 C.1∶3∶2 D.2∶3∶1
18.下列各组溶液,不用其它试剂就可以区别开的是
A.氯化钠 盐酸 偏铝酸钠 氢氧化钠
B.氯化钡 硫酸钠 硝酸钾 硫酸铵
C.盐酸 硝酸 氯化钾 碳酸钠
D.氯化钡 氯化钠 氢氧化钠 硫酸钠
|

A.30%
B.100% C.26.5%
D.---------×100%
|

17.下列离子方程式正确的是
A.硫酸氢钠溶液滴加氢氧化钡溶液至中性:Ba2++OH
-+H++SO42-=BaSO4↓+H2O
B.明矾与氢氧化钡反应得沉淀质量最大:
Al3++3SO42-+3Ba2++6OH-=Al(OH)3↓+3BaSO4↓
C.碘化亚铁溶液加氯水恰好将Fe2+全部氧化:2Fe2++4I-+3Cl2=2Fe3++6Cl-+2I2
D.磷酸二氢钠溶液加过量Ca(OH)2溶液:
3H2PO4-+3Ca2++6OH-=Ca3(PO4)2↓+PO43-+6H2O
16.在c(HCO3-) = 0.1mol·L-1的溶液中,可以大量共存的离子组是
A.Al3+、NO3-、NH4+、C1- B.Na+、SO42-、K+、CH3COO-
C.H+、Ba2+、Cl-、NO3- D.C1-、CO32-、Na+、OH -
15..实验室制取下列物质的方案不可能达到目的是
A.用生锈的废钢铁与稀H2SO4反应制绿矾 B.用碳酸钠与稀H2SO4反应制CO2
C.用食盐、二氧化锰和浓H2SO4共热制Cl2 D.用FeS和浓H2SO4反应制H2S
14.下列做法正确的是
A.将浓硝酸保存在无色玻璃瓶中 B.用镊子取出白磷并置于水中切割
C.把氯酸钾制氧气后的残渣倒入垃圾桶 D.氢气还原氧化铜实验先加热再通氢气
13.右图是气体制取装置,下列能用此装置制取气体并能“随开随用、随关随停”的是
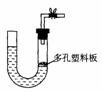 A.大理石和稀硫酸制取二氧化碳 B.锌粒和稀硫酸制氢
A.大理石和稀硫酸制取二氧化碳 B.锌粒和稀硫酸制氢
C.浓盐酸和二氧化锰制取氯气
D.电石和水制取乙炔
12.下列实验中,溶液颜色有明显变化的是
A.少量明矾溶液加入到过量NaOH溶液中
B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C.少量Na2O2固体加入到过量NaHSO3溶液中
D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
11.下列有关化学实验的叙述正确的是
A.用待测液润洗滴定用的锥形瓶
B.配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸
C.用稀盐酸洗涤盛放过石灰水的试剂瓶
D.Na2CO3溶液保存在带玻璃塞的试剂瓶中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com