
8ЃЎГЃЮТЪБЃЌНЋVlmLC1molЁЄLЃ1ЕФАБЫЎЕЮМгЕНV2mLC2molЁЄLЃ1бЮЫсжаЃЌЯТЪіНсТлжае§ШЗ
ЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ( )
ЁЁЁЁ AЃЎШєЛьКЯШмвКЕФpH=7ЃЌдђC1V1>C2V2
BЃЎШєVl=V2ЃЌC1=C2дђЛьКЯвКжаc(NH4+)=c(Cl-)
ЁЁЁЁЁЁ CЃЎШєЛьКЯвКЕФpH=7ЃЌдђЛьКЯвКжаc(NH4+)>c(ClЃ)
ЁЁЁЁЁЁ DЃЎШєV1=V2ЃЌЧвЛьКЯвКЕФpH<7ЃЌдђ-ЖЈгаC1<C2
7ЃЎжаКЭвЛЖЈСПЕФФГжжДзЫсШмвККФagNaOHЁЃШєЯШдкИУДзЫсШмвКжаШмШыЩйСПCH3COONaЃЌдйгУNaOHжаКЭЕЮЖЈЃЌКФbgNaOHЁЃдђaКЭbЕФЙиЯЕЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ )
AЃЎ a>bЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ a<bЁЁЁЁЁЁ ЁЁЁЁ CЃЎ a=bЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁ DЃЎ ЮоЗЈШЗЖЈ
6ЃЎгУЮяжЪЕФСПХЈЖШЮЊ0.1mol/LЕФбЮЫсКЭДзЫсШмвКЃЌЗжБ№жаКЭЕШЬхЛ§pH=12ЕФЧтбѕЛЏФЦШмвКЃЌЕБЧтбѕЛЏФЦЧЁКУБЛЭъШЋжаКЭЪБЃЌЯћКФбЮЫсКЭДзЫсШмвКЕФЬхЛ§ЪЧV1КЭV2ЃЌдђV1КЭV2ЕФЙиЯЕе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ )
ЁЁЁЁЁЁ AЃЎV1<V2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎV1=V2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎV1>V2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎV1ЁмV2
5ЃЎЯТСаШмвКвЛЖЈМюадЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ (ЁЁЁЁ )
ЁЁЁЁ AЃЎШмвКжаc(OH-)>c(H+)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎШмвКжаКЌгаOH‑Рызг
CЃЎЕЮМгМзЛљГШКѓШмвКЯдКьЩЋЁЁЁЁЁЁЁЁЁЁ DЃЎЕЮМгМзЛљГШКѓШмвКЯдЛЦЩЋ
4ЃЎгУ0.1mol/LЕФNaOHШмвКЕЮЖЈ100mL0.1mol/LбЮЫсЪБЃЌШчЙћЕЮЖЈЮѓВюдкЁР0.1%вдФкЃЌЗДгІЭъБЯКѓЃЌШмвКЕФpHЗЖЮЇЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ )
ЁЁЁЁ AЃЎ6.9-7.1ЁЁЁЁЁЁ ЁЁ BЃЎ3.3-10.7 ЁЁЁЁЁЁ CЃЎ4.3-9.7ЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ6-8
3ЃЎгавЛжЇ50mLЫсЪНЕЮЖЈЙм,ЦфжаЪЂгаШмвК,вКУцЧЁКУдк10.0mLПЬЖШДІ.АбЕЮЖЈЙмжаЕФШмвКЁЁ
ЁЁ ШЋВПСїЯТХХГі,ГаНгдкСПЭВжа,СПЭВФкШмвКЕФЬхЛ§ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ( )
ЁЁ AЃЎДѓгк40.0mL ЁЁЁЁЁЁ BЃЎЮЊ40.0mLЁЁЁЁЁЁЁЁЁЁ CЃЎаЁгк40.0mL ЁЁЁЁ DЃЎЮЊ10.0mL
2ЃЎЯТСаМИжжЧщПіЖджаКЭЕЮЖЈНсЙћЮогАЯьЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ )
AЃЎЪЂД§ВтвКЕФзЖаЮЦПРяСєгаеєСѓЫЎЁЁЁЁ
BЃЎЕЮЖЈЙмМтзьВПЗждкЕЮЖЈЧАгаЦјХн
CЃЎЕЮЖЈЙмдкЕЮЖЈЧАЮДНЋПЬЖШЕїдкЁА0ЁБЃЌЖјЕїдкЁА2.40ЁБ
DЃЎ ЕЮЖЈДяжеЕуЪБЃЌЪгЯпИпгкЕЮЖЈЙмФквКЬхЕФАМУцЕФзюЕЭЕу
1ЃЎгУБъзМбЮЫсШмвКЕЮЖЈЮДжЊХЈЖШЕФNaOHШмвКЪБ,ШєВтЕУНсЙћЦЋИп,дђВњЩњЮѓВюЕФдвђПЩФмЪЧ
AЃЎЕЮЖЈЪБ,зАЮДжЊХЈЖШNaOHШмвКЕФзЖаЮЦПЭќМЧгУNaOHШмвКШѓЯД
BЃЎЫсЪНЕЮЖЈЙмгУеєСѓЫЎЯДИЩОЛКѓ, ЭќМЧгУБъзМбЮЫсШѓЯД
CЃЎЕЮЖЈЪБ,ЕЮЖЈЙмЕФМтзьДІгаЦјХн,ЖјдкЕЮЖЈКѓЦјХнЯћЪЇ
ЁЁЁЁ DЃЎЕЮЖЈЧАвдбіЪгЕФзЫЪЦЖСШЁСЫЫсЪНЕЮЖЈЙмЕФЖСЪ§,ЕЮЖЈКѓЖСЪ§е§ШЗ
6ЁЂЮѓВюЗжЮі(жиЕугыФбЕу)
Р§ШчЃЌгУвбжЊХЈЖШЕФбЮЫсЕЮЖЈЮДжЊХЈЖШЕФNaOHШмвКЁЃ
cЫсVЫс==cМюVМюЁЁЁЁ
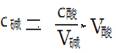
ЪНжаЃКcЫсЮЊБъзМШмвКЕФзМШЗХЈЖШ(ВЛБфСП)ЃЌVМюЮЊД§ВтвКЕФЬхЛ§(ВЛБфСП)ЁЃ
ЯдШЛЃЌгАЯьNaOHШмвКХЈЖШЕФвђЫиЪЧБъзМШмвКЕФЬхЛ§ЖСЪ§ЃЌШєЯћКФБъзМШмвКБШРэТлжЕЖрЃЌдђВтЖЈНсЙћЦЋИпЃЛШєЯћКФБъзМШмвКБШРэТлжЕЩйЃЌдђВтЖЈНсЙћЦЋЕЭЁЃМђЛЏЮЊЁАЖрдђИпЃЌЩйдђЕЭЁБЁЃ
жаКЭЕЮЖЈЙ§ГЬжаЃЌШнвзВњЩњЮѓВюЕФ6ИіЗНУцЪЧЃК
ЂХЯДЕгвЧЦїЃК(ЕЮЖЈЙмЁЂвЦвКЙмЁЂзЖаЮЦП)ЃЛ
ЂЦЦјХнЃЛ
ЂЧЬхЛ§ЖСЪ§(біЪгЁЂИЉЪг)ЃЛ
ЂШжИЪОМСбЁдёВЛЕБЃЛ
ЂЩдгжЪЕФгАЯьЃЛ
ЂЪВйзї(ШчгУСІЙ§УЭв§Ц№Д§ВтвКЭтМњЕШ)ЁЃ
ОпЬхЗжЮіШчЯТ:
ЂХЕЮЖЈЧАЃЌдкгУеєСѓЫЎЯДЕгЕЮЖЈЙмКѓЃЌЮДгУHClБъзМШмвКШѓЯДЫсЪНЕЮЖЈЙмОЭзАвКНјааЕЮЖЈЁЃ
ЂЦЕЮЖЈЧАЃЌгаЦјХнЃЌЕЮЖЈКѓЦјХнЯћЪЇЁЃ
ЂЧЕЮЖЈЧАЃЌгУД§ВтвКШѓЯДзЖаЮЦПЁЃ
ЂШШЁД§ВтвКЪБЃЌвЦвКЙмгУеєСѓЫЎЯДЕгКѓЃЌЮДгУД§ВтвКШѓЯДЁЃ
ЂЩШЁвКЪБЃЌвЦвКЙмМтЖЫЕФВаСєвКДЕШызЖаЮЦПжаЁЃ
ЂЪЖСШЁБъзМвКЕФПЬЖШЪБЃЌЕЮЖЈЙмПЊЪМЧАЦНЪгЖСЪ§ЃЌЕЮЖЈжеСЫЪБИЉЪгЖСЪ§ЁЃ
ЂЫШєгУМзЛљГШзїжИЪОМСЃЌзюКѓвЛЕЮбЮЫсЕЮШыЪЙШмвКгЩГШЩЋБфЮЊКьЩЋЁЃ
ЂЬЕЮЖЈЙ§ГЬжаЃЌзЖаЮЦПеёЕДЬЋОчСвЃЌгаЩйСПШмвКНІГіЁЃ
ЂЭЕЮЖЈКѓЃЌЕЮЖЈЙмМтЖЫЙвгавКЕЮЮДЕЮШызЖаЮЦПжаЁЃ
ЂЮЕЮЖЈЙмПЊЪМЧАбіЪгЖСЪ§ЃЌЕЮЖЈжеСЫЪБИЉЪгЖСЪ§ЁЃ
ЂЯЕЮЖЈЙ§ГЬжаЃЌЯђзЖаЮЦПжаМгШыЩйСПеєСѓЫЎЁЃ
ЂаЕЮЖЈЙ§ГЬжаЃЌЕЮЖЈЙмТЉвКЁЃ
ЂбЕЮЖЈСйНќжеЕуЪБЃЌгУЯДЦПжаЕФеєСѓЫЎЯДЯТЕЮЖЈЙмМтзьПкЕФАыЕЮБъзМШмвКжСзЖаЮЦПжаЁЃ
ЂвЙ§дчЙРМЦЕЮЖЈжеЕуЁЃ
ЂгЙ§ЭэЙРМЦЕЮЖЈжеЕуЁЃ
ЂдвЛЕЮБъзМШмвКИНдкзЖаЮЦПБкЩЯЮДЯДЯТЁЃ
ЂХЦЋИпЂЦЦЋИпЂЧЦЋИпЂШЦЋЕЭЂЩЦЋИпЂЪЦЋЕЭЂЫЦЋИпЂЬЦЋЕЭЂЭЦЋИпЂЮЦЋЕЭЂЯЮогАЯьЂаЦЋИп
ЂбВйзїе§ГЃЃЌЮогАЯьЂвЦЋЕЭЂгЦЋИпЂдЦЋИп
зЈЬтбЕСЗ
5ЁЂЖСЪ§гыМЧТМЁЁ
ЕЮЖЈЙмЕФЁА0ЁБПЬЖШдкЩЯЖЫ(гыСПЭВЯрЗД)ЃЌЖСЪщЪБЃЌЪгЯпЦНЪгЃЌВЛФмбіЪгЛђИЉЪгЁЃМЧТМЪ§ОнвЊгыЪЕбщЬѕМўЕФОЋШЗЖШвЛжТ(Шч12.5mL).вЊЧѓАбЭЌвЛбљЦЗЕЮЖЈСНДЮЃЌШЁСНДЮВтЖЈЪ§ОнЕФЦНОљжЕМЦЫуНсЙћЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com