
9.一个原电池的某极反应式为:Fe – 2e- = Fe2+,该原电池材料及电解质溶液可能是( )
|
|
A |
B |
C |
D |
|
正极 |
Fe |
Fe |
C |
Cu |
|
负极 |
Cu |
Zn |
Fe |
Fe |
|
电解质溶液 |
HCl |
CuSO4 |
CuSO4 |
Fe2(SO4)3 |
8.在指定环境中,下列各组离子一定可以大量共存的是 ( )
A.使pH试纸呈红色的溶液中:Fe2+、C1-、SO42-、Na+
B.在pH=10的溶液中:Na+、NO3-、C1-、Al3+
C.某溶液中由水电离生成的c(H+)=10-12 mol/L:CO32-、SO42-、C1-、Na+
D.加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42-
7.下列关于阿伏加德罗常数(NA)说法正确的是: ( )
A.乙烯和丙烯的混合物28g,含有碳原子的个数2NA
B.1摩尔氯气与足量的氢氧化钠反应,共转移了NA 的电子
C.在标准状况下,22.4L的己烷,含有6 NA碳原子
D.1mol/L的Na2S溶液中,含有的S2-的物质的量小于1 mol
6.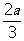 已知1-18号元素的离子aW3+、bX+、cY2-、dZ- 都具有相同电子层结构,下列关系正确的是 ( )
已知1-18号元素的离子aW3+、bX+、cY2-、dZ- 都具有相同电子层结构,下列关系正确的是 ( )
A.离子的还原性:Y2->Z- B.质子数:c>b
C.氢化物的稳定性:H2Y>HZ D.原子半径:X<W
5.向水中加入下列物质,其中能使水的电离程度增大的物质是: ( )
A.HCl B.NaOH B.NH4Cl D.NaCl
4.在3S + 6KOH = 2K2S + K2SO3 + 3H2O反应中,作氧化剂的S原子与作还原剂的S原子的物质的量之比是 ( )
A.1∶2 B.2∶1 C.1∶3 D.3∶1
3.下列说法正确的是 ( )
A.乙烯分子中碳碳双键键能是乙烷分子中碳碳单键键能的两倍,因此结构稳定
B.除去乙醇中的微量水可加入金属钠,使其完全反应
C.用苯可以萃取溴水中的溴,分液时有机层从下端放出。
D.可用饱和Na2CO3溶液出去乙酸乙酯中混有的乙酸和乙醇。
2.下列实验数据记录正确的是 ( )
A.用天平称取4.0克NaOH固体,用100ml量筒配制1.0000mol/L的NaOH溶液
B.用25mL的滴定管(内装有标准碱液)滴定未知浓度的酸用去碱液22.32mL
C.用pH试纸测得新制氯水的pH为4
D.常温下,用气球收集500mlNO2气体,求得NO2气体的物质的量为0.5/22.4mol
1.最近媒体报道了一些化学物质,如:爆炸力极强的N5、比黄金还贵的18O2、太空中的甲醇气团等。下列说法中,正确的是 ( )
A.18O2和16O2是两种不同的核素
B.甲醇(CH3OH)属于离子化合物
C.N5分子中含有极性共价键
 D.2 N5 5 N2 是化学变化
D.2 N5 5 N2 是化学变化
(二)选考题:共45分。请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。如果多做,则每学科按所做的第一题计分。
33.[物理--选修3-3](15分)
(1)以下说法正确的是 ( )
A.当分子间距离增大时,分子问作用力减小,分子势能增大
B.已知某物质的摩尔质量为M,密度为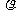 ,阿伏加德岁常数为M,则该种物质的分子体积为
,阿伏加德岁常数为M,则该种物质的分子体积为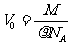
C.自然界发生的一切过程能量都是守恒的,符合能量守恒定律的宏观过程都能自然发
生
D.液品既具有液体的流动性,又具有单晶体的光学各向异性的特点
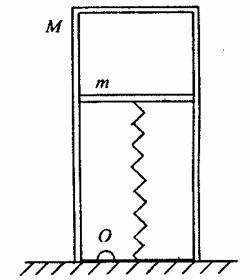
(2)一气缸竖直放在水平地面上,缸体质量M-10kg,活塞质量m=4kg,活塞横截面积S=2×10-3m2.活塞上面的气缸里封闭了一定质量的理想气体,下面有气孔O与外界相通,大气压强P0=1.0×105Pa。活塞下面与劲度系数k=2×103N/m的轻弹簧相连。当气缸内气体温度为127℃时弹簧为自然长度,此时缸内气柱长度L1=20cm,g取10m/s2,活塞不漏气且与缸壁无摩擦。
(i)当缸内气柱长度L2=24cm时,缸内气体温度为多少开?
(ii)缸内气体温度上升到瓦以上,气体将做等压膨胀,则T0为多少开?
34.[物理--选修3-4](15分)
(1)下列说法中正确的是 ( )
A.光传播时,若遇到的障碍物的尺寸比光的波长大很多,衍射现象十分明显,此时不
能认为光沿直线传播
B.在太阳光照射下,水面上油膜出现彩色花纹是光的色散现象
C.光导纤维丝内芯材料的折射率比外套材料的折射率大
D.麦克斯韦提出电磁场理论并预言电磁波存在,后来他又用实验证实电磁波的存在
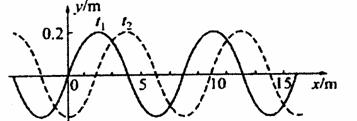
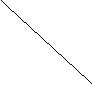
(2)一列横波在x轴上传播,在tl=0时刻波形如下图实线所示,t2=0.05s时刻波形如下 图虚线所示。
(i)由波形曲线读出这列波的振幅和波长;
(ii)若周期大于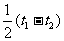 ,则最小波速是多少?方向如何?最大波速是多少?方向如
,则最小波速是多少?方向如何?最大波速是多少?方向如
何?
35.[物理--选修3-5](15分)
(1)以下是有关近代物理内容的若干叙述,其中正确的是 ( )
A.天然放射现象中发出的三种射线是从原子核内放出的看不见的射线
B.一束光照射到某种金属上不能发生光电效应,可能是因为这束光的光强太小
C.按照玻尔理论,氢原子核外电子从半径较小的轨道跃迁到半径较大的轨道时,电子 的动能减小,但原子的能量增大
D.原子核发生一次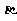 衰变,该原子外层就失去一个电子
衰变,该原子外层就失去一个电子
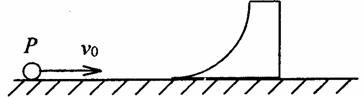
(2)光滑水平面上有一质量为M滑块,滑块的左侧是一光滑的丢圆弧,圆弧半径为R=lm。一质量为m的小球以速度v0。向右运动冲上滑块。已知M=4m,g取l0m/s2,若小球刚好没跃出 圆弧的上端,求:
圆弧的上端,求:
(i)小球的初速度v0是多少?
(ii)滑块获得的最大速度是多少?
36.[化学--选修化学与技术] (15分)
硫酸工业在国民经济中占有极其重要的地位。请回答硫酸工业中的如下问题:
(1)早期生产硫酸以黄铁矿为原料,目前很多国家都已经限制以黄铁矿为原料而以硫黄为原料,以硫黄为原料的优点是 。
(2)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3,是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO27%;O21l%;N2 82%);
 压强/Mpa 压强/Mpa转化率/% 温度/℃ |
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
85.8 |
89.5 |
96.4 |
利用表中数据分析。在实际生产中选择的适宜生产条件是:温度 ℃,
压强 MPa。
(3)选择适宜的催化剂,是否可以提高SO2的转化率? (填“是”或“否”),是否可以增大该反应所放出的热量? (填“是” 或“否”)。
(4)为提高SO3吸收率,实际生产中用 吸收SO3。
(5)在催化反应室中设有热交换装置,以下叙述与热交换装置的作用有关的是 (填写序号)。
A.保护环境。防止空气污染 B.充分利用热量,降低生产成本
C.升高温度,提高SO2的转化率 D.防止催化剂中毒
(6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方法可用
(填名称)吸收,然后再用硫酸处理,重新生成SO2和一种生产水泥的辅料,写出这两步反应的化学方程式 。
37.[化学一一选修物质结构与性质] (15分)
已知A、B、C、D都是元素周期表中前36号的元素,它们的原子序数依次增大。A原子核外部分电子排布式为:NsnNpn;B原子核外2P轨道有3个未成对电子:C原子核外S能级电子总数和P能级电子总数相同,且P能级成对电子数等于未成对电子数:D原子核外M层全充满,N层只有1个电子。
请回答:
(1)B元素外围电子排布图为: 。
(2)A、B、C的第一电离能由大到小顺序为 ,电负性由大到小顺序为
(用元素符号回答)。
(3)B和C两元素形成的阴离子BC-3中B的杂化类型为 ,空间构型为 。
(4)与BC-3互为等电子体且含有A、C两元素的微粒是 。(写化学式)
 (5)比较A、B的氢化物在水中溶解度大小并说明原因
。
(5)比较A、B的氢化物在水中溶解度大小并说明原因
。
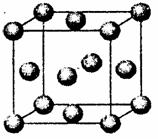
(6)D元素基态原子电子排布 ,该元素单质形成
的晶体晶胞如图所示,则D元素单质的堆积方式为
,已知D原子半径为r,相对原子质量为Mr,
则D元素单质的密度可表示为 。(用NA表
示阿伏加德罗常数)
38.[化学--选修有机化学基础](15分)
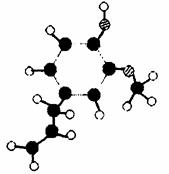 某有机化合物A因其具有麻醉作用,常用作局部麻醉
某有机化合物A因其具有麻醉作用,常用作局部麻醉
剂和镇痛剂。C10H12O2,其分子模型如右图所示(图中球
与球之间的连线代表化学键,如单键、双键等)。
请回答:
(1)根据右图模型写出有机物A的结构简式
。
(2)有机物A能发生的化学反应有(填序号)
。
①加成反应 ②水解反应
③加聚反应 ④消去反应
⑤氧化反应
(3)写出满足下列条件的A的一种同分异构体的结构简式 ;并指出该物质的核磁共振氢谱有 个峰,峰面积之比是 。
①能与碳酸氢钠溶液反应;
②苯环上的一氯取代物有1种。
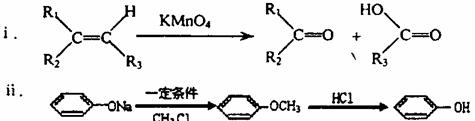
(4)已知:(如图)
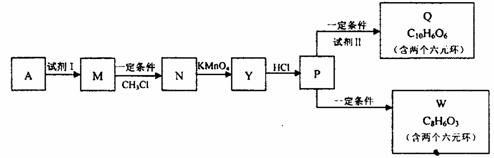
①试剂I不可选用的是(填字母) ;
a.CH3COONa溶液 b.NaOH溶液
c.NaHC3溶液 d. Na2CO3溶液
②在上述转化过程中,设置步骤M→N的目的是 ;
③写出P生成Q的化学方程式 ;
④写出W的结构简式 。
39.[生物--选修l生物技术实践](15分)
“葡萄美酒夜光杯,欲饮琵琶马上催。醉卧沙场君莫笑,古来征战几人回。”自古 酒就与人类生活息息相关。请回答下列酿制葡萄美酒的有关问题。
(1)人类使用酿制葡萄酒的微生物主要是酵母菌,它的同化作用类型是 ,
其无氧呼吸的反应式是 。
(2)酵母菌繁殖的最适温度是 ;酒精发酵一般将温度控制在 。
传统葡萄酒发酵技术所使用的酵母菌的来源是 。
(3)葡萄酒呈现深红色的原因是 。
(4)现在工厂化生产果酒,为提高果酒的品质,更好地抑制其它微生物的生长,采取
的措施是 ,并接入合适的菌种。
(5)某同学人工自酿葡萄酒时,在发酵后期向发酵液中通入空气,并将发酵液置于30-35℃环境中,结果发现发酵液中有 出现,这类微生物在糖类缺乏时可以使 转化为 ,后者再转化为 (物质)。
40.[生物--选修3现代生物科技专题] (15分)
下图为利用生物技术获得生物新品种的过程示意图。据图回答:
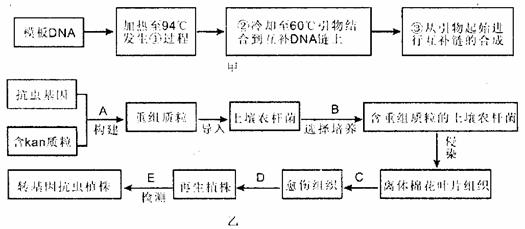 (1)随着科技发展,获取目的基因的方法也越来越多,若乙图中的“抗虫基因”是利用甲图中的方法获取的,该方法称为
。图中①过程与细胞中DNA复制过程相比,该过程不需要 酶。③是在
(填“酶的名称”)作用下进行延伸的。
(1)随着科技发展,获取目的基因的方法也越来越多,若乙图中的“抗虫基因”是利用甲图中的方法获取的,该方法称为
。图中①过程与细胞中DNA复制过程相比,该过程不需要 酶。③是在
(填“酶的名称”)作用下进行延伸的。
(2)在培育转基因植物的研究中,卡那霉素抗性基因(kan)常作为标记基因,只有含卡那霉素抗性基因的细胞才能在卡那霉素培养基上生长。乙图为获得抗虫棉技术的流程。A过程需要的酶有 、 。图中将目的基因导入植物受体细胞采用的方法是 。C过程的培养基除含有必要营养物质、琼脂和激素外,还必须加入 。
(3)离体棉花叶片组织经C、D、E成功地培育出了转基因抗虫植株,此过程涉及的细胞工程技术是 ,该技术的原理是 。
(4)检测目的基因是否转录出mRNA的具体方法是使用 与提取出的 做分子杂交。
(5)科学家将植株细胞培养到 ,包上人工种皮,制成了神奇的人工种子,以便更好地大面积推广培养。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com