
根据意义和句法作用,英语动词可分为四类:
1.行为动词(实义动词)
①及物动词:带宾语的动词
②不及物动词:不带宾语的动词
注意:英语里及物动词和不及物动词不是截然分开的,有的动词既可以是及物动词也可以是不及物动词。
It is important for you to learn how to learn.
第一个learn是及物动词,后面有宾语how to learn;第二个learn是不及物动词。
不及物动词向及物动词转化需要借助于介词、副词等构成短语动词。
He is working hard at English.
③状态动词(相对静止):contain, exist, own, prefer, belong
④动作动词:延续性(work, stay);非延续性(marry, go, come)
28.将绿矾(FeSO4.7H2O)隔绝空气条件下强热分解,已知产物全部为氧化物,为探究绿矾分解的反应产物,某同学进行了以下实验:
实验一:为探究固体产物中Fe元素的价态,该同学将固体产物溶于足量的稀H2SO4得到相应溶液,进行以下猜想和实验
|
猜想 |
实验操作 |
预期现象 |
|
猜想一:Fe元素只显______价 |
①向所得溶液中滴入KSCN溶液 ②向稀酸性KMnO4溶液中滴入所得溶液 |
KSCN溶液无明显现象 |
|
猜想二;Fe元素只显______价 |
稀酸性KMnO4溶液颜色_____ |
|
|
猜想三:Fe元素既有+2价又有+3价 |
KSCN溶液呈______色 稀酸性KMnO4溶液颜色______ |
实验二:为进一步探究该反应的产物,进行了如下图所示的实验
①实验开始时,点燃B处酒精喷灯之前应先打开A处活塞通CO2,其目的是
。
②装置图中C的作用是 。
③该组同学称取了55.6克绿矾按如图装置进行试验,待绿矾分解完全后,测得D瓶中沉淀的质量为23.3克,根据这些数据,可以得知,绿矾分解的化学方程式为_____________
④该组同学设计的装置存在着一个明显的缺陷是
27. 合成氨工业的部分工艺流程如下图所示:
合成氨工业的部分工艺流程如下图所示:
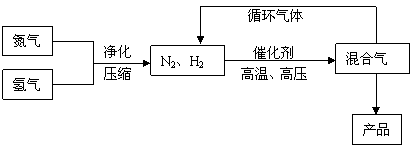






 请你回答下列问题:
请你回答下列问题:
 (1)已知:N2(g)+O2(g) =2NO(g);△H=180.5kJ·mol-1
(1)已知:N2(g)+O2(g) =2NO(g);△H=180.5kJ·mol-1
 4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ;△H=–905kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ;△H=–905kJ·mol-1
 2H2(g)+O2(g)=2H2O(g)
;△H=–483.6kJ·mol-1
2H2(g)+O2(g)=2H2O(g)
;△H=–483.6kJ·mol-1
 则N2(g)+3H2(g)
则N2(g)+3H2(g)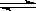 2NH3(g)的△H=_________________。
2NH3(g)的△H=_________________。
 (2)改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是_________
(2)改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是_________ 。
。
A.增大压强 B.降低温度 C.使用催化剂 D. 增大反应物的浓度 

(3)在一定条件下,将2molN2与5molH2混合于一个10L的密闭容器中,反应情况如右图所示: 图
①求5min内的平均反应速率v(NH3)=_______________
②达到平衡时NH3的体积分数为___________%
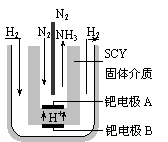 (4)近年来科学家提出了电解合成氨的方法:采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了高转化率的电解法合成氨(装置如右图)
(4)近年来科学家提出了电解合成氨的方法:采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了高转化率的电解法合成氨(装置如右图)
请回答:钯电极A是电解池的_______极(填“阳”或“阴”),该极上的电极反应式是_________________________
26.甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。
 已知:
已知:
(1)甲苯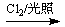 C的反应类型为________;
C的反应类型为________;
(2)F的结构简式为____________;
(3)写出下列反应方程式
①B+D→E______________________________________________________
②G→H ______________________________________________________
(4)E、J有多种同分异构体,写出符合下列条件的同分异构体结构简式(任写两种)
①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
_______________________________________________
25.A~E是原子序数依次增大的五种短周期元素,其性质或结构信息如下表所示
|
元素 |
A |
B |
C |
D |
E |
|
结构或性质信息 |
单质是空气中主要成分之一,其氢化物水溶液呈碱性 |
原子核外有两个未成对电子 |
日常生活中常见的金属,通常用电解法冶炼其单质 |
其简单阴离子带两个单位负电荷 |
单质有毒,常温下为有色气体,常用于自来水消毒 |
请结合表中信息完成下列各题:
(1)C在元素周期表中的位置是 ,
D的简单阴离子的核外电子排布式为 。
(2)下图是A~E的第一电离能和电负性数据,请回答
①图中序列5是元素 (用元素符号回答) 图
②下列各组元素最有可能形成离子化合物的是 (填编号)
a.A、B b.A、E c.B、C d.C、E
(3)A的常见单质分子中有多个共价键。
①常温下,该单质化学性质很稳定,是因为
②该单质分子中δ键与π键的数目之比为 。
(4)写出C、E形成的化合物与A的氢化物在水溶液中反应的离子方程式
。
13.下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的是
A.Mg2+、Na+、SO42-、Cl- B.K+、CO32-、Cl-、NO3-
C.Na+、K+、NO3-、SO32- D.NH4+、Na+、SO42-、NO3-
12.2010年在上海举办的世博会将主打环保牌,20辆氢燃料电池公交车、300辆氢燃料电池出租车将投入运行,它们以氢气为能源,实现了真正的零污染。氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是
A.正极反应式为:O2+2H2O+4e-=4OH-
B.工作一段时间后,电解液中KOH的物质的量浓度不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.2mol电子转移
11.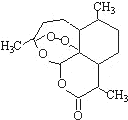 被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的
全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药
品。截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,
它在疟疾这一高传染性疾病治疗史上具有里程碑意义。其主要成分是
青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),
结构如右图所示。有关该化合物的叙述正确的是
A.该化合物分子结构中有三个酯基
B.该化合物在一定条件下不能与NaOH溶液反应
C.该化合物中含有过氧键,一定条件下有氧化性
D.青蒿素可溶于水
10.根据实验目的判断下列实验操作或装置正确的是
|
目的 |
实验室制O2 |
配制稀硫酸溶液 |
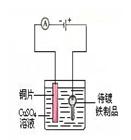
在铁制品上镀铜 |
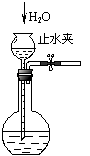 检查装置气密性 检查装置气密性 |
|
装置 或 操作 |
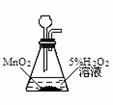 |
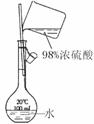 |
 |
|
|
选项 |
A |
B |
C |
D |
9. 设NA为阿伏加德罗常数,下列说法中正确的是
设NA为阿伏加德罗常数,下列说法中正确的是
 A.标准状况下,22.4 L水中含分子数为NA
A.标准状况下,22.4 L水中含分子数为NA
 B.23g金属Na与1L0.1mol/L的盐酸溶液反应,生成0.1NA个H2
B.23g金属Na与1L0.1mol/L的盐酸溶液反应,生成0.1NA个H2
 C.标准状况下,2.24L18O2中所含中子的数目为NA
C.标准状况下,2.24L18O2中所含中子的数目为NA
 D.14g分子式为CnH2n的(n≥2)链烃中含有的C=C的数目一定为NA/n
D.14g分子式为CnH2n的(n≥2)链烃中含有的C=C的数目一定为NA/n
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com