
19.⑴、KCl (1分) H2SO4 (1分)
⑵、2KMnO4+10KCl+8H2SO4=6K2SO4+2MnSO4+5Cl2↑+8H2O
(方程式没配平为0分,2分)
⑶、5 (2分)
⑷、NaBiO3的氧化性比KMnO4的强(答其它答案不得分,2分)
18. (1)C 2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O
(2)① C ② 先有红褐色沉淀出现,继续滴加硫酸溶液沉淀溶解得黄色溶液
(3)将溶液在较低温度下加热蒸发析出晶体,同时通以氯化氢气体防止水解(每空2分)
17. (1)还原、氧化 PbO2+4HCl PbCl2+Cl2↑+2H2O
PbCl2+Cl2↑+2H2O
⑵ Pb3O4 +2,+4 碱、 酸
⑶AsO43- +2I- +2H+ === AsO33- + I2↓ + H2O(2分) 2 (每空1分)
16.(1)四 , VB (2分)
(2)K2O·V2O5·2UO3·3H2O(2分,不必考虑物质的排列顺序)
|
(4)3V2O5+10Al ==== 6V+5Al2O3(1分)
15.(1)①x=1,y=1;(2分)
②6、2、4=1、3、2、4;(2分)
(2)PbS+4H2O2=PbSO4+4H2O(2分); 0.8(2分)
14. (1) P4(s)
+ 5O2(g) === 2P2O5(s);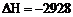 kJ/mol(2分)
kJ/mol(2分)
(2) 3 P4 + 10 HClO3 + 18 H2O = 10 HCl + 12 H3PO4(2分) ;HClO3 (1分)
(3) H3PO4(1分) ;12(1分)
13.(1)1、5、3、3、3、3。
(2)①I2+SO32 -+H2O = 2I-+SO42 -+2H+
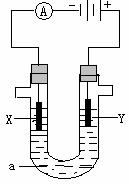
5.右图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同
时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为_______。在X极附近观察到的现象是_________。
②Y电极上的电极反应式为_____________,检验该电极反应产物的方法_________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是______,电极反应式_____________________。
②Y电极的材料是______,电极反应式_____________________。(说明:杂质发生的电极反应式不必写出)
1C 2B 3A 4D 5D 6A 7B 8C 9BC
12:(1)3C+2K2Cr2O7+8H2SO4===3CO2+2K2SO4+2Cr2(SO4)3+8H2O(2分)
(2)K2Cr2O7 CO2(各1分)(3)A (1分)(4)6.02×1023(1分)
2.极产物的判断。直接根据阳离子的放电顺序进行判断,阳离子的放电顺序:Ag+>Hg+>Fe3+>Cu2+>Pb2+ > H+ > Sn2+>Fe2+>Zn2+> H+ > Mg2+>Na+>Ca2+>K+
1. 阳极产物判断。首先看电极,当以较活泼金属(除Pt、Au)作电解池的阳极材料时,则电极材料失电子,电极被溶解;如果是惰性电极(Pt、Au、石墨),则要看溶液中的阴离子的失电子能力。阴离子的放电顺序:S2->I->Br->Cl->OH->
含氧酸根离子>F-
阳极产物判断。首先看电极,当以较活泼金属(除Pt、Au)作电解池的阳极材料时,则电极材料失电子,电极被溶解;如果是惰性电极(Pt、Au、石墨),则要看溶液中的阴离子的失电子能力。阴离子的放电顺序:S2->I->Br->Cl->OH->
含氧酸根离子>F-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com