
26£Æ(10∑÷)“—÷™¥º»©‘⁄“ª∂®Ãıº˛œ¬ƒÐ∑¢…˙Àı∫œ∑¥”¶£¨ æ¿˝»Áœ¬£∫“—÷™£∫
¢Ÿ”–ª˙ŒÔA£¨À¸µƒ∑÷◊” ΩŒ™C13H18O7”Γª∑÷◊”ÀÆ◊˜”√£¨ÀÆΩ‚…˙≥…B∫ÕC°£
°°°° ¢⁄BƒÐ∑¢…˙“¯æµ∑¥”¶£¨B“≤ø…”…µÌ∑€ÀÆΩ‚µ√µΩ£¨Bµƒ∑÷◊” ΩŒ™C6H12O6
°°°° ¢€C”ˆ¬»ªØÃ˙»Ð“∫ƒÐ∑¢…˙œ‘…´∑¥”¶£¨1molC”Î◊„¡øƒ∆∑¥”¶ø…≤˙…˙1molH2°£
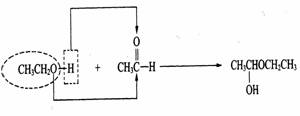 °°°° ¢ÐC‘⁄ µ±µƒÃıº˛œ¬”√—ıªØº¡—ıªØ£¨ø…µ√D£¨Dµƒ∑÷◊” ΩŒ™C7H6O3£¨œý∂‘∑÷◊”÷ ¡øD±»C¥Û14°£
°°°° ¢ÐC‘⁄ µ±µƒÃıº˛œ¬”√—ıªØº¡—ıªØ£¨ø…µ√D£¨Dµƒ∑÷◊” ΩŒ™C7H6O3£¨œý∂‘∑÷◊”÷ ¡øD±»C¥Û14°£
°°°° ¢ðD”–¡Ω∏ˆ»°¥˙ª˘£¨µ´≤ª «º‰Œª£¨À¸”ÎBr2‘⁄¥þªØº¡◊˜”√œ¬∑¢…˙“ª‰Â»°¥˙£¨≤˙ŒÔ”–Àƒ÷÷£¨DƒÐ”ÎúÀ·«‚ƒ∆»Ð“∫∑¥”¶°£
°°°° ¢ÞD”Γ“À·Ù˚£€(CH3CO)2O£ð∑¥”¶£¨ø…µ√≥£º˚“©ŒÔE∫Õ““À·£¨EƒÐ”ÎúÀ·«‚ƒ∆∑¥”¶∑≈≥ˆ∂˛—ıªØú°£
°°°° ‘ªÿ¥œ¬¡–Œ £∫
°° (1)–¥≥ˆΩ·ππºÚ Ω£∫C°°°°°°°°°°°°°°°°°° °°°°E°°°°°°°°°°°°°°°°°°°°°° °£
°° (2)–¥≥ˆ”ÎDª•Œ™Õ¨∑÷“Ïππð¢∫¨”–±Ωª∑«“∫¨”–ı•Ω·ππµƒΩ·ππºÚ Ω£∫
°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°£(–Ë–¥¡Ω÷÷)
(3)BÕ®≥£“‘¡˘‘™ª∑◊¥Ω·ππ¥Ê‘⁄£¨–¥≥ˆBµƒª∑◊¥Ω·ππºÚ Ω£∫°°°°°°°°°°°°°°°°°°°°°°
25£Æ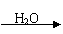 (12∑÷)“—÷™£∫HCNµƒΩ·ππŒ™H-C°‘N£ª°°°°°°°°
(12∑÷)“—÷™£∫HCNµƒΩ·ππŒ™H-C°‘N£ª°°°°°°°°
¢ŸR-CN°°°°°°°°°°°° RCOOH£¨°°°°°°°°
 ¢⁄R-Cl+CN£≠°°°°°°°°
R-CN+Cl£≠(RŒ™Ã˛ª˘)°£
¢⁄R-Cl+CN£≠°°°°°°°°
R-CN+Cl£≠(RŒ™Ã˛ª˘)°£
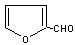 ”Ò√◊–æ°¢∏ ’·‘¸µ»∑œŒÔÀÆΩ‚∑¢ΩÕ∫Ûø…÷∆µ√ø∑»©
°°°°°°°°°°£¨À¸ «÷ÿ“™µƒªØπ§‘≠¡œ£¨À¸‘⁄“ª∂®Ãıº˛œ¬ø…∑¢…˙“‘œ¬±‰ªØ£∫
”Ò√◊–æ°¢∏ ’·‘¸µ»∑œŒÔÀÆΩ‚∑¢ΩÕ∫Ûø…÷∆µ√ø∑»©
°°°°°°°°°°£¨À¸ «÷ÿ“™µƒªØπ§‘≠¡œ£¨À¸‘⁄“ª∂®Ãıº˛œ¬ø…∑¢…˙“‘œ¬±‰ªØ£∫
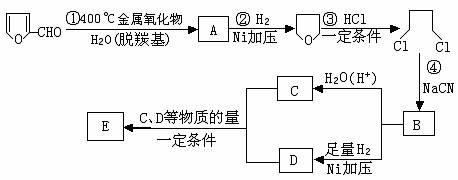
¢≈–¥≥ˆ∑¥”¶¿ý–Õ£∫¢⁄°°°° °°°°°°°°°° £¨¢Ð°°°° °°°°°°°°°° °£
¢∆–¥≥ˆ∑¥”¶¢€µƒªØ—ß∑Ω≥Ã Ω£∫ °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£ª
–¥≥ˆƒÐ÷§√˜ø∑»©÷–∫¨”–»©ª˘µƒ“ª∏ˆªØ—ß∑¥”¶∑Ω≥à Ω
°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
¢«»ÙEŒ™ª∑◊¥ªØ∫œŒÔ£¨‘Ú∆‰Ω·ππºÚ Ω°°°°°°°°°° °°°°°°°°°°°°°°°°°£
°°¢»»ÙEŒ™∏þ怌ԣ¨‘Ú∆‰Ω·ππºÚ Ω°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°£
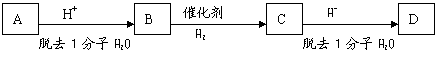
24£Æ(8∑÷)ƒ≥∂˛‘™¥ºA£¨∫¨—ıµƒ÷ ¡ø∑÷ ˝Œ™27.1%£¨∆‰”ý «Ãº∫Õ«‚°£A”–»Áœ¬Õº◊™ªØπÿœµ£¨‘⁄◊™ªØµƒπ˝≥Ã÷–ú‘≠◊”µƒ¡¨Ω”∑Ω Ωø…ƒÐª·∑¢…˙±‰ªØ£¨A°¢B°¢C∑÷◊”Ω·ππ÷–∂º”–4∏ˆº◊ª˘£¨«“æ˘Œ™¡¥◊¥Ω·ππ°£(“—÷™”–ª˙ŒÔ÷–Õ¨“ª∏ˆÃº…œ¡¨Ω”¡Ω∏ˆÙ«ª˘≤ªŒ»∂®)
 °°
°°
°° (1)Aµƒœý∂‘∑÷◊”÷ ¡ø «_________
(2)A∫ÕDµƒΩ·ππºÚ Ω∑÷± «________________∫Õ_______________________
(3)B◊™ªØŒ™CµƒªØ—ß∑Ω≥Ã Ω «(”√”–ª˙ŒÔµƒΩ·ππºÚ Ω±Ì æ)£∫
__________________________________________________________________
23£Æ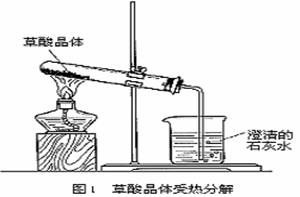 (12∑÷)ΩÃø∆ È£∫°∞»ÁÕº1À˘ 棨∏¯ ‘πÐ÷–µƒ““∂˛À·æßÃÂ(H2C2O4°§2H2O)º”»»£¨Ω´∑÷Ω‚≤˙ŒÔœ»Õ®»Î∏…‘Ôµƒ°¢¿‰µƒ–°…’±≠÷–£¨»ª∫Û‘ŸÕ®»Î≥Œ«Âµƒ ت“ÀÆ÷–£¨π€≤Ïœ÷œÛ°±°£
(12∑÷)ΩÃø∆ È£∫°∞»ÁÕº1À˘ 棨∏¯ ‘πÐ÷–µƒ““∂˛À·æßÃÂ(H2C2O4°§2H2O)º”»»£¨Ω´∑÷Ω‚≤˙ŒÔœ»Õ®»Î∏…‘Ôµƒ°¢¿‰µƒ–°…’±≠÷–£¨»ª∫Û‘ŸÕ®»Î≥Œ«Âµƒ ت“ÀÆ÷–£¨π€≤Ïœ÷œÛ°±°£
µ´‘⁄∑Ω∞∏ µ ©π˝≥Ã÷–£¨¥Ê‘⁄»Áœ¬±◊∂À£∫¢Ÿ ‘πÐø⁄œÚœ¬«„–±£¨““∂˛À·æßû€ªØ≥…“∫ã¨À≥ ‘πб⁄¡˜œÚ ‘πÐø⁄£¨µº÷¬ µ—È≤ªƒÐ≥…𶣪¢⁄Ω´∑÷Ω‚≤˙ŒÔÕ®»Î∏…‘Ôµƒ°¢¿‰µƒ–°…’±≠÷–£¨ºÏ—È≥ˆ¿¥µƒÀÆø…ƒÐ «““∂˛À·æßÃÂ∑÷Ω‚≥ˆ¿¥µƒΩ·æßÀÆ£¨≤ªƒÐ÷§√˜““∂˛À·∑÷Ω‚¡À£ª¢€““∂˛À· л»ª”∑¢≥ˆ’Ù∆¯Õ®»Î≥Œ«Âµƒ ت“ÀÆ÷–£¨…˙≥…µƒCaC2O4 «∞◊…´≥¡µÌ£¨∂‘—È÷§CO2”–∏…»≈£¨ŒÞ∑®»∑÷§““∂˛À·∑÷Ω‚£ª¢Ð““∂˛À·º”»»∑÷Ω‚µƒ≤˙ŒÔø…ƒÐŒ™CO2°¢CO°¢H2O£¨∆‰÷–CO «”–∂æ∆¯Ã£¨±ÿ–Î¥¶¿ÌµÙµ»°£
°°°° ’Î∂‘“‘…œ«Èøˆ£¨ƒ≥—–æø–‘—ßœ∞–°◊ÈΩ¯––ÃΩæø£¨…˺∆≥ˆ»Áœ¬ µ—ÈΩ¯––““∂˛À·µƒ∑÷Ω‚≤¢≤‚∂®∆‰∑÷Ω‚¬ £¨≤Ÿ◊˜≤Ω÷Ë»Áœ¬£∫
°°°° ¢Ÿ∞—““∂˛À·æßÃÂ∑≈‘⁄∫Êœ‰÷–Ω¯––∫Êø棨»•µÙΩ·æßÀÆ£¨±∏”√°£
°°°° ¢⁄∞¥Õº2¡¨Ω”∫√◊∞÷√°£
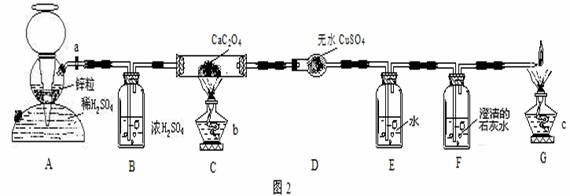
°°°° ¢€ºÏ≤È◊∞÷√µƒ∆¯√Ж‘°£
°°°° ¢Ð¥Úø™ªÓ»˚a£¨Õ®»ÎH2“ªª·∂˘£¨‘Ÿπÿ±’a£ªµ„»ºæ∆æ´µ∆b°¢c°£
°°°° ¢ðµ±C◊∞÷√÷–πÃÃÂœ˚ ß∫Û£¨Õ£÷πº”»»
°°°° ¢Þ¥Úø™ªÓ»˚a£¨ºÃ–¯Õ®»ÎH2£¨÷±÷¡¿‰»¥°£
°°°° ‘ªÿ¥œ¬¡–Œ £∫
¢≈◊∞÷√Bµƒ◊˜”√________________________________________________£ª
◊∞÷√Eµƒ◊˜”√________________________________________________°£
¢∆ºÏ—È∏√Ã◊◊∞÷√∆¯√Ж‘µƒ∑Ω∑® «
_____________________________________________________________________°£
¢«»Ù“∆◊þ◊∞÷√A°¢B£¨ª· πÀ˘≤‚““∂˛À·µƒ∑÷Ω‚¬ ____(ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±)°£
¢»ø…“‘¥˙ÃÊ◊∞÷√Gµƒ∑Ω∑® «_____________________________________________°£
¢…»Ù≥∆»°H2C2O4(∫Ê∏…)µƒ÷ ¡øŒ™4.5g£¨ µ—ÈΩ· ¯∫Û£¨≥∆µ√D°¢E°¢F∑÷±‘ˆ÷ÿ0.95g°¢0.40g°¢1.98g£¨‘Ú““∂˛À·µƒ∑÷Ω‚¬ Œ™_______________°£
22£Æ(14∑÷) œ¬√Ê «ƒ≥ªØ—ß—ßœ∞–°◊ȵƒÕ¨—ßΩ¯––—–æø–‘—ßœ∞µƒπ˝≥㨫΃„≤Œ”Î≤¢–≠÷˙À˚√«ÕÍ≥…œýπÿ—ßœ∞»ŒŒÒ°£
I£ÆøŒ±æΩȅСÀ““¥º—ıªØµƒ µ—È£∫∞—“ª∂ÀÕ‰≥…¬ð–˝◊¥µƒÕ≠Àø∑≈‘⁄æ∆æ´µ∆Õ‚—ʺ”»»£¨¥˝Õ≠Àø±Ì√ʱ‰∫⁄∫Û¡¢º¥∞—À¸≤»Π¢”–‘º2 mL““¥ºµƒ ‘πпԣ¨∑¥∏¥≤Ÿ◊˜º∏¥Œ°£◊¢“‚Œ≈…˙≥…ŒÔµƒ∆¯Œ∂£¨≤¢π€≤ÏÕ≠Àø±Ì√ʵƒ±‰ªØ°£
¢≈–°’‘Õ¨—ß”√ªØ—ß∑Ω∑®ÃÊ¥˙°∞Œ≈…˙≥…ŒÔµƒ∆¯Œ∂°±¿¥Àµ√˜…˙≥…ŒÔµƒ≥ˆœ÷£¨∏√ªØ—ß∑Ω∑®÷–À˘¡Ìº”µƒ ‘º¡º∞≥ˆœ÷µƒ÷˜“™œ÷œÛ «£∫__________£ª°°°°°°°°°°°°°°°°°°°°°°°° °£(”√À˘—ßµƒ÷™ ∂ªÿ¥)
¢∆–°’‘Õ¨—ß‘⁄ÃΩæø°∞Œ≈…˙≥…ŒÔµƒ∆¯Œ∂°±µƒÃÊ¥˙∑Ω∑® ±£¨≈º»ª∑¢œ÷œÚ‰ÂÀÆ÷–º”»Î◊„¡øµƒ““»©»Ð“∫£¨ø…“‘ø¥µΩ‰ÂÀÆÕ …´°£∏√Õ¨—ߌ™Ω‚ Õ…œ ˆœ÷œÛ£¨Ã·≥ˆ»˝÷÷≤¬œÎ£∫
¢Ÿ‰Â”Γ“»©∑¢…˙»°¥˙∑¥”¶£ª¢⁄°°°°°°°°°°°° ¢€”…”⁄»©ª˘æþ”–ªπ‘≠–‘£¨‰ÂΩ´““»©—ıªØŒ™““À·°£
Œ™ÃΩæøƒƒ÷÷≤¬œÎ’˝»∑£¨–°¿ÓÕ¨—ß÷≥ˆ¡À»Áœ¬¡Ω÷÷ µ—È∑Ω∞∏£∫
∑Ω∞∏“ª£∫”√pH ‘÷ΩºÏ≤‚‰ÂÀÆÕ …´∫ۻГ∫µƒÀ·ºÓ–‘£ª
∑Ω∞∏∂˛£∫≤‚∂®∑¥”¶«∞‰ÂÀÆ÷–Br2µƒŒÔ÷ µƒ¡ø∫Õ∑¥”¶∫ۻГ∫÷–Br-¿Î◊”µƒŒÔ÷ µƒ¡ø°£
(3)∑Ω∞∏“ª «∑Òø…––°°°°°°°° (ÃÓ°∞ «°±ªÚ°∞∑Ò°±)£¨¿Ì”… «°° °°°°°°°°°°°°°°°°°°°£
(4)–°¿ÓÕ¨—ß»œŒ™£∫ºŸ…Ë≤‚µ√∑¥”¶«∞‰ÂÀÆ÷–Br2µƒŒÔ÷ µƒ¡øŒ™amol£¨»Ù≤‚µ√∑¥”¶∫Û
n(Br-)=°°°°°°°°°° mol£¨‘ÚÀµ√˜‰Â”Γ“»©∑¢…˙»°¥˙∑¥”¶°£
(5)–°Œ‚Õ¨—߅˺∆»Áœ¬ µ—È∑Ω∞∏£∫¢Ÿ∞¥ŒÔ÷ µƒ¡ø÷Ʊ»Œ™1£∫5≈‰÷∆KBrO3-KBr»Ð“∫£¨º”∫œ µƒ ¡øµƒÀ·£¨ÕÍ»´∑¥”¶≤¢œ°÷¡1L£¨…˙≥…0.5molBr2°£¢⁄»°…œ ˆ»Ð“∫10mLº”»Î◊„¡ø““»©»Ð“∫£¨ π÷ÆÕ …´£¨»ª∫ÛΩ´À˘µ√»Ð“∫œ° ÕŒ™100mL£¨◊º»∑¡ø»°∆‰÷–10mL°£¢€º”»Îπ˝¡øµƒAgNO3»Ð“∫£¨π˝¬À°¢œ¥µ”°¢∏…‘Ô∫Û≥∆¡øµ√µΩµ≠ª∆…´πÃÃÂ0.188g°£»Ù“—÷™CH3COOAg“◊»Ð”⁄ÀÆ°£
‘Õ®π˝º∆À„≈–∂œ£∫‰Â”Γ“»©∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°°°°°°°°°
–°’≈Õ¨—ß»œŒ™∫œ µƒÀ·º»≤ª «¡ÚÀ·“≤≤ª «—ŒÀ·£¨’‚ «Œ™ ≤√¥£ø°°°°°°°°°°°°°°°°°°
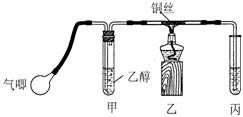 ¢Ú£Æ–°«ÆÕ¨—ß¿˚”√œ¬Õº◊∞÷√Ω¯––““¥ºµƒ¥þªØ—ıªØ µ—È≤¢÷∆»°““»©( ‘πб˚÷–”√ÀÆŒ¸ ’≤˙ŒÔ)£¨Õº÷–Ã˙ºÐîµ»◊∞÷√“—¬‘»•°£ µ—È ±£¨œ»º”»»≤£¡ßπÐ÷–µƒÕ≠Àø£¨‘ºlmin∫Ûπƒ»Îø’∆¯°£
¢Ú£Æ–°«ÆÕ¨—ß¿˚”√œ¬Õº◊∞÷√Ω¯––““¥ºµƒ¥þªØ—ıªØ µ—È≤¢÷∆»°““»©( ‘πб˚÷–”√ÀÆŒ¸ ’≤˙ŒÔ)£¨Õº÷–Ã˙ºÐîµ»◊∞÷√“—¬‘»•°£ µ—È ±£¨œ»º”»»≤£¡ßπÐ÷–µƒÕ≠Àø£¨‘ºlmin∫Ûπƒ»Îø’∆¯°£
«ÎÃÓ–¥œ¬¡–ø’∞◊£∫
¢≈““¥º∑¢…˙¥þªØ—ıªØµƒªØ—ß∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
 ¢∆ µ—È ±£¨–°«ÆÕ¨—ßΩ´º◊◊∞÷√Ω˛‘⁄70°Ê-80°ÊµƒÀÆ‘°÷–£¨ƒøµƒ «°°°°°°°°°°°°°°°°
____°£
¢∆ µ—È ±£¨–°«ÆÕ¨—ßΩ´º◊◊∞÷√Ω˛‘⁄70°Ê-80°ÊµƒÀÆ‘°÷–£¨ƒøµƒ «°°°°°°°°°°°°°°°°
____°£
–°ÀÔÕ¨—ß»œŒ™£∫”…”⁄–°«ÆÕ¨—ß◊∞÷√…˺∆…œµƒ»±œð£¨ µ—ÈΩ¯–– ±ø…ƒÐª· °°°°°°°°____________°£
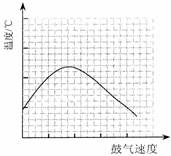
¢«∑¥”¶∑¢…˙∫Û£¨“∆»•æ∆æ´µ∆£¨¿˚”√∑¥”¶◊‘…Ì∑≈≥ˆµƒ»»¡øø…Œ¨≥÷∑¥”¶ºÃ–¯Ω¯––°£Ω¯“ª≤ΩÃΩæø±Ì√˜£¨πƒ∆¯ÀŸ∂»”Î∑¥”¶ÃÂœµµƒŒ¬∂»πÿœµ«˙œþ»ÁÕºÀ˘ æ°£
«Îƒ„Ω‚ Õπƒ∆¯ÀŸ∂»π˝øÏ£¨∑¥”¶ÃÂœµŒ¬∂»∑¥∂¯œ¬Ωµµƒ‘≠“Ú£∫°°°°°°°°°°°°°°°° °£
ƒ„»œŒ™∏√ µ—È÷–°∞πƒ∆¯ÀŸ∂»°±’‚“ª±‰¡øø…”√°°°°°°°°°°°°°°°°°°°°°° ¿¥º∆¡ø°£
21£Æ(4∑÷)œ¬¡–”–πÿ µ—ȵƒ– ˆ£¨’˝»∑µƒ «(ÃÓ–Ú∫≈)°°°°°°°°°°°°°°
A°¢”√NaOH»Ð“∫≥˝»•““À·““ı•÷–ªÏ”–µƒ““À·°¢““¥º£¨»ª∫Û∑÷“∫
B°¢∑÷¡Û Ø”Õ ±£¨Œ¬∂»º∆µƒƒ©∂À±ÿ–Î≤»Γ∫√Êœ¬
C°¢”√∑÷“∫¬©∂∑∑÷¿Îª∑º∫ÕÈ∫ÕÀƵƒªÏ∫œ“∫ÃÂ
D°¢”√≈®∞±ÀÆœ¥µ”◊ˆπ˝“¯æµ∑¥”¶µƒ ‘πÐ
E°¢≈‰÷∆“¯∞±»Ð“∫ ±£¨Ω´œ°∞±ÀƬ˝¬˝µŒº”µΩœ°œıÀ·“¯»Ð“∫÷–£¨≤˙…˙∞◊…´≥¡µÌ∫ۺÖ¯µŒº”µΩ≥¡µÌ∏’∫√»ÐΩ‚Œ™÷π
F°¢’·Ã«ÀÆΩ‚∫Û£¨÷±Ω”µŒº”–¬÷∆«‚—ıªØÕ≠–¸◊«“∫≤¢º”»»ºÏ—ÈÀÆΩ‚≤˙ŒÔ÷–µƒ∆œÃ—ë
20£ÆŒÞ…´µƒ”–ª˙ŒÔI «”°÷∆∑¿Œ±…ñ͵ƒ“ª÷÷‘≠¡œ£¨‘⁄◊œÕ‚π‚∑¯…‰œ¬Iø…◊™±‰≥…Ω·ππ¢Ú(œ‘≥»…´)£¨∑¥”¶»Áœ¬(R1°¢R2°¢R3 «Ã˛ª˘)£∫”–πÿ…œ ˆ±‰ªØµƒÀµ∑®≤ª’˝»∑µƒ «(°°°° )
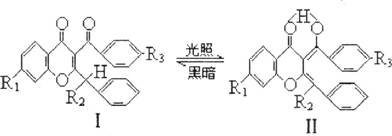
A£ÆI∫ÕIIª•Œ™Õ¨∑÷“Ïππ㪰° °°B£ÆI°¢¢Ú∑÷◊”÷–À˘”–‘≠◊”∂ºø…ƒÐ‘⁄Õ¨“ª∆Ω√Ê…œ£ª
C£ÆIIø…ø¥◊˜¥º¿ý£ª°°°° °°°°°°°°D£Æ¢ÚƒÐ∑¢…˙º”≥…∑¥”¶°£
µ⁄¢ÒIæÌ( π≤80∑÷)
19£ÆΩ´1mol ““À·(∆‰÷–µƒÙ«ª˘—ı”√ 18O ±Íº«)‘⁄≈®¡ÚÀ·¥Ê‘⁄œ¬≤¢º”»»”Î◊„¡ø““¥º≥‰∑÷∑¥”¶°£œ¬¡–– ˆ≤ª’˝»∑µƒ «(°°°° )°°
A£Æ…˙≥…µƒ““À·““ı•÷–∫¨”–18O°°°°°° °°B£Æ…˙≥…µƒÀÆ∑÷◊”÷–∫¨”–18O
C£Æø…ƒÐ…˙≥… 45g ““À·““ı•°°°°°°°° D£Æ≤ªø…ƒÐ…˙≥… 88g ““À·““ı•
18£Æ“ª–©ÕÈÃ˛µƒ»º…’»»(KJ/mol)»Áœ¬±Ì£∫
|
ªØ∫œŒÔ |
»º…’»» |
ªØ∫œŒÔ |
»º…’»» |
|
º◊ÕÈ |
891.0 |
’˝∂°ÕÈ |
2878.0 |
|
““ÕÈ |
1560.8 |
“Ï∂°ÕÈ |
2869.6 |
|
±˚ÕÈ |
2221.5 |
2£≠º◊ª˘∂°ÕÈ |
3531.3 |
°°œ¬¡–±Ì¥Ô’˝»∑µƒ «(°°°° )
A£Æ»»Œ»∂®–‘£∫’˝∂°ÕÈ£º“Ï∂°ÕÈ°°°°
B£Æ““ÕÈ»º…’µƒ»»ªØ—ß∑Ω≥Ã ΩŒ™£∫
2C2H6(g)+7O2(g)£Ω4CO2(g)+6H2O(g) ¶§H£Ω£≠1560.8KJ/mol
C£Æ’˝ŒÏÕȵƒ»º…’»»¥Û‘º‘⁄3540 KJ/mol◊Û”“
D£ÆœýÕ¨÷ ¡øµƒÕÈÃ˛£¨Ãºµƒ÷ ¡ø∑÷ ˝‘Ω¥Û£¨ÕÍ»´»º…’∑≈≥ˆµƒ»»¡ø‘Ω∂ý
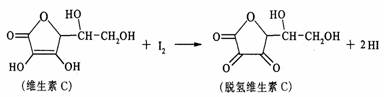
17£Æ–¬œ ÀÆπ˚°¢ þ≤À°¢»È÷∆∆∑÷–∏ª∫¨µƒŒ¨…˙ÀÿCæþ”–√˜œ‘µƒøπÀ•¿œ◊˜”√£¨µ´“◊±ªø’∆¯—ıªØ°£ƒ≥øŒÕ‚–°◊È¿˚”√µ‚µŒ∂®∑®≤‚ƒ≥≥»÷≠÷–Œ¨…˙ÀÿCµƒ∫¨¡ø£¨∆‰ªØ—ß∑Ω≥Ã ΩŒ™£∫°°
 °°°°
°°°°
œ¬¡–Àµ∑®’˝»∑µƒ «(°°°° )°°°°
A£Æ…œ ˆ∑¥”¶Œ™»°¥˙∑¥”¶°°°°°° °°°°°°°° B£ÆµŒ∂® ±ø…”√µÌ∑€»Ð“∫◊˜÷∏ 溡
C£ÆµŒ∂® ±”¶æÁ¡“’Òµ¥◊∂–Œ∆ø°°°° °°°°°°°° D£ÆÕ—«‚Œ¨…˙ÀÿCµƒ∑÷◊” ΩŒ™C6H6O6
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com