
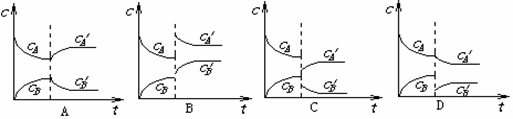
26£®(16·Ö)æÉÄę·“Ó¦2A(g) 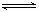 B(g)(·ÅČČ·“Ó¦)“Ó·“Ó¦æŖŹ¼ÖĮ½ØĮ¢Ę½ŗāŗóøıäijŅ»Ķā½ēĢõ¼ž(Ķā½ēĢõ¼žÖøµÄŹĒĪĀ¶Č”¢Ń¹Ē攢ÅضČŗĶ“߻ƼĮ)Ź¹Ę½ŗā·¢ÉśĮĖŅʶÆÖĮŠĀµÄĘ½ŗā£¬øĆ¹ż³ĢÖŠø÷ĪļÖŹµÄÅضČ(ÓĆc±ķŹ¾)Ėꏱ¼ä±ä»ÆĒéæöČēĻĀĶ¼ĖłŹ¾£¬ŹŌ·ÖĪöø÷Ķ¼£¬Öø³öµ¼ÖĀĘ½ŗāŅĘ¶ÆµÄŅņĖŲŗĶĘ½ŗāŅĘ¶ÆµÄ·½Ļņ£ŗ
B(g)(·ÅČČ·“Ó¦)“Ó·“Ó¦æŖŹ¼ÖĮ½ØĮ¢Ę½ŗāŗóøıäijŅ»Ķā½ēĢõ¼ž(Ķā½ēĢõ¼žÖøµÄŹĒĪĀ¶Č”¢Ń¹Ē攢ÅضČŗĶ“߻ƼĮ)Ź¹Ę½ŗā·¢ÉśĮĖŅʶÆÖĮŠĀµÄĘ½ŗā£¬øĆ¹ż³ĢÖŠø÷ĪļÖŹµÄÅضČ(ÓĆc±ķŹ¾)Ėꏱ¼ä±ä»ÆĒéæöČēĻĀĶ¼ĖłŹ¾£¬ŹŌ·ÖĪöø÷Ķ¼£¬Öø³öµ¼ÖĀĘ½ŗāŅĘ¶ÆµÄŅņĖŲŗĶĘ½ŗāŅĘ¶ÆµÄ·½Ļņ£ŗ
|
ŠņŗÅ |
Ę½ŗāŅĘ¶ÆµÄŅņĖŲ |
Ę½ŗāŅĘ¶ÆµÄ·½Ļņ |
|
A |
”” |
”” |
|
B |
”” |
”” |
|
C |
”” |
”” |
|
D |
”” |
”” |
25£®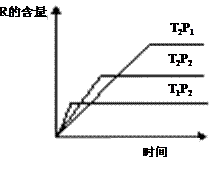 ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠĻĀĮŠ·“Ó¦£ŗ
ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠĻĀĮŠ·“Ó¦£ŗ
M (g)+N (g)  ””R
(g)+2 L
””R
(g)+2 L
“Ė·“Ó¦·ūŗĻÓŅ±ßĶ¼Ļń”£ĻĀĮŠŠšŹö
ÕżČ·µÄŹĒ”””””””””””” (”” ””)
”””” A£®Õż·“Ó¦ĪüČČ£¬LŹĒĘųĢå””””””
B£®Õż·“Ó¦ĪüČČ£¬LŹĒ¹ĢĢå
”””””” C£®Õż·“Ó¦·ÅČČ£¬LŹĒŅŗĢå ””””””””””””””””””””
D£®Õż·“Ó¦·ÅČČ£¬LŹĒĘųĢå
µŚ¢ņ¾ķ(·ĒŃ”ŌńĢā£¬¹²50·Ö)
24£®³£ĪĀĻĀ£¬Ä³ČÜŅŗÖŠÓÉĖ®µēĄėµÄc(H+) = 1”Į10-13mol”¤L£1£¬øĆČÜŅŗæÉÄÜŹĒ”””””””””” ( ””””)
”””” ¢Ł¶žŃõ»ÆĮņĖ®ČÜŅŗ”” ”””””””””””””””””””””””””””””””” ¢ŚĀČ»Æļ§Ė®ČÜŅŗ
”””” ¢ŪĻõĖįÄĘĖ®ČÜŅŗ”” ”””””””””””””””””””””””””””””””””” ¢ÜĒāŃõ»ÆÄĘĖ®ČÜŅŗ
”””” A£®¢Ł¢Ü”””””””””””””””””” B£®¢Ł¢Ś”””””””””””””””””” C£®¢Ś¢Ū”””””””””””””””””” D£®¢Ū¢Ü
23£®æÉŅŌÖ¤Ć÷æÉÄę·“Ó¦N2 + 3H2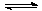 2NH3ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ”””””””””””””””””””””””””” (”””” )
2NH3ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ”””””””””””””””””””””””””” (”””” )
¢ŁŅ»øöN”ŌN¶ĻĮѵÄĶ¬Ź±£¬ÓŠ3øöH£H¼ü¶ĻĮŃ””
¢ŚŅ»øöN”ŌN¼ü¶ĻĮѵÄĶ¬Ź±£¬ÓŠ6øöN£H¼ü¶ĻĮŃ””
¢ŪĘäĖüĢõ¼ž²»±äŹ±£¬»ģŗĻĘųĢåĘ½¾łŹ½Įæ²»ŌŁøı䔔
¢Ü±£³ÖĘäĖüĢõ¼ž²»±äŹ±£¬ĢåĻµŃ¹Ēæ²»ŌŁøı䔔
¢ŻNH3%”¢N2%”¢H2%¶¼²»ŌŁøı䔔
¢ŽŗćĪĀŗćČŻŹ±£¬Ćܶȱ£³Ö²»±ä””
¢ßÕż·“Ó¦ĖŁĀŹv(H2) = 0.6mol/(L”¤min)£¬Äę·“Ó¦ĖŁĀŹv(NH3) = 0.4mol/(L”¤min)
A£®Č«²æ”¢”””””””””””””” B£®Ö»ÓŠ¢Ł¢Ū¢Ü¢Ż”” C£®¢Ś¢Ū¢Ü¢Ż¢ß ”””””” D£®Ö»ÓŠ¢Ū¢Ż¢Ž¢ß
22£®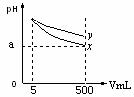 pH=11µÄx”¢yĮ½ÖÖ¼īČÜŅŗø÷5mL£¬·Ö±šĻ”ŹĶÖĮ500mL£¬ĘäpHÓėČÜŅŗĢå»ż(V)µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(”””” )
pH=11µÄx”¢yĮ½ÖÖ¼īČÜŅŗø÷5mL£¬·Ö±šĻ”ŹĶÖĮ500mL£¬ĘäpHÓėČÜŅŗĢå»ż(V)µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(”””” )
”””””” A£®Ļ”ŹĶŗóxČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č±ČyČÜŅŗÖŠĖ®µēĄė³Ģ¶ČŠ”
B£®Čōx”¢yŹĒŅ»ŌŖ¼ī£¬µČĪļÖŹµÄĮæÅØ¶ČµÄŃĪĖįŃĪČÜŅŗyµÄpH“ó
C£®Čōx”¢y¶¼ŹĒČõ¼ī£¬ŌņaµÄÖµŅ»¶Ø“óÓŚ9
D£®ĶźČ«ÖŠŗĶx£¬yĮ½ČÜŅŗŹ±£¬ĻūŗÄĶ¬ÅضČĻ”ĮņĖįµÄĢå»żV(x)>V(y)
21£®ÖŲĖ®D2OµÄĄė×Ó»żĪŖ1.6”Į10-15£¬æÉŅŌÓĆPHŅ»ŃłµÄ¶ØŅåĄ“¹ę¶ØpD=-lgc(D+),ŅŌĻĀ¹ŲÓŚpDµÄŠšŹöÕżČ·µÄŹĒ”””””””””””” ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” (”””” )
”””” A£®ÖŠŠŌČÜŅŗÖŠPD=7
”””” B£®ŌŚ1LD2OµÄČÜŅŗÖŠČܽā0.01mol NaOD(ÉčČÜŅŗµÄĢå»żĪŖ1L)£¬ĘäÖŠpD=12
”””” C£®ŌŚ1L D2OÖŠČܽā 0.01mol DCl(ÉčČÜŅŗµÄĢå»żĪŖ1L)£¬ĘäÖŠpD=2
D£®ŌŚ100mL 0.25mol”¤L-1µÄNaODÖŲĖ®ČÜŅŗÖŠ¼ÓČė50mL 0.2mol”¤L-1DClµÄµÄÖŲĖ®ČÜŅŗ£¬ĘäpD=1
20£®ŗćĪĀĻĀ£¬ČŻ»ż¾łĪŖ2LµÄĆܱÕČŻĘ÷M”¢NÖŠ£¬·Ö±šÓŠŅŌĻĀĮŠĮ½ÖÖĘšŹ¼Ķ¶ĮĻ½ØĮ¢µÄæÉÄę·“Ó¦3A(g)+2B(g)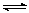 2C(g)+xD(s)µÄ»ÆŃ§Ę½ŗāדĢ¬£¬Ļą¹ŲŹż¾ŻČēĻĀ£ŗM£ŗ3 mol A ”¢2
mol B£»2 min“ļĘ½ŗā£¬Éś³ÉD 1.2 mol£¬²āµĆ“Ó·“Ó¦æŖŹ¼µ½Ę½ŗāCµÄĖŁĀŹĪŖ0.3 mol”¤(L”¤min)-1”£N£ŗ2molC”¢ymolD£»“ļĘ½ŗāŹ±c(A)=0.6
mol”¤L£1”£ĻĀĮŠĶʶĻµÄ½įĀŪÖŠ²»ÕżČ·µÄŹĒ(”””” )
2C(g)+xD(s)µÄ»ÆŃ§Ę½ŗāדĢ¬£¬Ļą¹ŲŹż¾ŻČēĻĀ£ŗM£ŗ3 mol A ”¢2
mol B£»2 min“ļĘ½ŗā£¬Éś³ÉD 1.2 mol£¬²āµĆ“Ó·“Ó¦æŖŹ¼µ½Ę½ŗāCµÄĖŁĀŹĪŖ0.3 mol”¤(L”¤min)-1”£N£ŗ2molC”¢ymolD£»“ļĘ½ŗāŹ±c(A)=0.6
mol”¤L£1”£ĻĀĮŠĶʶĻµÄ½įĀŪÖŠ²»ÕżČ·µÄŹĒ(”””” )
A£®x=2”””””””””” ”””””””””””””””””””””””””””””””” B£®Ę½ŗāŹ±MÖŠc(A)<0.6mol/L
C£®y>0.8”””””””” ”””””””””””””””””””””””””””””””” D£®y<0.8
19£®500 mL KNO3ŗĶCu(NO3)2µÄ»ģŗĻČÜŅŗÖŠc(NO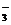 )=6mol”¤L£1£¬ÓĆŹÆÄ«×÷µē¼«µē½ā“ĖČÜŅŗ£¬µ±ĶصēŅ»¶ĪŹ±¼äŗó£¬Į½¼«¾łŹÕ¼Æµ½22£®4 LĘųĢå(±ź×¼×“æö)£¬¼Ł¶Øµē½āŗóČÜŅŗĢå»żČŌĪŖ500 mL£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”””””””””””””””””” (”””” )
)=6mol”¤L£1£¬ÓĆŹÆÄ«×÷µē¼«µē½ā“ĖČÜŅŗ£¬µ±ĶصēŅ»¶ĪŹ±¼äŗó£¬Į½¼«¾łŹÕ¼Æµ½22£®4 LĘųĢå(±ź×¼×“æö)£¬¼Ł¶Øµē½āŗóČÜŅŗĢå»żČŌĪŖ500 mL£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”””””””””””””””””” (”””” )
”””” A£®Ō»ģŗĻČÜŅŗÖŠ c (K+)ĪŖ2 mol”¤L£1 ”””” B£®ÉĻŹöµē½ā¹ż³ĢÖŠ¹²×ŖŅĘ4 molµē×Ó
”””” C£®µē½āµĆµ½µÄCuµÄĪļÖŹµÄĮæĪŖ0.5mol”””” D£®µē½āŗóČÜŅŗÖŠc(H+)ĪŖ2 mol”¤L£1
18£®Ģå»żĻąĶ¬µÄ¼×”¢ŅŅĮ½ČŻĘ÷ÖŠ·Ö±š³äÓŠµČĪļÖŹµÄĮæµÄSO2ŗĶO2£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗ2SO2 + O2 ””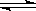 2SO3²¢“ļµ½Ę½ŗā£¬ŌŚÕā¹ż³ĢÖŠ£¬¼×ČŻĘ÷±£³ÖĢå»ż²»±ä£¬ŅŅČŻĘ÷±£³ÖŃ¹Ēæ²»±ä£¬Čō¼×ČŻĘ÷ÄŚSO2µÄ×Ŗ»ÆĀŹĪŖP%£¬ŌņŅŅČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹ”””””””””””””””””””” (”””” )
2SO3²¢“ļµ½Ę½ŗā£¬ŌŚÕā¹ż³ĢÖŠ£¬¼×ČŻĘ÷±£³ÖĢå»ż²»±ä£¬ŅŅČŻĘ÷±£³ÖŃ¹Ēæ²»±ä£¬Čō¼×ČŻĘ÷ÄŚSO2µÄ×Ŗ»ÆĀŹĪŖP%£¬ŌņŅŅČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹ”””””””””””””””””””” (”””” )
A£®µČÓŚP%”” ”””””””” B£®“óÓŚP%”” ”””””””” C£®Š”ÓŚP%”” ”””””””” D£®ĪŽ·ØÅŠ¶Ļ
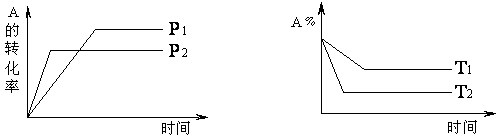
17£®æÉÄę·“Ó¦aA(g) + bB(g) cC(g) + dD(g)·ūŗĻĻĀĶ¼”£ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ(”””” )
cC(g) + dD(g)·ūŗĻĻĀĶ¼”£ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ(”””” )
 ””
””
””
””
”””””” A£®a+b < c+d£»Õż·“Ó¦ĪüČČ”” ”””””””””””” B£®a+b > c+d£»Õż·“Ó¦·ÅČČ
C£®a+b < c+d£»Õż·“Ó¦·ÅČČ”””””””””” D£®a+b > c+d£»Õż·“Ó¦ĪüČČ
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com