
29.(18分)
某研究小组的同学调查了野外山坡上三个不同地点A、B、C的植物群落,并测量了三个地点的土壤特征等环境因素,结果见下表。根据所得数据回答问题。
|
生物种类 |
地点A(山腰) |
地点B(山腰) |
地点C(山腰) |
|
草 |
3种 |
5种 |
9种 |
|
蕨类 |
7种 |
5种 |
8种 |
|
灌木 |
15种 |
4种 |
2种 |
|
松树 |
0种 |
2种 |
0种 |
|
落叶树 |
20种 |
5种 |
0种 |
|
非生物因素 |
地点A(山腰) |
地点B(山腰) |
地点C(山腰) |
|
风速 |
低 |
高 |
高 |
|
距地1.5米的光强 |
低 |
中 |
高 |
|
土壤湿度/% |
48 |
35 |
15 |
|
土壤的有机质/% |
6.5 |
3.8 |
2.5 |
|
土壤深度/cm |
>300 |
-100 |
<15 |
|
土壤氨量/mg.Kg-1 |
9.4 |
4.5 |
2.3 |
(1)根据调查结果判断,物种丰度最大的是地点 处的植物群落。
(2)如果遭遇山火,山坡的植被彻底烧光,则原地点将发生的群落演替类型属于
演替。群落演替总是向着 方向发展,直至达到 为止。
(3)如果地点A、B、C处的光照条件同等充足,则能更有效地利用太阳光能的是地点
的植物群落,原因是 。
(4)土壤中的有机质经过 才能被植物吸收利用。土壤缺氧时,抑制根对矿质元素离子的吸收,据此可知根吸收矿质元素离子的方式为 。
(5)落叶树在地点C不能生长的原因是 。(说出不少于两个原因)
28.(J4分)
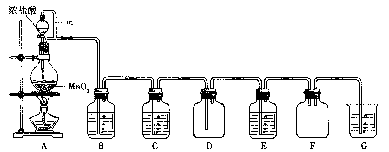 二氧化锰(MnO2)与浓盐酸混合加热可得到氯气、氯化锰等,下图是制取并探究Cl2化学性质的装置图。
二氧化锰(MnO2)与浓盐酸混合加热可得到氯气、氯化锰等,下图是制取并探究Cl2化学性质的装置图。
(1)已知锰元素的常见化合价为+7、+6、+4、+2,写出圆底烧瓶中反应的化学方程式
。
(2)A中m管的作用是 ,装置F的作用是 。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是 。
(4)E中若装有FeCl2溶液,反应的离子方程式为 ;E中若装有淀粉碘化钾溶液,能观察到的实验现象是 。
(5)实验中发现:浓盐酸与Mn0:混合加热生成氯气,稀盐酸与Mn0:混合加热不生成氯气。针对上述现象,化学小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通人HCl气体,加热
b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸,加热
d.Mn02与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是 ;实验c的目的是 。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是 。
27.(12分)
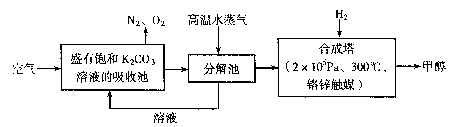 为减小和消除CO2对环境的影响,有科学家提出“绿色自由”构想。即先把空气吹人碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
为减小和消除CO2对环境的影响,有科学家提出“绿色自由”构想。即先把空气吹人碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
(1)写出分解池中反应的化学方程式 。
(2)在合成塔中,当有4.4kg CO2与足量H2完全反应,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
(3)写出以氢氧化钾为电解质的甲醇燃料电池的负极反应式 。
当电子转移为 mol时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)在体积为l L的密闭容器中,充人1mol CO2和3molH2在500°C下发生反应。有关物质的浓度随时问变化如下图所示。
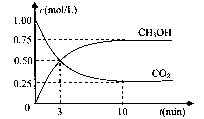
①从反应开始到平衡,H2的平均反应速率v(H2)= 。
②若其他条件不变,只将温度提高到800°C,再次达平衡时,n(CH3OH)/n(CO2)比值 (填“增大”、“减小”或“不变”)。
26.(16分)
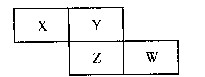 X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
I.若Z元素原子的最外层电子数是电子层数的2倍
(1)W在周期表中的位置为 。
(2)Y和Z可组成的化合物的化学式为 。
(3)写出铜和X的最高价氧化物水化物稀溶液反应的离子方程式 。
(4)W最高价氧化物水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28mol电子转移时,共产生9mol气体,写出该反应的化学方程式 。
II.若Y和z的核外电子数之和为22
(1)Y的气态氢化物电子式为 ,工业合成该物质的化学方程式为 。
(2)将X的最高价氧化物通人到苯酚钠溶液中,实验现象是 。
(3)X单质与W的最高价氧化物水化物的浓溶液反应,当电:子转移0.4mol时,产生气体的体积(标准状况下)是 。
25.(16分)
以A和乙醇为有机基础原料,合成香料甲的流程图如下:
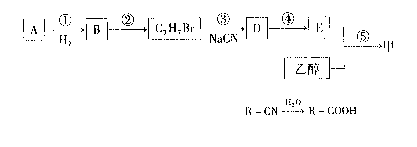
已知:R-Br+NaCN→R→CN+NaBr;
杏仁中含有A,A能发生银镜反应。质谱测定,A的相对分子质量为106。5.3g A完全
燃烧时,生成15.4g CO:和2.7g HO。
(1)A的分子式为 ,A发生银镜反应的化学方程式为 。
(2)写出反应②的化学方程式 。
(3)上述反应中属于取代反应的是: 。
(4)符合下列条件的E的同分异构体有 种;
a.能发生银镜反应 b.不含Cu c.不能水解
写出其中2种结构简式
(5)写出反应⑤的化学方程式 。
24.(18分)把一个质量为m、带正电荷且电量为q的小物块m放在一个水平轨道的P点上,在轨道的O点有一面与轨道垂直的固定墙壁。轨道处于匀强电场中,电场强度的大小为E,其方向与轨道(ox轴)平行且方向向左。若把小物块m从静止状态开始释放,它能够沿着轨道滑动。已知小物块m与轨道之间的动摩擦因数μ,P点到墙壁的距离为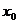 ,若m与墙壁发生碰撞时,其电荷q保持不变,而且碰撞为完全弹性碰撞(不损失机械能)。求:
,若m与墙壁发生碰撞时,其电荷q保持不变,而且碰撞为完全弹性碰撞(不损失机械能)。求:
(1)如果在P点把小物块从静止状态开始释放,那么它第1次撞墙后瞬时速度为零的位置坐标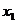 、第2次撞墙之后速度为零的位置坐标
、第2次撞墙之后速度为零的位置坐标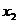 的表达式分别是什么?
的表达式分别是什么?
(2)如果在P点把小物块从静止状态开始释放,那么它最终会停留在什么位置?从开始到最后它一共走了多少路程(s)?
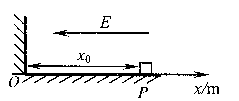 (3)如果在P点瞬间给小物块一个沿着x轴向右的初始冲量,其大小设为I,那么它第一次又回到P点时的速度(
(3)如果在P点瞬间给小物块一个沿着x轴向右的初始冲量,其大小设为I,那么它第一次又回到P点时的速度(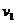 )大小为多少?它最终会停留在什么位置?从开始到最后它一共走了多少路程
)大小为多少?它最终会停留在什么位置?从开始到最后它一共走了多少路程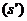 ?
?
23.(18分)下图为汤姆生在1897年测量阴极射线(电子)的荷质比时所用实验装置的示意图。K为阴极,A1和A2为连接在一起的中心空透的阳极,电子从阴检发出后被电场加速,只有运动方向与A1和A2的狭缝方向相同的电子才能通过,电子被加速后沿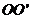 方向垂直进入方向互相垂直的电场、磁场的叠加区域。磁场方向垂直纸面向里,电场极板水平放置,电子在电场力和磁场力的共同作用下发生偏转。已知圆形磁场的半径为R,圆心为C。
方向垂直进入方向互相垂直的电场、磁场的叠加区域。磁场方向垂直纸面向里,电场极板水平放置,电子在电场力和磁场力的共同作用下发生偏转。已知圆形磁场的半径为R,圆心为C。
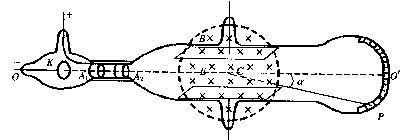
某校物理实验小组的同学们利用该装置,进行了以下探究测量:
首先他们调节两种场强的大小:当电场强度的大小为E,磁感应强度的大小为B时,使得电子恰好能够在复合场区域内沿直线运动;然后撤去电场,保持磁场和电子的速度不变,使电子只在磁场力的作用下发生偏转,打要荧屏上出现一个亮点P,通过推算得到电子的偏转角为α(即: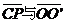 之间的夹角)。若可以忽略电子在阴极K处的初速度,则:
之间的夹角)。若可以忽略电子在阴极K处的初速度,则:
(1)电子在复合场中沿直线向右飞行的速度为多大?
(2)电子的比荷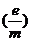 为多大?
为多大?
(3)利用上述已知条件,你还能再求出一个其它的量吗?若能,请指出这个量的名称。
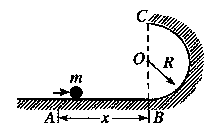
22.(16分)如图所示,在光滑水平面右端拱点处连接一个竖直的半径为冗的光滑半圆形轨
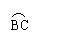
道 ,在距离B为x的A点,用一个较大的水平力向右瞬间弹击质量为m的小钢球,使其获得一个水平向右的初速度,质点到达廖点后沿半圆形轨道运动,经过C点后在空中飞行,正好又落回到A点。求:
(1)小钢球经过C时的速度有多大?
(2)小钢球经过B时的速度有多大?
 (3)在4点,这个瞬间弹击小钢球的力的冲量需要有多大?
(3)在4点,这个瞬间弹击小钢球的力的冲量需要有多大?
21.(20分)
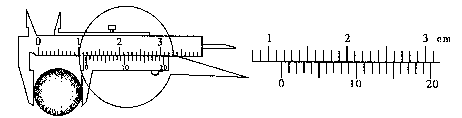
(1)(6分)从下图中读出球的直径是 mm。
(2)(14分)有一个量程为3V的电压表,代号为④,经过初步粗测其内阻大约为3kn,现在的任务是:测出该电压表内阻的精确值。现在实验室可提供的器材有:
①取值范围为0.1Ω到9999.9Ω,最大电流为0.1A,代号为Ra的电阻箱一台;
②最大电阻为1000Ω最大电流为0.2A,代号为尺Rb的滑动变阻器一个;
③开路电压约为5V、内阻可忽略不计的电源一个,代号为E;
④代号为K的电键一个;
⑤供连接用的导线若干条。
要求:
(a)在这些器材中,适当选择有用的器材,设计一个简便易行的测量电路,画出电路图
并标出所用器材的代号。
(b)列出测量步骤:并写出计算电压表内阻的最终表达式。
20.如图所示,在匀强磁场B中放一电阻不计的平行金
属导轨,导轨跟固定的大导体环M相连接,导轨上
放一根金属导体棒ab并与导轨紧密接触,磁感应线
垂直于导轨所在平面。若导体棒匀速地向右做切割磁
感线的运动,则在此过程中M所包围的固定闭合导
体环N内 ( )
A.产生顺时针方向的感应电流 B.产生交变电流
C.产生逆时针方向的感应电流 D.没有感应电流
第Ⅱ卷(非选择题共180分)
本卷共11小题,共180分。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com