
9.下列说法中,不正确的是( )
A.在NaAlO2溶液中,HCO3-不可能大量存在
B.在0.1mol·L-1的氢溴酸中加入适量的蒸馏水,溶液的c(H+)减小
C.在由水电离出的c(OH-)=1×10-12mol·L-1的溶液中,Al3+不可能大量存在
D.室温下pH=6的酸性溶液中,可能存在NH3·H2O分子
8.已知:⑴ Na2HPO3是正盐,可水解;⑵ H3C=2H++HC2-,HC2-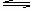 H++C3-,则下列说法不正确的是( )
H++C3-,则下列说法不正确的是( )
A.若存在Na2HPO3和Na2HC混合液,则其既能与强酸反应,又能与强碱反应
B.溶液NaH2C呈酸性
C.可能存在Na2HPO3和 NaH2C混合液
D.溶液Na2HC呈酸性
7.(06四县市联考)已知NaHSO3溶液和Na2CO3溶液混合后加热煮沸能产生CO2气体。现有浓度均为0.1mol/L的NaHSO3溶液和NaHCO3溶液,两溶液中各粒子物质的量浓度的关系一定正确的是(R表示S或C) ( )
A.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
B.c(H+)+c(H2RO3)=c(RO32-)+c(OH-)
C.c(Na+) >c(HRO3-) >c(H+) >c(OH-)>c(RO32-)
D.c(HRO3-)>c(H2RO3)>c(OH-)>c(RO32-)>c(H+)
6.(05上海)叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是( )
A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-)
B.HN3与NH3作用生成的叠氮酸铵是共价化合物
C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+)
D.N3-与CO2含相等电子数
5.(06江苏卷)下列叙述正确的是( )
A.0.1mol·L-1氨水中,c(OH-)=c(NH4+)
B.10 mL 0.02mol·L-1HCl溶液与10 mL 0.02mol·L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
C.在0.1mol·L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
4.一种一元强酸HA溶液中加入一种碱MOH反应后,溶液呈中性,下列判断正确的( )
A.加入的碱过量 B.混合前酸与碱中溶质的物质的量相等
C.生成的盐不发生水解 D.反应后溶液中A-、M+物质的量浓度相等
3.将0.2mol/L的KOH溶液与0.1mol/L的H2SO3溶液等体积混合后,溶液中各粒子浓度大小关系不正确的是( )
A.c(K+)+c(H+)=c(OH-)+c(HSO3-)+c(SO32-)
B.c(K+)+c(OH-)=c(H+)+2c(SO32-)+3c(HSO3-)+4c(H2SO3)
C.c(K+)>c(SO32-)>c(HSO3-)>c(H2SO3)
D.c(SO32-)+c(HSO3-)+c(H2SO3)=0.1mol/L
2.某无色溶液中可以大量共存的离子组是( )
A.Mg2+、Al3+、HCO3-、SO32- B.K+、Ca2+、MnO4-、Cl-
C.Ba2+、Na+、AlO2-、NO3- D.NH4+、Fe3+、SO42-、SCN-
1.若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是( )
A.生成了一种强酸弱碱盐 B.弱酸溶液和强碱溶液反应
C.弱酸溶液和弱碱溶液反应 D.一元强酸溶液和一元强碱溶液反应
6.请用多种方法证明CH3COOH是弱酸。
[课后作业]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com