
ΗΏ÷–”οΈΡΩΦΗΌ“Σ«σΩΦ…ζΡήΕ‘ΥυΗχΒΡΙ≈¥ζ ΪΈΡΒΡΥΦœκΡΎ»ίΫχ––ΤάΥΒΘ§Ε‘Τδ–ΈœσΓΔ”ο―‘ΦΑ±μ¥οΦΦ«…Ϋχ––…ΆΈωΓΘΤάΦέΉςΤΖΒΡΥΦœκΡΎ»ίΑϋά®Η≈ά®÷ς÷ΦΓΔΦρΈωΉςΤΖΒΡ’ΰ÷Έ“β“εΓΔΥΦœκ“β“εΓΔ»Υ…ζ“β“εΘ§…ΆΈωΉς’ΏΒΡ…ζΜν«ι»ΛΓΔ…σΟά«ι»ΛΚΆ“’ θΖγΗώΓΘ’βΨΆ“Σ«σΩΦ…ζΡή’ΐ»ΖΑ―Έ’ΉςΤΖΒΡΥΦœκ«ιΗ–Θ§≤Δ”ΟΙφΖΕΒΡ±μ ω¥πΧβΓΘ
Ι≈ Ϊ¥ ÷–Υυ±μ¥οΒΡΥΦœκ«ιΗ–Θ§Ω…ΡήΝς¬Ε‘ΎΧβΡΩ…œΓΔ Ϊ―έ…œΓΔ“βœσ…œΘ§Ά§ ±“≤”κΉς’Ώ…ζΜνΒΡ…γΜαΜΖΨ≥ΚΆΉ‘ΦΚΒΡ…ζΜνΨ≠άζœΔœΔœύΙΊΘ§“ρ¥Υ‘ΎΤάΦέΉςΤΖΒΡΥΦœκΡΎ»ί ±Θ§“ΣΉΞΉΓ Ϊ―έΓΔΖ÷Έω“βœσΓΔ’ϊΧεΑ―Έ’Θ§≤ΔΫαΚœΉΔ ΆΓΔ÷Σ»Υ¬έ ΪΓΘΈΣ¥ΥΘ§ΗυΨίΩΈ±ξ÷–ΓΑ÷Σ ΕΚΆΡήΝΠΓΔΙΐ≥ΧΚΆΖΫΖ®ΓΔ«ιΗ–Χ§Ε»ΚΆΦέ÷ΒΙέΓ±»ΐΗωΈ§Ε»ΒΡ“Σ«σΘ§±ΨΧΟΩΈΒΡΫΧ―ßΡΩ±ξ»ΖΕ®ΈΣΘΚ
1Θ°ΓΓΓΓΓΓΓΓΓΓΓΓ »Ο―ß…ζΑ―Έ’άμΫβ ΪΗη«ιΗ–ΒΡ«–»κΒψΘΜ
15Θ°(12Ζ÷)»γœ¬ΆΦΥυ ΨΘ§Α― ‘ΙήΖ≈»κ Δ”–ΒΡ±ΞΚΆ ·Μ“Υ°»ή“ΚΒΡ…’±≠÷–Θ§”ΟΧζΦ–ΙΧΕ®ΚΟΓΘ‘Ύ ‘Ιή÷–Ζ≈»κΦΗΤ§ΟΨΧθΘ§‘ΌΒΈ»κ10 mL―ΈΥα”Ύ ‘Ιή÷–ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
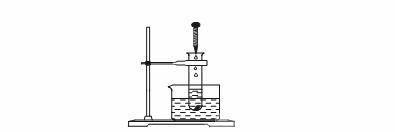
(1) Β―ι÷–Ιέ≤λΒΫΒΡœ÷œσ «_______________________________ΓΘ
ΓΓ(2)≤ζ…ζ…œ ωœ÷œσΒΡ‘≠“ρ «_______________________________ΓΘ
(3)»γΙϊΑ―4.8gΟΨΆΕ»κ≈®Ε»ΈΣ2.5mol/l ΒΡ 200mLœΓ―ΈΥα÷–Θ§Ζ≈≥ωΒΡH2‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐΈΣ____ΓΘ
(4)ΫΪ…ζ≥…ΒΡH2Ά®ΙΐΙΐΝΩΒΡΉΤ»»CuOΘ§ΦΌ…ηΖ¥”ΠΆξ»ΪΘ§‘ρ±ΜΜΙ‘≠≥ωΒΡΆ≠ΒΡ÷ ΝΩΈΣ__________ΓΘ

 ΓΓ
ΓΓ
14Θ° ≥ΘΈ¬œ¬Θ§ΫΪNaC1÷ ΝΩΖ÷ ΐΈΣ14.0%ΒΡ»ή“Κ20.0g”κ NaCl÷ ΝΩΖ÷ ΐΈΣ24.0%ΒΡ»ή“Κ30.0gΜλΚœΘ§ΒΟΒΫΟήΕ»ΈΣ
≥ΘΈ¬œ¬Θ§ΫΪNaC1÷ ΝΩΖ÷ ΐΈΣ14.0%ΒΡ»ή“Κ20.0g”κ NaCl÷ ΝΩΖ÷ ΐΈΣ24.0%ΒΡ»ή“Κ30.0gΜλΚœΘ§ΒΟΒΫΟήΕ»ΈΣ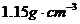 ΒΡΜλΚœ»ή“ΚΘ§ΦΤΥψΘΚ
ΒΡΜλΚœ»ή“ΚΘ§ΦΤΥψΘΚ
(1)ΗΟ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»ΓΘ
(2)‘Ύ1000gΥ°÷––η»ή»κΕύ…ΌmolNaClΘ§≤≈Ρή ΙΤδΈο÷ ΒΡΝΩ≈®Ε»«ΓΚΟ”κ …œ ωΜλΚœ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»œύΒ»ΘΩ
…œ ωΜλΚœ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»œύΒ»ΘΩ
ΫβΈωΘΚ(1)ΜλΚœ»ή“Κ÷–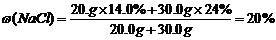
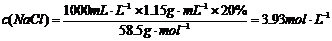
(2)…η–η»ήΫβxmolNaClΓΘ‘ρ ΓΓΓΓΓΓ
x=4.27mol
ΓΓΓΓΓΓ
x=4.27mol
¥πΑΗΘΚ(1)ΜλΚœ»ή“ΚΈο÷ ΒΡΝΩ≈®Ε»ΈΣ ΓΘ
ΓΘ
(2)1000gΥ°÷–Φ”4.27molNaClΘ§Φ¥Ω…ΒΟΒΫ”κ…œ ωΜλΚœ“Κ≈®Ε»œύΆ§ΒΡ»ή“ΚΓΘ
12. (2010ΓΛ Κ”±± ·Φ“ Ή·)ΫΪ100g≈®Ε»ΈΣ18molΓΛLΘ≠1ΓΔΟήΕ»ΈΣΠ―gΓΛcm-3ΒΡ≈®ΝρΥαΦ”»κΒΫ“ΜΕ®ΝΩΒΡΥ°÷–Θ§ Ι÷°œΓ Ά≥…9molΓΛLΘ≠1ΒΡΝρΥαΘ§‘ρ–ηΥ°ΒΡΧεΜΐΈΣ(ΓΓΓΓ )
Ή·)ΫΪ100g≈®Ε»ΈΣ18molΓΛLΘ≠1ΓΔΟήΕ»ΈΣΠ―gΓΛcm-3ΒΡ≈®ΝρΥαΦ”»κΒΫ“ΜΕ®ΝΩΒΡΥ°÷–Θ§ Ι÷°œΓ Ά≥…9molΓΛLΘ≠1ΒΡΝρΥαΘ§‘ρ–ηΥ°ΒΡΧεΜΐΈΣ(ΓΓΓΓ )
AΘ°–Γ”Ύ100mLΓΓΓΓΓΓ BΘ°Β»”Ύ100mLΓΓΓΓ
CΘ°¥σ”Ύ100mLΓΓΓΓΓΓ DΘ°Β»”Ύ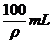

1 3. (2010ΓΛΡΰœΡ“χ¥®)
3. (2010ΓΛΡΰœΡ“χ¥®)
(1)”Ο18molΓΛLΘ≠1ΒΡΝρΥα≈δ÷Τ100mL1.0molΓΛL Θ≠1ΝρΥαΘ§»τ Β―ι“«Τς”–ΘΚ
Θ≠1ΝρΥαΘ§»τ Β―ι“«Τς”–ΘΚ
AΘ°100mLΝΩΆ≤ΓΓ BΘ°Ά–≈ΧΧλΤΫΓΓ CΘ°≤ΘΝßΑτΓΓ DΘ°50mL»ίΝΩΤΩΓΓ EΘ°10mLΝΩΆ≤ΓΓ
ΓΓFΘ°ΫΚΆΖΒΈΙήΓΓ GΘ°50mL…’±≠ΓΓ HΘ°100mL»ίΝΩΤΩ
Β―ι ±”ЯÔϓ«ΤςΒΡœ»ΚσΥ≥–ρ «(Χν»κ±ύΚ≈)_______ __________________ΓΘ
__________________ΓΘ
(2)‘Ύ»ίΝΩΤΩΒΡ Ι”ΟΖΫΖ®÷–Θ§œ¬Ν–≤ΌΉς≤Μ’ΐ»ΖΒΡ «(Χν–¥±ύΚ≈)_________________ΓΘ
AΘ° Ι”Ο»ίΝΩΤΩ«ΑΦλ≤ιΥϋ «Ζώ¬©Υ°
BΘ°»ίΝΩΤΩ”Ο’τΝσΥ°œ¥ΨΜΚσΘ§‘Ό”Ο¥ΐ≈δ»ή“Κ»σœ¥
CΘ°≈δ÷Τ»ή“Κ ±Θ§»γΙϊ ‘―υ «ΙΧΧεΘ§Α―≥ΤΚΟΒΡ ‘―υ”Ο÷ΫΧθ–Γ–ΡΒΙ»κ»ίΝΩΤΩ÷–Θ§ΜΚ¬ΐΦ”»κ’τΝσΥ°ΒΫΫ”Ϋϋ±ξœΏ2cm-3cm¥ΠΘ§”ΟΒΈΙήΒΈΦ”’τΝσΥ°ΒΫ±ξœΏ
DΘ°≈δ÷Τ»ή“Κ ±Θ§»γΙϊ ‘―υ «“ΚΧεΘ§”ΟΝΩΆ≤ΝΩ»Γ ‘―υΚσ÷±Ϋ”ΒΙ»κ»ίΝΩΤΩ÷–Θ§ΜΚ¬ΐΦ”»κ’τΝσΥ°ΒΫΫ”Ϋϋ»ίΝΩΤΩΩΧΕ»±ξœΏ1cm-2cm¥ΠΘ§”ΟΒΈΙήΒΈΦ”’τΝσΥ°ΒΫΩΧΕ»œΏ
EΘ°Η«ΚΟΤΩ»ϊΘ§”Ο ≥÷ΗΕΞΉΓΤΩ»ϊΘ§”ΟΝμ“Μ÷Μ ÷ΒΡ ÷÷ΗΆ–ΉΓΤΩΒΉΘ§Α―»ίΝΩΤΩΒΙΉΣΚΆ“ΓΕ·Εύ¥Έ
11. (2010ΓΛΚ”Ρœ÷Θ÷ί)œύΕ‘Ζ÷Ή”÷ ΝΩΈΣMΒΡΡ≥»ή÷ ‘Ύ “Έ¬œ¬ΒΡ»ήΫβΕ»ΈΣSg/100gΥ°Θ§¥Υ ±≤βΒΟ±ΞΚΆ»ή“ΚΒΡΟήΕ»ΈΣ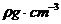 Θ§‘ρΗΟ±ΞΚΆ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε» «(ΓΓΓΓ )
Θ§‘ρΗΟ±ΞΚΆ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε» «(ΓΓΓΓ )
AΘ°molΓΛLΘ≠1ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°molΓΛLΘ≠1
CΘ° molΓΛLΘ≠1ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°molΓΛLΘ≠1

10.(2010ΓΛ±±Ψ©Ές≥«)Ρ≥―ß…ζ≈δ÷Τ100mL1 molΓΛLΘ≠1ΒΡΝρΥα»ή“ΚΘ§Ϋχ––œ¬Ν–≤ΌΉςΘ§»ΜΚσΕ‘»ή“Κ≈®Ε»ΉςΨΪ»Ζ≤βΕ®Θ§ΖΔœ÷’φ Β≈®Ε»–Γ”Ύ1 molΓΛLΘ≠1Θ§ΥϊΒΡœ¬Ν–≤ΌΉς÷– Ι≈®Ε»ΤΪΒΆΒΡ‘≠“ρ «(ΓΓ )
ΔΌ”ΟΝΩΆ≤ΝΩ»Γ≈®ΝρΥα ±Θ§Η© ”ΕΝ ΐΓΘ
ΔΎΝΩΆ≤÷–≈®ΝρΥα»Ϊ≤ΩΉΣ»κ…’±≠÷–œΓ ΆΚσΘ§‘ΌΉΣ“ΤΒΫ1 00mL»ίΝΩΤΩ÷–Θ§…’±≠Έ¥œ¥Β”ΓΘ
00mL»ίΝΩΤΩ÷–Θ§…’±≠Έ¥œ¥Β”ΓΘ
Δέ”Ο≤ΘΝßΑτ“ΐΝςΘ§ΫΪ»ή“ΚΉΣ“ΤΒΫ»ίΝΩΤΩ÷–”–»ή“ΚΝςΒΫΝΥ»ίΝΩΤΩΆβΟφΓΘ
Δή≈®ΝρΥα‘Ύ–Γ…’±≠÷–œΓ ΆΚσΘ§ΟΜ”–ά以آ¬μ…œΉΣ“Τ»κ»ίΝΩΤΩΓΘ
Δί”ΟΫΚΆΖΒΈΙήΦ”’τΝσΥ° ±Θ§Φ”»κΙΐΩλΕχ Ι“ΚΟφ≥§ΙΐΝΥΩΧΕ»œΏΘ§ΝΔΦ¥”ΟΒΈΙήΈϋ»ΞΕύ”ύΒΡΥ°Θ§ Ι»ή“ΚΑΦΟφΗ’ΚΟ”κΩΧΕ»œΏœύ«–ΓΘ
ΔόΒΈΦ”»κ’τΝσΥ°Θ§ Ι»ή“ΚΑΦΟφΗ’ΚΟ”κΩΧΕ»œΏœύ«–Θ§Η«…œΤΩ»ϊΖ¥Η¥“Γ‘»ΚσΘ§Ψ≤÷ΟΘ§ΖΔœ÷“ΚΟφ±»ΩΧΕ»œΏΒΆΘ§‘ΌΦ”Υ°÷ΝΩΧΕ»œΏΓΘ
AΘ°ΔΎΔέΔήΔίΔόΓΓΓΓΓΓ BΘ°ΔΌΔΎΔέΔίΔόΓΓΓΓ CΘ°ΔΎΔέΔίΔόΓΓΓΓΓΓΓΓ DΘ°ΔΌΔΎΔέΔήΔί
ΫβΈωΘΚΔΌΗ© ”ΝΩΆ≤ΕΝ ΐ»Γ“ΚΜαΤΪ…ΌΔΎ…’±≠÷–”–≤–ΝτΥαΔέΉΣ“ΤΙΐ≥Χ÷–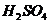 Υπ ßΔή≤ΘΝß≈ρ’Ά±»“ΚΧε≈ρ’Ά ήΈ¬Ε»”Αœλ¥σΔίΈϋΥ° ±¥χ≥ωΝΥΝρΥαΔό‘≠ά¥Φ”Υ°ΒΡΝΩ’ΐΚΟΘ§“Γ‘»ΚσΤΪ…Ό «“ρΈΣ“ΚΧε’≥ΒΫΤΩ±Ύ…œΘ§‘ΌΦ”Υ°ΨΆΤΪΕύΓΘ
Υπ ßΔή≤ΘΝß≈ρ’Ά±»“ΚΧε≈ρ’Ά ήΈ¬Ε»”Αœλ¥σΔίΈϋΥ° ±¥χ≥ωΝΥΝρΥαΔό‘≠ά¥Φ”Υ°ΒΡΝΩ’ΐΚΟΘ§“Γ‘»ΚσΤΪ…Ό «“ρΈΣ“ΚΧε’≥ΒΫΤΩ±Ύ…œΘ§‘ΌΦ”Υ°ΨΆΤΪΕύΓΘ
¥πΑΗΘΚB
9. (‘≠¥¥) Β―ι‘±”ϊΫΪ»ή“Κ≈®Ε»‘ω¥σΘ§Α―≈®Ε»ΈΣA%ΒΡKOH»ή“Κ’τΖΔΒτW gΥ°ΚσΘ§≥…ΈΣV mLΒΡ2A%ΒΡKOH»ή“ΚΘ§‘ρ’τΖΔΚσΒΡ»ή“ΚΤδΈο÷ ΒΡΝΩ≈®Ε»ΈΣ(ΓΓ)
A.ΓΓ molΓΛLΘ≠1ΓΓ ΓΓ B. molΓΛLΘ≠1 ΓΓΓΓ
C. molΓΛLΘ≠1ΓΓΓΓ ΓΓΓΓΓΓ D. molΓΛLΘ≠1
ΫβΈωΘΚ…η’τΖΔ«Α»ή“ΚΒΡ÷ ΝΩ ΈΣx g‘ρΘΚxA%=(xΘ≠W)2A%,ΫβΒΟ:x=2W(g)Θ§‘ρ’τΖΔΚσ»ή“ΚΒΡ≈®Ε»c(KOH)=n(KOH)/V=
ΈΣx g‘ρΘΚxA%=(xΘ≠W)2A%,ΫβΒΟ:x=2W(g)Θ§‘ρ’τΖΔΚσ»ή“ΚΒΡ≈®Ε»c(KOH)=n(KOH)/V=
 m
m ol/LΓΘ
ol/LΓΘ
¥πΑΗΘΚA
8. (2010ΓΛΙψΕΪ…νέΎ)20Γφ ±Θ§±ΞΚΆKCl»ή“ΚΒΡΟήΕ»ΈΣ1.174 gΓΛcmΘ≠3Θ§Έο÷ ΒΡΝΩ≈®Ε»ΈΣ4.0 molΓΛLΘ≠1Θ§‘ρœ¬Ν–ΥΒΖ®÷–≤Μ’ΐ»ΖΒΡ «
(ΓΓ )ΓΓΓΓ
(2010ΓΛΙψΕΪ…νέΎ)20Γφ ±Θ§±ΞΚΆKCl»ή“ΚΒΡΟήΕ»ΈΣ1.174 gΓΛcmΘ≠3Θ§Έο÷ ΒΡΝΩ≈®Ε»ΈΣ4.0 molΓΛLΘ≠1Θ§‘ρœ¬Ν–ΥΒΖ®÷–≤Μ’ΐ»ΖΒΡ «
(ΓΓ )ΓΓΓΓ
AΘ°25Γφ ±Θ§±ΞΚΆKCl»ή“ΚΒΡ≈®Ε»¥σ”Ύ4.0 molΓΛLΘ≠1
BΘ°¥Υ»ή“Κ÷–KClΒΡ÷ ΝΩΖ÷ ΐΈΣ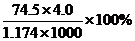
CΘ°20Γφ ±Θ§ΟήΕ»–Γ”Ύ1.174 gΓΛcmΘ≠3ΒΡKCl»ή“Κ «≤Μ±ΞΚΆ»ή “Κ
“Κ
DΘ°ΫΪ¥Υ»ή“Κ’τΖΔ≤ΩΖ÷Υ°Θ§‘ΌΜ÷Η¥ΒΫ20Γφ ±Θ§»ή“ΚΟήΕ»“ΜΕ®¥σ”Ύ1.174gΓΛcm-3
ΫβΈωΘΚΈ¬Ε»“ΜΕ®ΒΡΧθΦΰœ¬Θ§»ή“ΚΒΡ»ήΫβΕ»≤Μ±δΘ§≈®Ε»“≤≤Μ±δΘ§Υυ“‘ΟήΕ»“≤≤Μ±δΓΘ
¥πΑΗΘΚD
7. (2010ΓΛΫ≠Υ’ΡœΨ©)ΫΪ±ξΉΦΉ¥Ωωœ¬ΒΡaLHC1(ΤχΧε)Άξ»Ϊ»ή”Ύ1000gΥ°÷–Θ§ΒΟΒΫΒΡ―ΈΥαΟήΕ»ΈΣbgΓΛcm-3Θ§‘ρΗΟ―ΈΥαΒΡΈο÷ ΒΡΝΩ≈®Ε» «(ΓΓΓΓΓΓ
)
(2010ΓΛΫ≠Υ’ΡœΨ©)ΫΪ±ξΉΦΉ¥Ωωœ¬ΒΡaLHC1(ΤχΧε)Άξ»Ϊ»ή”Ύ1000gΥ°÷–Θ§ΒΟΒΫΒΡ―ΈΥαΟήΕ»ΈΣbgΓΛcm-3Θ§‘ρΗΟ―ΈΥαΒΡΈο÷ ΒΡΝΩ≈®Ε» «(ΓΓΓΓΓΓ
)
AΘ° molΓΛLΘ≠1ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ° molΓΛLΘ≠1
CΘ° molΓΛLΘ≠1ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ° molΓΛLΘ≠1
6. (2010ΓΛ…¬Ές
(2010ΓΛ…¬Ές ΈςΑ≤)“―÷ΣΡ≥±ΞΚΆ»ή“ΚΒΡΔΌ»ή“ΚΒΡ÷ ΝΩΔΎ»ήΦΝΒΡ÷ ΝΩΔέ»ή“ΚΒΡΧεΜΐΔή»ή÷ ΒΡΡΠΕϊ÷ ΝΩΔί»ή÷ ΒΡ»ήΫβΕ»Δό»ή“ΚΒΡΟήΕ»ΓΘœ¬Ν–”–ΙΊ“‘…œΧθΦΰΒΡΉιΚœΘ§Τδ÷–≤ΜΡήΦΤΥψ≥ωΗΟ±ΞΚΆ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»ΒΡ «(ΓΓΓΓ )
ΈςΑ≤)“―÷ΣΡ≥±ΞΚΆ»ή“ΚΒΡΔΌ»ή“ΚΒΡ÷ ΝΩΔΎ»ήΦΝΒΡ÷ ΝΩΔέ»ή“ΚΒΡΧεΜΐΔή»ή÷ ΒΡΡΠΕϊ÷ ΝΩΔί»ή÷ ΒΡ»ήΫβΕ»Δό»ή“ΚΒΡΟήΕ»ΓΘœ¬Ν–”–ΙΊ“‘…œΧθΦΰΒΡΉιΚœΘ§Τδ÷–≤ΜΡήΦΤΥψ≥ωΗΟ±ΞΚΆ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»ΒΡ «(ΓΓΓΓ )
AΘ°ΔΌΔΎΔέΔήΓΓΓΓΓΓΓΓ BΘ°ΔΌΔέΔήΔίΓΓΓΓΓΓΓΓ CΘ°ΔήΔίΔόΓΓΓΓΓΓΓΓ DΘ°ΔΌΔήΔό
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com